
刘亚丽,中国医学科学院北京协和医院副研究员。《医学参考报微生物与感染频道》编辑部副主任,全国细菌耐药监测学术委员会青年委员,ChiCAST秘书,北京医学会检验学会微生物与感染分会青年委员,《临床药物治疗杂志》审稿专家。主持国家级、省部级及校级课题8项,发表SCI及中文文章35篇,获省部级奖励5项,参加教材及书籍编写11部,共识撰写2篇,行标1项。

李进,检验师,中国医学科学院北京协和医院检验科。参与课题:科技基础资源调查专项“中国感染病原菌规范化分层监测体系建立与药物敏感性和耐药性现状调查”,“艾滋病和病毒性肝炎等重大传染病防治”重大专项-子课题“病原细菌与突发急性真菌感染高通量快速检测与应急筛检技术研究”等。研究方向:临床病原微生物耐药监测及流行病学研究。
【摘要】目的 比较两中心微量肉汤稀释法检测苛养菌体外药物敏感性试验结果的不一致性。方法 本试验选取两中心分别对相同菌株(流感嗜血杆菌、卡他莫拉菌、产单核细胞李斯特菌各30株)进行微量肉汤稀释法体外药物敏感性试验,比较其结果的基本一致率(EA%)、分类一致率(CA%)、极大错误率(VME%)、大错误率(ME%)及小错误率(MIE%)。结果 两中心流感嗜血杆菌体外药敏试验结果有3种抗菌药物CA%<90%,5种抗菌药物VME%>3%;卡他莫拉菌体外药物敏感性试验结果有1种抗菌药物CA%<90%,所有抗菌药物VME%<3%;产单核细胞李斯特菌所有抗菌药物体外药敏试验结果均可接受,即EA%≥90%、CA%≥90%、VME%<3%、ME3%。结论 两中心采用微量肉汤稀释法对相同菌株的体外药物敏感性试验结果存在较大差异。
【关键词】微量肉汤稀释法;苛养菌;体外药物敏感性试验
微量肉汤稀释法作为美国临床和实验室标准化协会(CLSI)推荐的体外药物敏感性试验的标准方法,在临床和科研中应用非常广泛,是获取菌株体外药物敏感性数据的重要手段[1]。然而随着跨区域、多中心协作的细菌体外药物敏感性研究项目的逐渐增多,不同中心对彼此结果的认可度成为一大突出问题。本次试验选取两家中心,采用微量肉汤稀释法对相同菌株进行体外药物敏感性试验并分析其差异[2]。
一、材料与方法
1. 菌株:从科技基础资源调查专项“中国感染病原菌规范化分层监测体系建立与药物敏感性和耐药性现状调查”建立的菌株库中选取流感嗜血杆菌、卡他莫拉菌、产单核细胞李斯特菌各30株进行本次试验。
2. 主要试剂与材料:本次试验用到的22种抗菌药物,两中心的氨苄西林(AMP)、舒巴坦(SUL)、克拉维酸(CLA)、氨曲南(ATM)、美洛培南(MEM)、四环素(TCY)、左氧氟沙星(LVX)、利福平(RIF)、环丙沙星(CIP)、头孢噻肟(CTX)、头孢他啶(CAZ)、青霉素(PEN)均来源于中国食品药品检定研究院;甲氧苄啶(TMP)、磺胺甲噁唑(SMX)、氯霉素(CHL)均来源于中国药品生物制品检定所;亚胺培南(IMP)均来源于美仑生物。两中心阳离子调节肉汤(CAMHB)均来源于美国BD公司,酵母粉、培养基添加剂均来源于赛默飞世尔科技公司。其余抗菌药物与材料来源见表1。
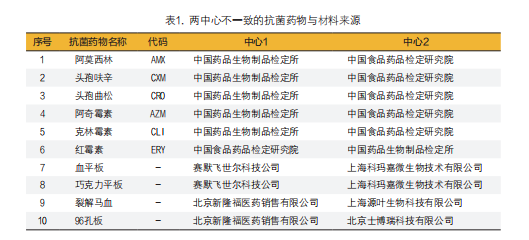
3. 方法:本研究选择两个实验室(中心1和中心2)进行开展,两中心对流感嗜血杆菌、卡他莫拉菌、产单核细胞李斯特菌各30株进行微量肉汤稀释法体外药物敏感性试验。本试验采用相同的药物浓度梯度,根据CLSI M07-A11[3]的要求进行药敏板配置。
将冻存菌株复苏后,再次传代,流感嗜血杆菌接种于巧克力平板,卡他莫拉菌和产单核细胞李斯特菌接种于血平板,35℃ 5%CO2孵育20~24h。挑取单个菌落,制备0.5麦氏浊度菌悬液,流感嗜血杆菌菌悬液加入HTM肉汤中,卡他莫拉菌菌悬液加入CAMHB肉汤中,产单核细胞李斯特菌菌悬液加入马血肉汤中,颠倒混匀后分别接种于各自的96孔药敏板中,35℃孵育20~24h,读取抗菌药物的最低抑菌浓度(MIC)。
4. 统计分析:以中心1为对比方法,计算两中心体外药物敏感性试验结果浓度梯度的差值。统计两中心同种抗菌药物体外药物敏感性试验结果浓度梯度差值的基本一致率(EA%)和分类一致率(CA%)[4-6],判定标准按照已有文献,结果可接受标准为:CA%≥90%、EA%≥90%、VME%<3%、ME%<3%[6]。体外药物敏感性判定折点参照CLSI M100 31st和M45 3rd[7-8]。
二、结果
以中心1为对比方法,中心2为待测方法进行统计,计算两中心体外药物敏感性试验结果的基本一致率和分类一致率(表2和表3)。
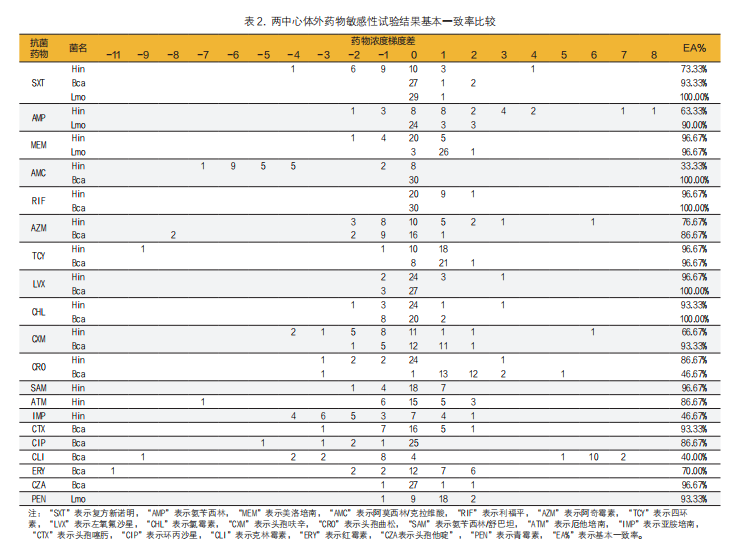
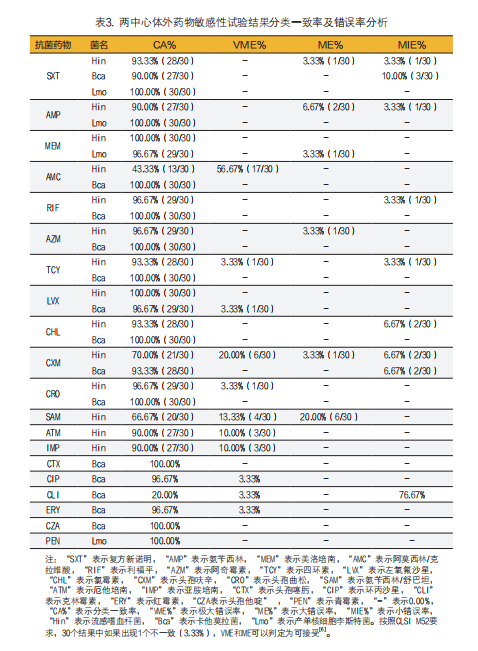
1. 两中心流感嗜血杆菌微量肉汤稀释法体外药敏结果不一致分析:EA%<90%的抗菌药物有头孢曲松、氨曲南、阿奇霉素、复方新诺明、头孢呋辛、氨苄西林、亚胺培南、阿莫西林/克拉维酸。CA%<90%的抗菌药物有头孢呋辛、氨苄西林/舒巴坦、阿莫西林/克拉维酸;VME%>3%的抗菌药物有阿莫西林/克拉维酸、头孢呋辛、氨苄西林/舒巴坦、氨曲南、亚胺培南;ME%>3%的抗菌药物有氨苄西林/舒巴坦、氨苄西林。
2. 两中心卡他莫拉菌微量肉汤稀释法体外药敏结果不一致分析:EA%<90%的抗菌药物有阿奇霉素、环丙沙星、红霉素、头孢曲松、克林霉素。CA%<90%的药有克林霉素;所有抗菌药物体外药物敏感性试验结果的VME%和ME%均在可接受范围内。
3. 两中心产单核细胞李斯特菌微量肉汤稀释法体外药敏结果不一致分析:本次试验中所有抗菌药物体外药物敏感性试验结果的EA%、CA%、VME%和ME%均在可接受范围内。
三、讨论
本试验结果显示,两中心美洛培南、四环素、左氧氟沙星、氯霉素、利福平5种抗菌药物对流感嗜血杆菌和卡他莫拉菌体外药物敏感性结果的EA%和CA%均在90%以上,结果较稳定,受环境、人员等因素影响较小。两中心卡他莫拉菌克林霉素的体外药物敏感性结果的EA%为40.00%,CA%为20.00%,结果差异较大。此外,两中心阿莫西林/克拉维酸、头孢呋辛两种抗菌药物对卡他莫拉菌体外药物敏感性试验结果的EA%和CA%均在90%以上,结果较稳定;而流感嗜血杆菌阿莫西林/克拉维酸、头孢呋辛的体外药物敏感性试验结果的VME%分别为56.67%和20.00%,结果一致性较差。对于该研究发现的不一致结果,我们推测可能与样本量较小、抗菌药物稳定性差、抗菌药物来源不同、菌种差异、以及不同操作人员对结果判读存在差异等因素有关。获得待测细菌准确的体外药敏试验结果对临床用药和科学研究都至关重要,微量肉汤稀释法作为CLSI推荐的体外药物敏感性试验的标准方法,在临床和科研中应用非常广泛。该研究提示,即使采用相同参考标准和实验流程,不同中心得到的微量肉汤稀释法结果仍存在较大差异,如何评估和判断其结果的可靠性仍面临较大挑战。
参考文献
Clinical And Laboratory Standards Institute(CLSI). Performance Standards for Antimicrobial Disk and Dilution Susceptibility Tests for Bacteria Isolated From Animals;Approved Standard--Fourth Edition[S].USA:National. Committee for Clinical Laboratory Standards,2013.
张筝, 赵俊杰, 李运喜, 等. 微量肉汤稀释法药敏试验的误差分析[J]. 中国抗菌药物杂志, 2016, 41(11): 858-864.
CLSI. Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria That Grow Aerobically.11th ed. CLSI standard M07. Wayne, PA: Clinical and Laboratory Standard Institute; 2018.
刘亚丽, 徐和平, 肖盟, 等. 2015-评估纸片扩散法与Vitek2-compact GN13测定肠杆菌科细菌体外药敏[J]. 中华微生物学和免疫学杂志, 2015, 35(2): 139-145.
刘亚丽, 张戈, 徐英春, 等. 5种国产与进口E-test药敏条的一致性比较. 临床检验技术研究[J]. 临床检验杂志, 2016, 34(11): 827-830.
CLSI. Verification of Commercial Microbial Identification and Susceptibility Testing Systems.1st ed. CLSI guideline M52. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.
CLSI. Performance Standards for Antimicrobial Susceptibility Testing. 31st ed. CLSI supplement M100. Clinical and Laboratory Standards Institute; 2021.
CLSI. Methods for Antimicrobial Dilution and Disk Susceptibility Testing of Infrequently Isolated or Fastidious Bacteria.3rd ed. CLSI guideline M45. Wayne, PA: Clinical and Laboratory Standards Institute; 2015.