一例由新冠病毒引发的血小板冷凝素病
怎么快速提高专业能力?
笔者认为有两点很重要,一个是与优秀的同行老师交流;另一点就是多读书。
现实情况是我们优秀的同行老师交流的机会总是那么难得,但还好,互联网为我们提供了机会,我们可以借助网络,读到优秀的老师们写的文章,这仍然不失为一种高效的学习方法。一来可以拓展视野,二来可以提高专业知识。
笔者已经养成了经常在数据库里检索一下与检验有关的文献。
昨天,笔者读到了法国法兰西岛哥伦比亚路易-穆里耶医院重症医学科的Yachar Dawudi发表在 BMJ Case Rep杂志上的一篇关于新冠病毒引发血小板凝集的病例。比较典型的冷凝集的案例。
文章报道了一例新冠肺炎重症患者血小板有严重的冷凝集现象,患者一度出现出现了急性呼吸窘迫综合征、急性肾衰竭和溶血性贫血。经血液检查,直接抗球蛋白试验呈阳性,冷凝集素滴度为1:512。未能明确病因。后经输血治疗,仍有持续的贫血。后续输注了单克隆抗C5抗体(Eculizumab,伊库利珠单抗)。伊库利珠单抗治疗几天后解决了患者的溶血问题,但最终病人死于严重的COVID-19感染。有关COVID-19期间冷凝集素病例报道较少,笔者尝试与大家分享这篇文献。
01 背景
2019年12月,中国首次发现新冠病毒,随后COVID-19迅速大流行,在世界范围内造成大量患者死亡。新冠病毒感染者的临床表现从无症状到危及生命的并发症,轻重程度不等。目前,对其病理生理学的理解仍不完整,但越来越多的证据表明,免疫反应受损和炎症失控可能是出现严重病例的原因。
02 病例介绍
患者男,有糖尿病、高血压和T细胞淋巴瘤(Sezary综合征B1期缓解期)病史,既往无溶血性贫血史,在出现急性呼吸窘迫综合征之前,有两周的持续发烧、咳嗽和疲劳症状。
胸部CT显示双侧肺栓塞和磨玻璃样变。给氧治疗未能缓解呼吸窘迫、神经系统紊乱和呼吸性酸中毒,遂行气管插管,以改善呼吸。
对气管内粘液进行RT-PCR检测,诊断为SARS-CoV-2感染。发病时,临床未发现任何皮肤病变或周围淋巴结。
患者的血红蛋白从第1天的109g/L下降到第4天的80g/L,并伴有急性肾衰竭。血小板计数保持正常。
乳酸脱氢酶(LDH)血清水平升高至2072 U/L(正常值<245 U/L),结合珠蛋白率低至17 mg/dL(正常值>56 mg/dL),网织红细胞计数升高至123.7×10^9 /L(正常值50-120×109 /L),证实贫血的性质。
鉴于溶血和肾衰竭同时存在,最初怀疑可能是血栓性微血管病,但后来由于血涂片检查未发现有红细胞碎片,肾活检未见单个肾小管坏死,因此被排除血栓性微血管病的可能。
随后进行了自身免疫性溶血性贫血相关检查。结果显示C3d强阳性,IgG直接抗球蛋白试验弱阳性。C3 56毫克/分升(正常范围80-170毫克/分升)和C4 8毫克/分升(正常范围12-40毫克/分升)补体部分和CH50 25U/毫升(正常范围25-100U/毫升)的减少表明补体经典途径被激活。
血涂片显示室温下红细胞明显凝集(图1)。
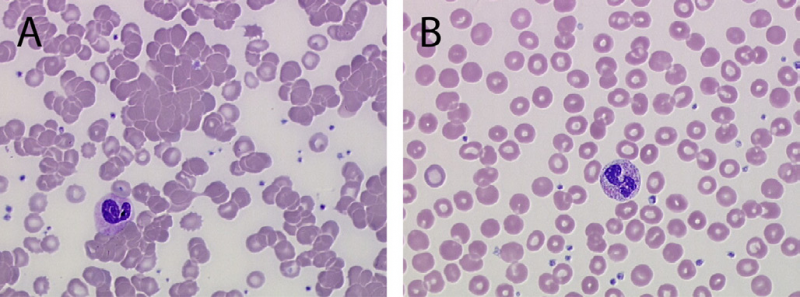
图一 (A) Eculizumab治疗前血涂片显示室温下有明显的红细胞凝集(吉姆萨染色,×40)(B) Eculizumab治疗后的血涂片检查显示无红细胞凝集(吉姆萨染色,×40)
诊断为冷凝集素病(CAD),两个冷凝集素滴度分别为1:128和1:512,具有抗I的特异性,进一步检查旨在确定CAD的基本病因。
首先鉴别诊断,没有证据表明是原发性CAD。寒冷引起的循环系统症状,如雷诺现象或感染过程中的急性贫血,90%发生在原发性CAD,本例患者无相关病史,可以排除寒冷引起CAD。
继发性CAD可能与血液系统疾病或感染性疾病有关。大多数CAD的病例是继发于血液病,如淋巴增生性疾病。肺炎支原体,呼吸道病毒感染也可能继发CAD。为了排除本例患者血液恶性肿瘤,对患者血液进行了淋巴细胞免疫分型,显示只有B型和T型淋巴细胞减少,无淋巴增生性疾病,特别是T细胞淋巴瘤。
血清电泳和免疫固定没未发现任何单克隆丙种球蛋白病。胸腹腔CT扫描没有淋巴结病或肿瘤。骨髓穿刺显示没有恶性浸润。同时,检测了导致CAD的一些可能的主要病毒。对气管内吸出物进行了多重PCR检测,包括检测流感病毒和肺炎支原体,结果为阴性。
还检测了丙型肝炎病毒和HIV血清学检测、B19副病毒的PCR检测,结果均为阴性。Epstein-Barr病毒和巨细胞病毒的PCR检测显示病毒复制有限(<3 log)。因此,除了SARS-CoV-2,未发现其他病原体。
总之,尽管无法正式确定因果关系,但仍支持COVID-19感染性导致的冷凝集素综合征的诊断。
03 病例处理
第8天诊断为CAD。CAD的溶血是由低温诱发的,因此最初的治疗包括对患者输注的所有液体进行加温,特别是输注的红细胞。为了支持骨髓再生,还增加了红细胞生成素治疗。
尽管进行了初步治疗,溶血仍然存在,LDH升高到1151 U/L,而且检测不到巯基血红蛋白。住院第10天,患者输注了悬浮红细胞,但没有血浆,尽管如此,患者的临床症状继续恶化,甚至出现了严重的心肺衰竭。随后医生讨论了治疗方案。但没有使用皮质类固醇,因为在CAD治疗指南中没有强烈的推荐级别,而且担心增加鼻腔感染的风险。
此外,该病例发生在不同的研究发表之前,这些研究显示了皮质类固醇治疗在COVID-19中的益处。该患者按照非COVID急性呼吸窘迫综合征(ARDS)的护理标准进行管理。由于利妥昔单抗的起效时间较长,所以没有选择它。血浆置换有血流动力学风险,而且患者已患有心力衰竭。因此,决定使用伊库利珠单抗治疗病人,它具有更好的效益/风险比,而且起效时间短。所以,第11天和第13天进行了伊库利珠单抗输液。
04 结果和随访
输注伊库利珠单抗一天后,溶血相关的指标降低(LDH 514U/L,haptoglobin 223mg/dL),血涂片检查显示没有红细胞凝集(图1)。在接下来的10天时间里,患者只输注了两个单位的红细胞。溶血现象减轻,没有复发。
不幸的是,由于COVID-19相关的ARDS和多器官衰竭(呼吸系统、肝脏、神经系统、心脏和肾脏衰竭),患者的病情恶化。家属做出取消生命支持的决定后,患者在入院后第33天死亡。
05 讨论
在本病例中,COVID-19引起的ARDS在短期内威胁患者生命。溶血可能加重了心脏和呼吸衰竭。考虑到利妥昔单抗相比伊库利珠单抗起效慢,以及类固醇对CAD无效的事实,选择用伊库利珠单抗治疗溶血症。
CAD的病理生理学主要涉及IgM抗体的激活。IgM抗体是强有力的补体激活能力。暴露在寒冷中会诱发红细胞上抗体的固定,从而引发经典补体途径的激活。C1q的结合诱导C2和C4的激活,导致C3b的形成,C3b与红细胞结合,通过渗透作用产生血管外溶血,主要是在肝脏。C3b还能激活C5,导致形成血管内溶血的膜攻击复合物。
伊库利珠单抗是一种抗C5的抗体,通过阻断膜攻击复合物的形成来抑制血管内溶血,但不会阻断血管外溶血。10多年来,伊库利珠单抗已被安全地用于各种补体介导的疾病,最近的研究表明,严重的COVID-19的呼吸功能恶化可能是由补体途径激活介导的微血管损伤引起的。本例患者出现了急性心力衰竭并伴有血流动力学不稳定,因此伊库利珠单抗似乎具有更好的风险效益比。虽然病人因严重的COVID-19感染而死亡,但由于没有复发溶血,临床仍可认为CAD已治愈。
COVID-19出现的两年多以来,重症病例仍然没有革命性的治疗方法。皮质类固醇治疗是唯一被证明对需要吸氧的病人有益的治疗方法之一。当出现CAD时,伊库利珠单抗可能是严重的COVID-19的一个正确选择,然而需要更多的研究来评估其疗效和安全性。
总之,在没有其他的CAD病因(未发现其他病毒,也未发现肿瘤)都表明SARS-CoV-2是我们病例中CAD的病因,即使不能明确证明。临床医生在面对异常血细胞计数异常时,应提高警惕,做好后续检查。对CAD的具体治疗策略,如伊库利珠单抗,应在更多的研究中进行评估,需要更多的研究来充分了解其基本作用机制。
06 总结
01 文章中提到了溶血性贫血,主要检测指标有乳酸脱氢酶(LDH);结合珠蛋白;
乳酸脱氢酶在红细胞破裂时会释放入血造成大幅升高,所以在生化检查时,此类受溶血影响较大的项目检验科对标本溶血是零容忍的,本篇文献却恰好可以利用LDH来判断有无溶血发生。
结合珠蛋白可用于诊断溶血性贫血,触珠蛋白浓度在溶血时会降低。血管内溶血时,结合珠蛋白降低的程度比血管外溶血更明显。严重溶血时,结合珠蛋白与血红蛋白结合而被彻底消耗,以至于血清中检测不到HP。因此,HP水平是评价溶血与否的敏感指标, 可用来检查溶血相关疾病,在阵发性睡眠性血红蛋白尿、血肿、组织出血、G-6PD缺乏症、巨红细胞性贫血时降低。
骨髓中红细胞系统的发育过程是:多能干细胞→单能干细胞→原始红细胞→早幼红细胞→中幼红细胞→晚幼红细胞→网织红细胞→成熟红细胞。网织红细胞增多表示骨髓红细胞系增生旺盛,常见于溶血性贫血、急性失血等。所以,本篇文献中特别提到了网织红细胞升高,可以作为贫血的诊断指标。
02 血栓性微血管病。它是一组急性临床综合征,呈微血管病性溶血性贫血、血小板减少及由于微循环中血小板血栓造成的器官受累表现。其突出的病理特点为小血管内皮细胞病变,表现为内皮细胞肿胀、官腔狭窄,部分小血管腔内可见血栓形成。病因多种多样,其发病机制不明确。常见肾损伤,红细胞碎片。本例患者血涂片未见红细胞碎片,也未见肾小管病变,固排除了血栓性微血管病。
03 血小板冷凝集。多数情况下,采集的血常规标本37度水浴后,可以纠正冷凝集现象,可以得到较为接近真实状况的血小板计数。或者采血后及时上机检测,也可以得到纠正。血小板凝集在血常规涂片检查中较为容易发现。但积极寻找血小板凝集的原因,是检验人重要学习的方向。
04 本例冷凝集素病(CAD)最终考虑可能为新冠病毒感染导致激活补体的经典途径,导致C3b与红细胞结合,通过渗透作用产生血管外溶血。C3b还能激活C5,导致形成血管内溶血的膜攻击复合物。
05 伊库利珠单抗是一种抗C5的抗体,通过阻断膜攻击复合物的形成来抑制血管内溶血。
编辑:骆秉涵



