行标学习 | WS/T442-2024临床实验室生物安全指南--风险评估
临床实验室生物安全风险评估参考示例A.1 风险评估总体要求 A.1.1 基本原则 本示例提供了基于定性分析的风险评估方法所形成的风险评估报告。定量和半定量的评估方法也可 以用于风险评估。实验室应使用最能满足其实际需求的评估方法,也可针对特定实验活动需求,开发个 性化评估方法、评分方法和评估指标体系。 A.1.2 风险评估前应首先明确参与风险评估的人员,本次风险评估适用的专业室、检验项目、标本类 型、可能涉及的病原微生物等危险因素,以及相应的实验活动。可以是具体某个特定的检验项目,也可 以是生物安全风险相同、实验流程及操作过程相同或相似的一组检验项目。 A.1.3 准备评审依据(参见WS/T 442《临床实验室生物安全指南》第4.1.5条):实验室生物安全管理 文件以及设施、设备及项目的相关信息(如检测仪器和项目的标准操作规程)等。 A.1.4 风险识别 A.1.4.1 识别临床标本可能存在的潜在病原微生物及其危害,包括传染性、传播途径、感染剂量、致 病性、在环境中的稳定性和对消毒剂的敏感性、治疗和预防措施;识别临床标本可能发生的职业暴露及其后果等。 A.1.4.2 识别检验工作全过程的实验活动的潜在风险,并对其特性进行描述,包括但不限于:a) 检验前过程:标本采集(采样空间、人员、标本类型、标本容器及要求)、标本暂存方法及安全措施,标本运输转运箱及要求;标本核收过程等。如采样空间不符合要求,采样人员手套破损、口罩选择不正确及佩戴不规范、采血时发生针刺伤,采样过程中发生标本迸溅,采样后 未注意手卫生,标本运输过程中发生泄露、溢洒或丢失等风险; b) 检验过程:标本离心、研磨、振荡、匀浆等处理;标本加样、转运、涂片、培养及鉴定、药 敏试验、锐器使用(玻璃器皿、剪刀、针头、移液管)、检测仪器运行状态等。如标本离心或离心管破碎产生气溶胶,使用注射器等锐器时发生针刺伤,各种原因产生的标本迸溅或溢洒等风险; c) 检验后过程及医疗废物处理:标本保存(保存管、保存条件、存放/调取管理、安全措施)、 标本处理方式(如高压灭菌、消毒等)及效果评估;物体表面和环境消毒方式、消毒剂浓度及作用时间;医疗废物包装容器质量,医疗废物转运、处理等。如标本发生溢洒、标本丢失、消 毒剂失效、医用垃圾袋泄露、医疗废物未按要求标识、仪器实验废水泄漏等风险;d) 相关人员:资质、经验、能力、健康状态等;个体防护装备使用规范性等。如使用高压灭菌器人员无资质,PCR 检测人员无资质,个体防护装备质量不达标、使用不规范等风险; e) 设施设备:离心机、高压灭菌器、生物安全柜、紫外消毒灯等设备设施的性能和状态,更衣 柜设置等。如上述设施设备状态异常、校准不合格,报废仪器未经消毒处理移出实验室等存在的风险;个人与工作服混放的污染风险等; f) 实验室环境:环境温度、湿度;采用机械通风时,空气换气次数、压力情况、定向气流稳定 性,中、高效过滤器使用时间及效果等。如环境温度过高导致人员晕倒;采用机械通风时,空气换气次数不足导致人员乏氧,压力错误导致污染外泄等风险; g) 安全管理:实验室人员准入措施;保存标本/菌(毒)株的冰箱或场所的安保措施等。如外来人员未经实验室批准和安全告知,擅自进入实验室;标本、菌(毒)株被盗或恶意使用带来的风险等。 h) 意外停电、发水、火灾等突发情况以及化学危害(如易燃易爆品、有毒性、刺激性或挥发性 物质)、物理危害(如高处物品掉落砸伤、高温、低温等)、自然灾害等风险。 A.1.5 风险分析A.1.5.1 依据《人间传染的病原微生物目录》对相关病原微生物危害程度分类,根据临床检验过程中 各种感染性材料和实验活动的特点,对风险涉及事件发生的可能性及其后果的严重性进行分析。依据风 险涉及事件发生的可能性,分为Ⅰ-Ⅴ五个等级;评估导致后果的严重性,分为 1-5 五个等级。 A.1.5.2 参照 RB/T 040 附录 B 实验室生物安全风险评估矩阵,对暴露或污染发生的可能性及其导致后果的严重性进行风险等级评估(见表 A.1 风险等级矩阵)。
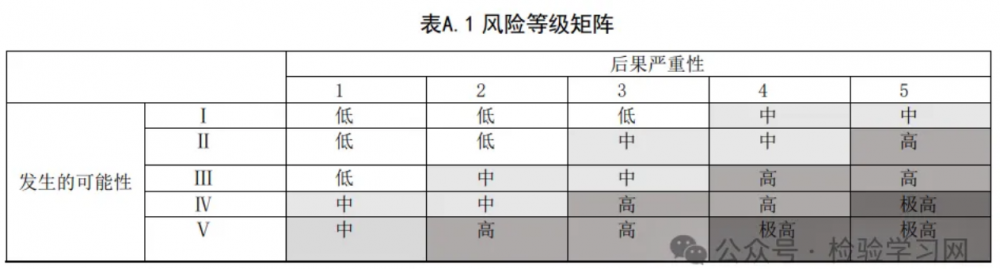
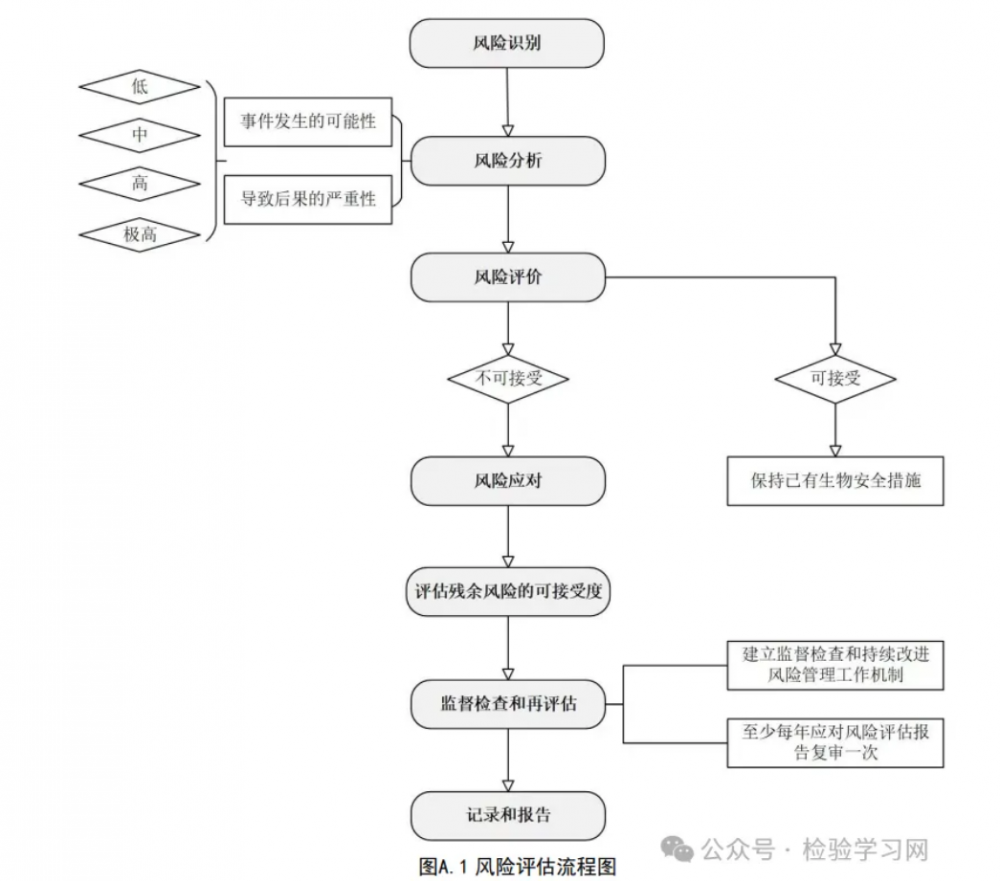
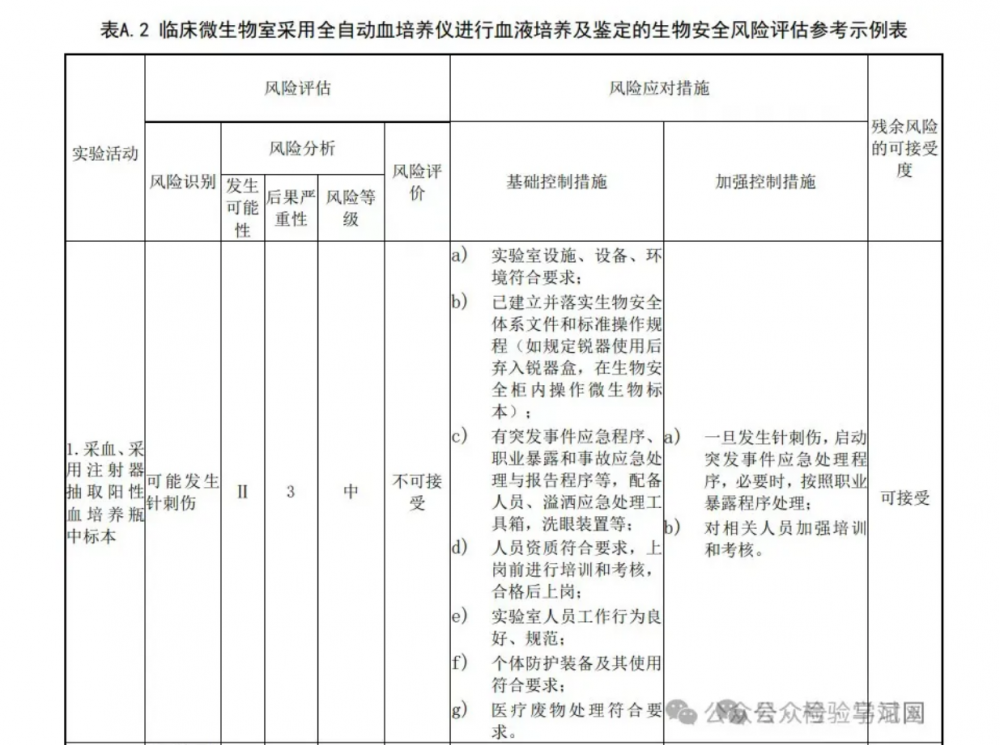
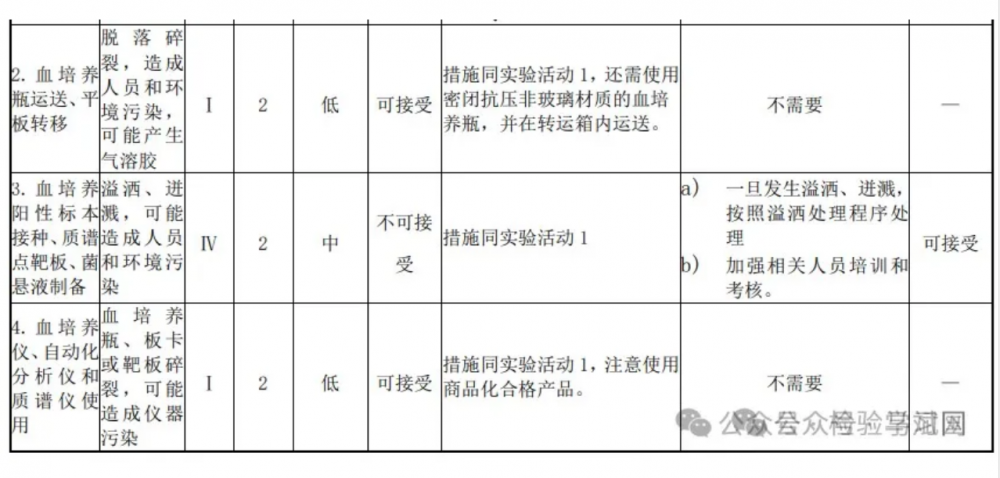
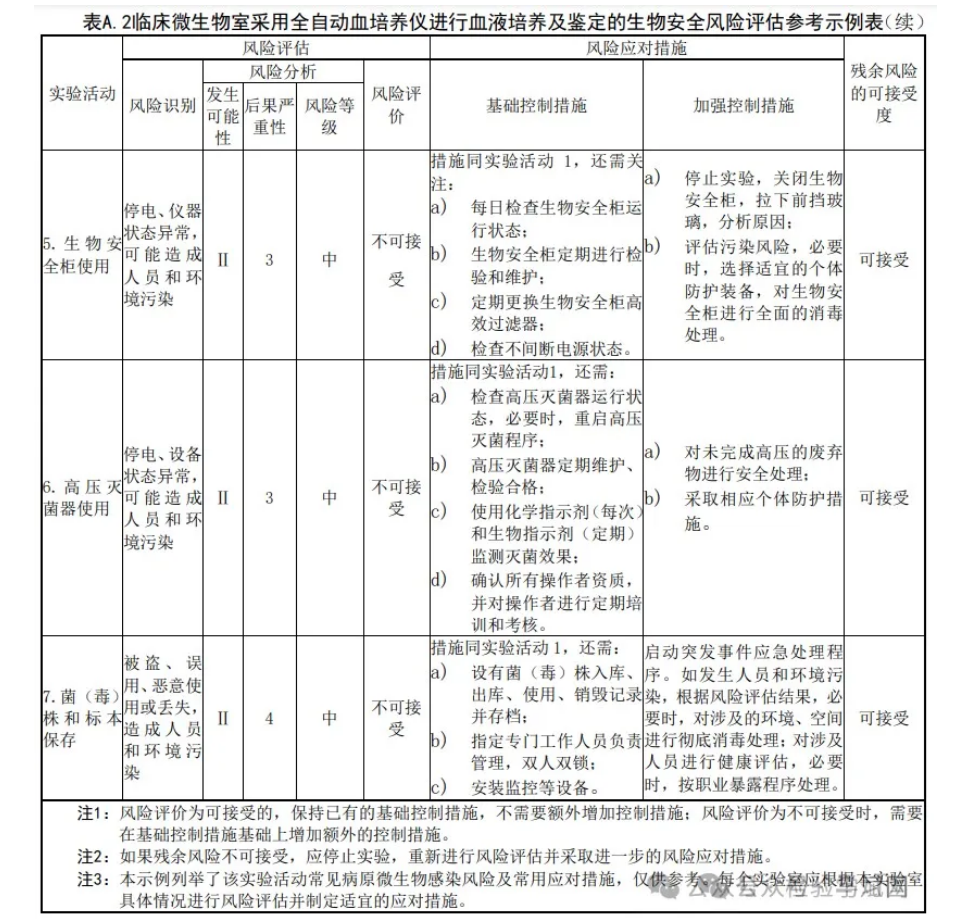
A.1.6 风险评价:对比风险分析结果和风险准则,以确定风险和/或其大小是否可以接受。当风险可接受时,保持已有的生物安全措施;当风险不可接受时,采取风险应对措施。 A.1.7 风险应对 A.1.7.1 针对风险评估所识别出的不可接受的风险,制定风险应对措施,以降低或规避风险,包括制定风险应对计划,实施风险应对措施,评价风险应对计划的有效性,评估残余风险的可接受度。 A.1.7.2 如果残余风险不可接受,应停止实验,重新进行风险评估并制定进一步的风险应对措施。 A.1.8 形成生物安全风险评估报告,报告内容参照本标准第4.5.2条的要求。 A.1.9 依据风险评估报告,修改和完善生物安全管理体系及实验活动相关操作规程,并落实到风险管理的各个环节。对相关人员进行宣贯、培训、考核。定期监督检查,必要时再评估。 A.2 风险评估报告参考示例:临床微生物室采用全自动血培养仪进行血液培养及鉴定的生物安全风险评估 。A.2.1 评估目的:识别采用新进全自动血培养仪进行血液培养及鉴定的生物安全风险,采取相应的应对措施,完善相关安全管理制度,建立相关标准操作规程并落实,确保人员和环境安全。 A.2.2 评估范围:血液培养及鉴定检验全流程的实验活动。A.2.3 评估依据 A.2.3.1 法律法规、指南标准:《中华人民共和国生物安全法》、《病原微生物实验室生物安全管理 条例》、《医疗卫生机构医疗废物管理办法》、《人间传染的病原微生物目录》、《医疗废物分类目录》、 GB 19489、WS 233 等。 A.2.3.2 实验室生物安全管理文件、现有检验项目的标准操作规程等。A.2.4 参与风险评估人员:实验室负责人、专业负责人、岗位工作人员、仪器设备管理人员等。 A.2.5 评估程序和方法:评估程序见图A.1风险评估流程图;风险识别方法参照本标准附录A的A.1.4 风险识别;风险分析方法采用矩阵法(见表A.1风险等级矩阵)确定风险等级;根据风险等级确定可接受度,决定是否采取应对措施,残余风险不可接受时进行再评估。 A.2.6 评估内容 A.2.6.1 涉及的病原微生物:a) 临床血液标本中可能存在的病原微生物,主要为《人间传染的病原微生物目录》中危害程度分类为 第三类和第四类病原微生物,以及第二类病原微生物中的布鲁氏菌、结核分枝杆菌、HIV 等; b) 临床实验室血液培养阳性时的病原微生物,主要为《人间传染的病原微生物目录》中危害程度分类为第三类和第四类的细菌和真菌,以及第二类病原微生物的布鲁氏菌。注:布鲁氏菌的分离纯化、生化鉴定、涂片、显微观察等初步检测活动,可在BSL-2实验室操作。 A.2.6.2 病原微生物特性:包括传染性、传播途径、感染剂量、致病性、在环境中的稳定性和对消毒剂的敏感性、治疗和预防措施;职业暴露及其后果等。注:实验室针对所涉及的病原微生物及其特性应已进行了系统的风险评估,本报告示例受篇幅所限,略去该部分内容。 A.2.6.3 具体评估内容:见表 A.2 血液培养及鉴定的风险评估内容参考示例表。 A.2.7 评估结论:现有基础控制措施及加强控制措施对血液培养及鉴定的生物安全风险可控,可开展该检验项目。注:本示例报告仅涉及病原微生物风险评估,未涉及试剂、设备、设施和环境等相关化学性、物理性等风险因子评估。A.2.8 参与、编写、审核、批准人员:a) 报告编写人员:XXX; b) 报告审核人员:XXX; c) 报告批准人员:XXX; d) 生效日期:()年()月()日。
声明:本微信号注明来源的稿件均为转载,仅用于分享,不代表平台立场,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!
内容来源 | 马斌国
图片来源 | veer、ibaotu
排版 | jinbao
审校 | 金宝



