形态学中突现危急值,这份“凶险”的报告应该怎么发?
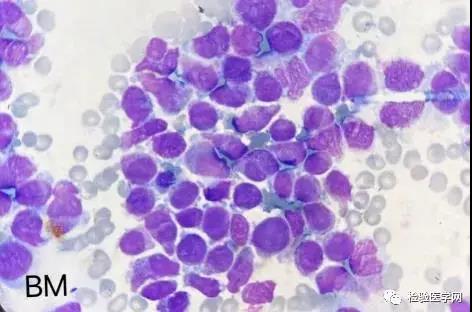
治疗相关性AML(t-AML)是指在原发疾病(包括良性疾病和恶性肿瘤)使用细胞毒性药物治疗和或放射治疗后晚期并发的急性髓系白血病。t-AML多发生于治疗后的10-192个月,分为烷化剂/放疗相关性和拓扑异构酶II抑制剂相关性。
案 例 经 过
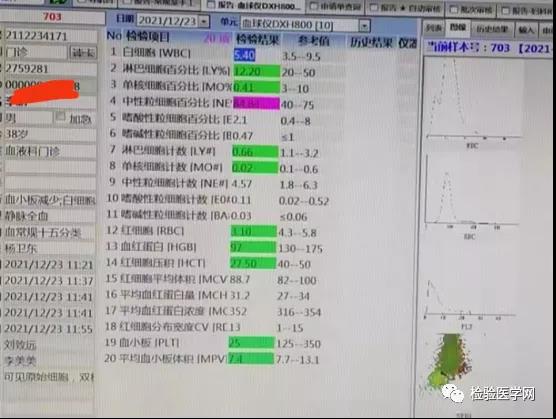
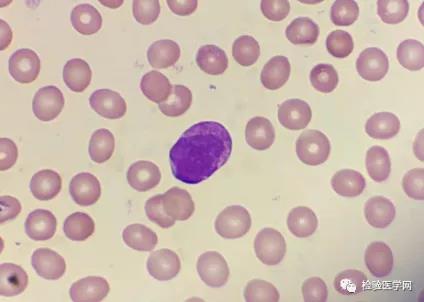
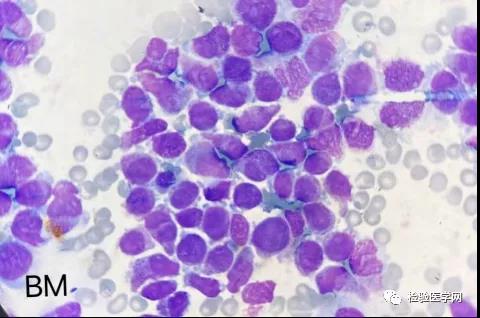
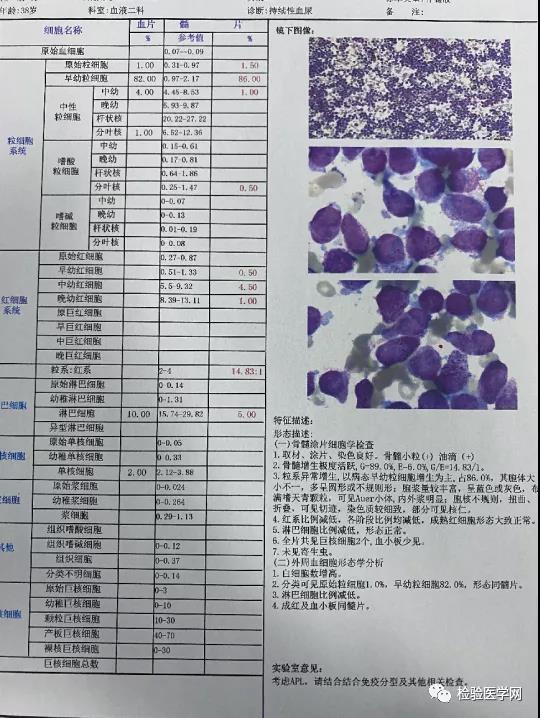

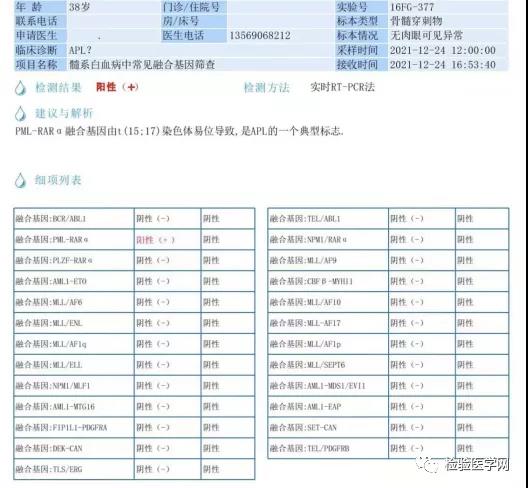
案 例 分 析
1、t(8;21)(q22;q22.1); RUNX1-RUNX1T1
2、inv(16)(p13.1;q22)或t(16;16)(p13;q22); CBFB-MYH11
3、PML-RARA


编辑:骆秉涵
点赞 0 反对 0 收藏 0
评论 0



