DNA甲基化检测在衰老评估和疾病诊断中的价值

李 睿
副研究员。中国科学院大学理学博士,深圳华大生命科学研究院和哈尔滨工业大学联合培养博士后,生物信息副研究员。在基因调控,组学数据研究等方向发表多篇文章,目前主要研究方向为健康衰老评估和多组学数据分析。
一、DNA甲基化介绍
DNA甲基化(DNA methylation)是DNA的一种化学修饰,在哺乳动物中是指在DNA甲基化转移酶的作用下,基因组CpG二核苷酸的胞嘧啶5'碳位共价键结合一个甲基基团(如图1a所示)传学的一部分,会影响基因表达,从而影响表型。甲基化能够引起染色质结构以及DNA构象变化从而导致和蛋白质相互作用发生变化,尤其导致转录启动子区域(transcription promotor)和转录起始复合物(transcription initiation complex)的相互作用发生变化,从而导致基因表达水平的变化(哺乳动物基因附近甲基化的情形如图1b所示)。
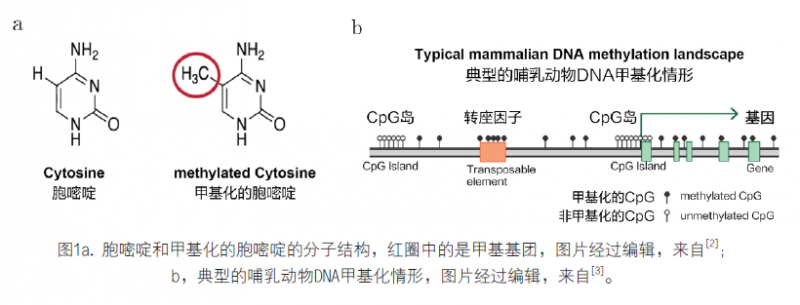
在衰老的过程中,随着年龄的增大,不同位点的甲基化会发生变化,比较普遍的趋势是组织中不同位点甲基化的水平趋向于50%,也就是随机的状态。对于不同器官和细胞类型,可以分别通过一组位点的甲基化水平,比较准确的预测对应的年龄,这个预测的生物学年龄就是器官和组织衰老水平的一种度量。
在很多疾病中,很多位点尤其是基因启动子区域的甲基化水平会发生变化,比如不正常的高甲基化水平会导致基因表达的抑制。DNA甲基化的变化被认为是癌症发展的重要因素。低甲基化会导致基因组的不稳定,超甲基化会导致基因表达的抑制,但是可以作为甲基化编辑的位点。
对不同器官健康的监控,直接采集不同器官和组织的样本不太现实,近年来血液中细胞游离DNA(cell free DNA,cfDNA)检测技术的发展提供了通过血液样本了解器官和组织健康衰老状况的机遇。cfDNA有来自于不同器官和组织,对这部分cfDNA信息的提取就可以了解其来源器官和组织的健康信息,这些信息可以用于器官和组织的衰老评估,也可以用于相关疾病的检测。本文主要介绍通过细胞游离DNA的甲基化来进行衰老评估和衰老相关疾病的研究及检测。
二、DNA甲基化检测技术
DNA甲基化的检测分为整体甲基化水平检测和基因位点特异的甲基化水平检测,这里我们只关注基因位点特异的甲基化水平检测。对于基因位点特异的的甲基化水平检测,目前主要有基于芯片的甲基化检测和基于高通量测序的全基因组甲基化检测,在这里进行简单的介绍。
1. 基于芯片的甲基化检测技术:这种检测只能获得基因组上某些位点的甲基化水平的检测,检测的费用相对于全基因组的甲基化检测的费用较低。这种检测,首先获得DNA片段,然后再杂交到芯片上,进行甲基化水平的检测。目前DNA处理和捕获的策略主要分为三种,第一种是基于用重亚硫酸盐转化,基于甲基化抗体或MBD(Methyl-CpG-Binding Domain)亲和的富集方法,另一种是用限制性内切酶进行酶切[4]。
2. 基于高通量测序的全基因组甲基化检测技术:这种检测通过高通量测序获得全基因组上各位点的甲基化水平,目前这种检测的价格还比较高。目前基于二代测序的检测方法有,WGBS(Whole-Genome Bisulfite Sequencing),RRBS(Reduced representation bisulfite sequencing),前一种是目前全基因组甲基化检测的金标准,后一种检测方法大概能检测到人类基因组中85%的CpG岛[5]。目前还有基于三代测序技术的甲基化检测方法,Oxford Nanopore开发了基于纳米孔的测序技术,单链DNA通过脂膜中蛋白纳米孔的时候,系统记录下离子电流的变化可以得到DNA的序列信息。甲基化和非甲基化的DNA通过纳米孔的时候电流不同,从而测得不同位点DNA的甲基化水平[6]。
受限于甲基化检测的价格还比较高,目前的研究数量还较少,但是甲基化作为表观遗传学的重要部分,有很大的价值,随着未来甲基化检测的价格能够降下来,将会有更多的研究。
三、Cell free DNA的组织和器官溯源
cfDNA的组织和器官溯源,为通过DNA甲基化进行器官和组织的衰老和疾病评估提供了基础。细胞游离DNA是指游离在血液里边的DNA, 来自于身体各处死亡的细胞。近年的研究发现可以通过组织和器官特异的cfDNA信息来追溯cfDNA的组织来源。通过cfDNA的核小体的包被模式[7],器官特异的甲基化位点信息[8],以及通过相邻甲基化位点之间的关联[9],来达到cfDNA的组织和器官的溯源。
cfDNA的DNA片段分布式和DNA在原来的组织中被核小体包被情况是相关的,通过提取cfDNA中的片段信息,Snyder等人[7]通过傅里叶变换对癌症病人的cfDNA进行了组织溯源,虽然和癌症状况的关联度还不错,但是组织溯源的精度还是不够。Moss等人[8]通过建立不同组织和器官的甲基化参考基准(reference panel),通过去卷积的算法实现了比较准确的组织溯源,他们发现健康人血液中cfDNA,55%来源于白细胞,30%来源于红细胞祖细胞,10%来源于血管上皮细胞,以及1%来源于肝细胞。当机体有炎症,损伤,器官移植,癌症发生的时候,研究发现,来源于这些位置的cfDNA会增多[8,10]。由于甲基化和去甲基化酶的作用,相邻CpG sites可以是同时甲基化的。Guo等人[9]找到47,888这种紧密关联的甲基化区域。通过分析组织特异的甲基化区域信息,他们对59个肺癌或结直肠癌患者进行了癌症负荷的量化,以及对cfDNA进行了组织和器官溯源。
CfDNA可以通过甲基化进行比较准确的组织和器官溯源,为从血液样本获取组织和组织的衰老和疾病状况提供了珍贵的定位信息,使得通过检测CfDNA的甲基化比较准确的对身体不同部位的衰老和疾病状况进行检测提供了潜力,近年的研究不断涌现出相关的成果,为临床的应用提供了基础。
四、DNA甲基化用于衰老评估
通过不同类型的衰老标记物,研究者开发了不同类型的生物学年龄,端粒长度[13],血液生化指标,DNA甲基化[14,15],转录组[16],蛋白组[17],小RNA[18],可穿戴设备的数据[19]等指标都可以用来评估生物学年龄。比较不同的生物学年龄,甲基化年龄的一个突出特点就是预测的实际年龄比较准,和实际年龄的关联系数通常都能达到0.95以上[16,18,20]。
表观遗传的改变是衰老的分子机理的重要部分,表观遗传有三个层次,DNA的甲基化,组蛋白修饰和染色质重编程[21]。DNA的甲基化是通过影响基因转录,从而影响基因的表达。一条DNA上的位点,有甲基化和非甲基化两种状态。如果同时测到同一位点的很多条DNA,就会得到位点甲基化的比例,这个比例会随着年龄发生变化。这个随年龄变化的比例就提供了评估年龄的方法。从甲基化位点中,找到一组和年龄相关,而且相对独立的一组位点,通过这组位点预测到年龄就作为甲基化生物学年龄(参考综述文献[14,15])。2011年,Bocklandt等人[22]首先开发出用88个位点的甲基化水平预测的甲基化生物学年龄。
1. 甲基化年龄具有器官的分辨率:不同器官的甲基化不完全相同,这取决于不同的基因表达需求。这样,器官和组织特异的位点就可以用来对器官和组织的衰老分别进行评估。目前大部分的研究都是从全血,或白细胞的DNA甲基化评估的生物学年龄。癌症治疗过程可以得到不同器官的癌组织和健康对照,为不同器官的甲基化年龄提供了样本。Steve Horvath在2013年,开发了适用于多器官和细胞类型的甲基化年龄[20],这种适用性是由于在位点挑选和模型参数训练的时候就对多器官同时进行优化,他最后挑选出来的位点有353个,但是在实践中,尤其是对于相对健康的人,采集各种器官和组织的样本进行甲基化检测在实践中的不具有可行性。Hannum等人[16]用血液的甲基化位点训练出甲基化年龄的模型,在对其它的器官中测试的时候,显示不同器官预测的年龄和实际年龄的拟合线的斜率和截距有不相同,通过特异的调整可以实现不同器官和系统比较准确的生物学年龄预测,这验证了不同器官的甲基化变化是不同的。在动物模型中,研究者也进行了相关的探索,Han等人[23]用老鼠进行了研究,用血液样本中挑选出来的3个甲基化位点用来评估同一只老鼠不同的器官的衰老程度,会得出不同的生物学年龄,也显示出不同器官甲基化的衰老模式的不同。中国北京基因组所的数据库The Methylation Bank(MethBank),收集了不同物种的甲基化检测的数据,利用数据库的数据,他们还开发了在线的甲基化年龄的计算工具[24]。
2. 甲基化年龄在疾病人群中的表现:用不同类型的衰老标记物评估出来的生物学年龄可能反映的是机体衰老的不同方面[25],不同的研究者开发的甲基化年龄所用的位点不完全相同,所用的算法也不尽相同,检验生物学年龄的有效性是检验其在疾病预测,寿命预测,抗衰老干预中的作用。组织和器官的甲基化变化反映的可能是比较长期性的,相对稳定的变化,所评估出来的甲基化年龄在慢性病,或者慢性的衰老症状上有比较明显的信号。目前比较经典的甲基化年龄是Horvath的353位点模型[20],和Hannum的71位点的甲基化年龄[16],以及Levine的513位点的甲基化年龄[18]。Steve Horvath 和Kenneth Raj[15]系统的比较了三种甲基化年龄。并且系统的比较了三种甲基化化年龄,而且总结了甲基化年龄增加的衰老相关症状和疾病。甲基化年龄的加速和大龄人的,癌症(如图2所示),神经系统疾病、唐氏综合症、帕金森、沃纳综合征,生理和认知的健康度、以及长寿老人的状况都有比较好的关联[15]。
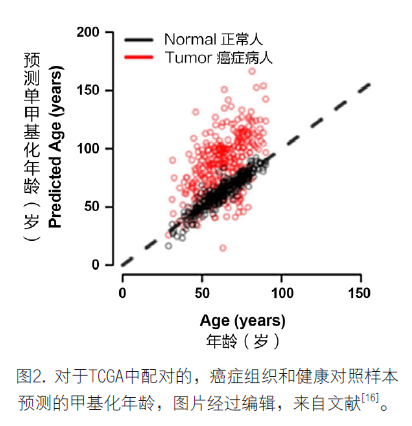
总之,甲基化年龄可以作为一种准确的预测年龄的方法,同时在衰老相关症状和疾病也有比较好的指示作用。
五、DNA甲基化用于衰老相关疾病的应用和研究
在上节中,衰老相关疾病的人群会显示出甲基化生物学年龄加速的现象,这部分我们将讨论,用甲基化位点对疾病进行预测,诊断,以及辅助治疗研究的介绍。
由于cfDNA的甲基化可以进行器官和组织溯源,而且各个器官发生病变的时候会增大释放到血液中的cfDNA的量,同时一些慢性病的甲基化还有特殊的信号。综合这些信息,cfDNA的甲基化在疾病诊断有着重要的作用,目前一些研究成果已经显示出相关的前景。cfDNA上的甲基化水平,cfDNA上的基因的体细胞突变,其在血液中的含量,以及cfDNA片段的分布包含着不同的信息,对于疾病检测具有不同的价值。在这里,我们只介绍通过cfDNA甲基化信号进行检测的研究。目前这方面的研究和应用在癌症中最多,在其他的神经类和代谢类的疾病,以及其它疾病中还相对较少。
1. cfDNA甲基化用于癌症的检测:由于甲基化信号可以进行组织溯源,而且在器官和组织发生病变的时候,来源于该组织的cfDNA就会增多。甲基化对癌症诊断和治疗的应用体现在癌症诊断,以及癌症治疗效果的评估。除了上边介绍过的甲基化生物学年龄对于癌症患者会有加速衰老的信号外,近年的研究也显示了cfDNA的甲基化检测会提供更多的信息。
Moss等人[8]通过建立不同器官和组织的甲基化基准,利用去卷积算法实现了cfDNA的组织溯源,他们发现,通过检测血液中cfDNA的甲基化信息,发现对于转移性的结肠癌(4例),乳腺癌(3例),肺癌(4例),相对于健康人这些病人的血液中,cfDNA的含量会增大很多(大于20倍),尤其是癌症来源器官的比例增大最为明显(图3 a-c)。为了验证这个算法对于癌症组织来源的判断,他们在未知癌症来源的病人进行检测,也发现了和病史相关的信号。这些结果展示这种甲基化去卷积算法对于判断癌症组织来源上的潜力。如图3d所示,他们对肿瘤治疗的敏感性也进行了检测,发现对于治疗敏感的前列腺癌症患者,来自前列腺的cfDNA的比例会有明显的下降;而对治疗抵抗的患者,这个比例并没有表现出明显的下降[8]。Liu等人[26]通过组织特异性的甲基化位点,通过多分类器模型也实现了癌症组织来源的高准确度和高特异性的检测。他们在一个有不同癌症阶段的50种癌症进行了测试,对于癌症的组织特异性达到了99.3%;在提前确定好的12种癌症中,可以实现不同癌症阶段的分类,I-III期的敏感性达到67.3%,癌症越晚期,分类的效果越好。这个研究同样是基于血液的cfDNA甲基化实现了癌症的组织和器官溯源。
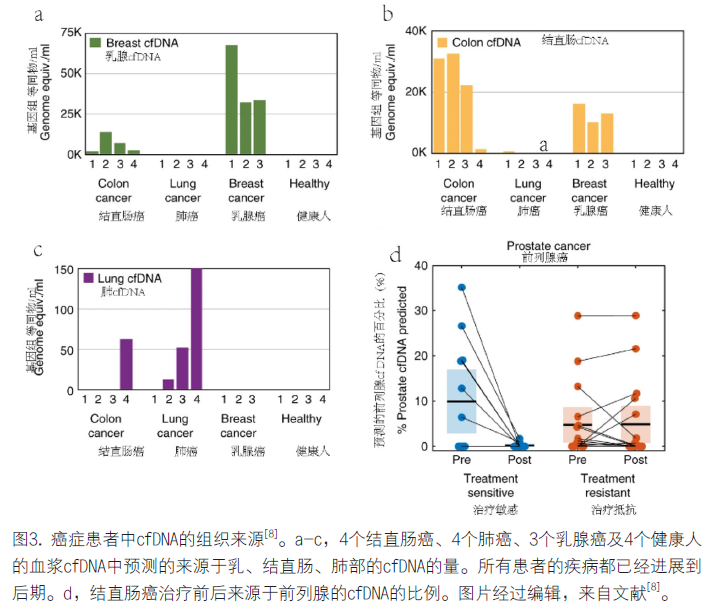
目前,甲基化在癌症诊断,治疗领域的研究还在快速的发展,未来还会有更多更好的研究出现。高灵敏的检测将逐渐针对早期癌症,甚至在影像学还未能检测的阶段,就可以检测到癌症的发生,使患者更早的接受治疗。
2. DNA甲基化用于阿兹海默(Alzheimer disease,AD)的研究:阿兹海默(AD)是一种神经退行性疾病,在确诊前,脑部已经发生了退行性的变化,早诊和诊断的标记物对于治疗有很高的价值。目前已经有一些研究对阿兹海默患者的脑组织的甲基化进行研究。对基因背景相近甚至相同个体出现不同疾病症状,暗示表观遗传在AD发生发展中可能会不同,不同脑区DNA甲基化发生了变化[27],目前的有些结论尚有争议。能在血液中检测到甲基化变化的价值更高。Pai 等人[28]发现AD患者血液中的cfDNA水平会比正常人高,他们还在这些人的血液中发现神经组织特有的甲基化的LHX2甲基化位点。Konki等人[29]报道了在对于在阿兹海默患者上有不同疾病状态的双胞胎的血液中,对cfDNA的甲基化进行了检测。在23对这样的芬兰的双胞胎血液中,他们发现了11个基因为位点的甲基化水平有差异。虽然这些甲基化影响了一些神经功能和疾病相关基因的表达,但是这些变化和阿兹海默患者的进展还未发现关联。其中一个在基因ADARB2上差异的甲基化位点,对于非双胞胎AD患者的前海马体以及内嗅皮层,有相对于健康人不同的甲基化水平,只是这个位点目前尚不足以作为诊断标准。DNA甲基化的组织溯源中,发现脑部受伤后,来自脑部的cfDNA会变多[8],对于AD前期以及AD患者中来源于脑部的cfDNA比例的变化值得去仔细研究。目前血液中DNA的甲基化对于艾兹海默的诊断的研究还不多,还需要更进一步的加强。
3. 甲基化在其它疾病中的研究[30]:目前也有不少关于代谢性疾病中DNA甲基化的研究,虽然有些疾病可以用基因突变来解释,但是gWAS(genome wide association study)研究发现,关联的基因位点只能解释非常少部分(<5-10%)的病例[31]。环境和生活习惯的影响可能通过表观遗传学发生影响。通过检测血液中DNA的甲基化,发现一系列的和代谢性疾病,比如和肥胖相关的位点[32]。一项研究发现,经过高脂饮食的喂养,小鼠脂肪组织的甲基化发生了变化,从而出现类似肥胖和其它糖尿病类似的症状[33]。作为验证,作者也发现在肥胖人群的脂肪组织中也重复发现了这些变化的甲基化位点。值得注意的是,这类甲基化的变化相对比较温和,小于5-10%,这些变化的对生理以及心理的影响还不确定。目前还没发现,这类变化和疾病的发生有确切的关联。虽然从机制上还无法解释甲基化变化对疾病的影响,但是目前来自血液样本中,某些特定基因上的DNA甲基化位点,已经可以作为某些自身免疫疾病的生物标记物,如系统性的红斑狼疮[34,35]。
六、展望
综上所述,DNA甲基化检测,可以提供不同于DNA序列的信息,挖掘DNA甲基化中的信息,尤其是比较方便取得的样本的cfDNA甲基化的信息,为抗衰老实践,以及老年病,尤其是癌症的诊断和治疗提供宝贵的工具。cfDNA甲基化可以进行组织的溯源,为进一步的研究和诊疗技术开发提供了巨大的潜力,未来还会有更多更实用的研究及技术值得期待。
注:本文来源于《临床实验室》2020年第7期“老年医学与检验”专题



