M3白血病一定会有凝血四项异常吗?
前 言
凝血四项包括PT、APTT、TT、Fib,是初诊血小板减少患者、初诊出血与血栓患者的常规检验项目。发现凝血四项异常,尤其是低纤维蛋白原血症,在排除肝病、德巴金等药物的使用史后,是早期快速急性早幼粒细胞白血病识别的重要特征。但表现为全血细胞减少、初诊及治疗过程中均未发生凝血四项异常的急性早幼粒细胞白血病较为罕见,我们遇到一例,现报道如下。
案例经过
患者为51岁男性,以“乏力5天”入院。既往史无特殊。查体:全身皮肤粘膜无黄染、瘀点、瘀斑,胸骨无压痛,肝脾肋下未触及。
查血常规:白细胞1.21 ↓(4-10 ×10^9/L),血红蛋白94 ↓(120-160 g/L) ,血小板计数41 ↓↓(100-300 ×10^9/L)。
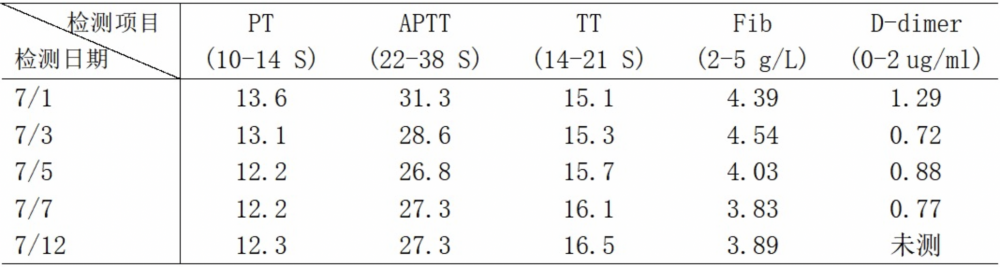
凝血四项及D-dimer结果见表1.
血髓象:急性早幼粒细胞白血病。
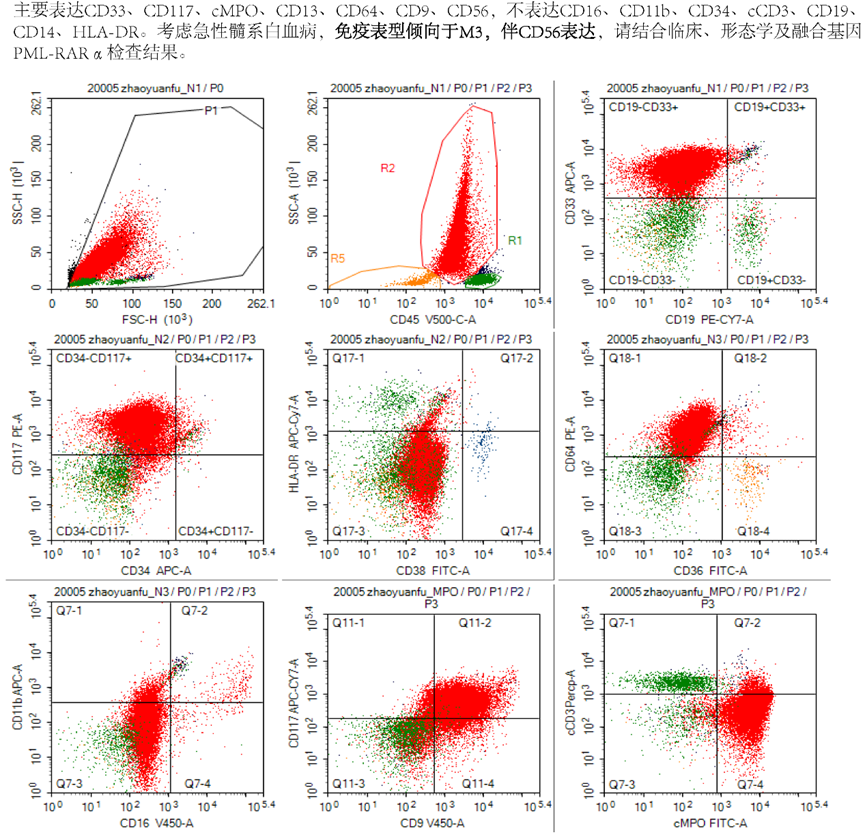
骨髓免疫分型:免疫表型倾向于M3伴CD56表达。
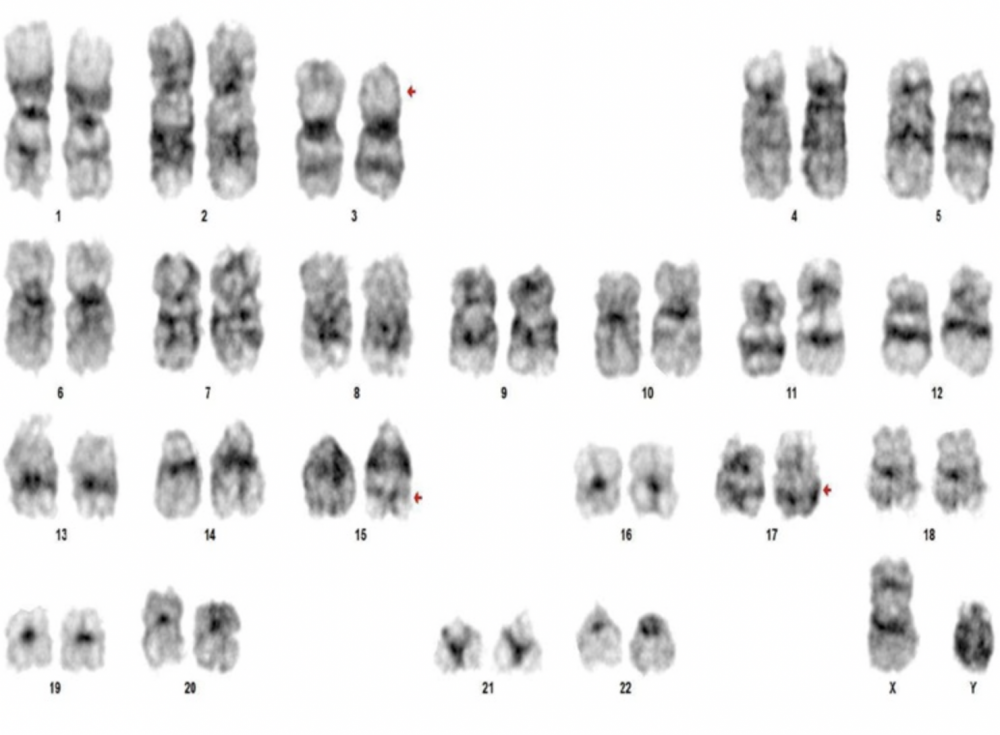
骨髓染色体G显带:46,XY,t(3;17;15)(p21;q21;q22)[15]/46,XY[5]
骨髓融合基因:PML-RARα融合基因短型阳性。
骨髓病理:结合融合基因检查结果符合急性早幼粒细胞白血病M3。

MICM综合诊断:急性早幼粒细胞白血病。
案例分析
维A酸+亚砷酸双诱导治疗的广泛应用,已显著降低了APL患者的死亡率,显著提高了APL患者的长期生存率、治愈率。但早期死亡仍是困扰APL治疗的难题。其中,出血尤其是颅脑出血、肺出血是早期死亡的最主要原因,也是APL最终走向治愈的严重障碍。
促凝、抗凝、促纤溶系统三者的动态平衡最终决定APL患者是发生出血还是血栓。但APL患者往往以凝血因子与血小板的消耗,纤溶活化为主,故最常表现为出血。
一方面[1],APL细胞高表达annexin II ,导致纤溶酶异常活化, 导致低纤维蛋白原血症或纤维蛋白原降低;另一方面[1],APL患者血清中α2-抗纤溶酶降低,也导致低纤维蛋白原血症;最后,弹性蛋白酶活性异常、金属肽酶活化、组织因子途径抑制物(TFPI)水平升高、APL细胞异常分泌的细胞因子与粘附分子也参与了APL患者的止凝血障碍[2]。
本例患者为低白细胞性APL。尽管研究表明高白细胞性APL更易出现致命性出血[3],但工作中遇到的低白细胞性APL罕见无显性出血者,罕有不发生纤维蛋白原水平下降,也是及时疑诊APL的一个重要的常规检验项目。
该患者骨髓免疫表型检查中发现,APL表达CD56,一个预后差的标志,那该患者无显性出血是否与CD56表达有关呢?
2018年ASH年会上的一篇POSTER拒绝了这一猜想。在该篇POSER中,有34例(13%)患者表达CD56,CD56表达患者的出血更为严重[4]。
分子学研究表明[5],基因表达异常参与了癌症患者的止凝血紊乱。该患者染色体为46,XY,t(3;17;15)(p21;q21;q22),涉及三条染色体平衡易位,并非常规的t(15;17)(q22;q21),按ISCN平衡易位描述规则,该患者仍可形成PML-RARAα融合基因,且经融合基因检查证实,且最终经维A酸、亚砷酸双诱导治疗获分子学CR,随访至今已有7月时间,仍处于分子学CR。是否是染色体3p21上的基因表达改变或者新形成的其它融合基因造成了该患者未发生出血?有待于进一步研究。限于患者的接受度,我们未能对该患者进行进一步的转录组测序检查。
该患者是否有更高的血栓风险呢?APL患者毕竟有2-15%的概率发生血栓事件,回顾性及前瞻性研究表明[2],深静脉血栓、肺血栓栓塞、脑卒中、急性心肌梗死、导管相关血栓均有可能在APL患者中发生。限于医院的技术条件,除D-dimer外,我们未能对该患者行新血栓四项、血栓弹力图等检查。幸运的时,从初诊直至获得分子学CR,该患者并未发生血栓事件。
总 结
部分医院以PT衍算法报告Fib浓度,故得出APL患者Fib正常的错误结论。一项包括211名APL患者的回顾性分析[6]发现,初诊时Fib浓度在正常范围者仅有1例。尽管罕见,但初诊及治疗过程中,凝血四项始终无异常,也无出血、血栓表现的急性早幼粒细胞白血病患者,却可能在临床工作中无意间遇到。这提示我们在临床工作中更应该精益求精,及时联想到多种可能性。并及时与检验科沟通,充分利用白细胞散点图等多种手段,以利于疾病的及时、精准诊断。在医院信息化建设如火如荼的今天,医院也应该将血常规检验中的白细胞散点图等图像信息及时传送至临床科室的电脑中,有利于提高检验及临床的工作效率,最终有利于患者的及时诊疗。
参考文献
[1]. Hambley, B. C., Tomuleasa, C. & Ghiaur, G. Coagulopathy in Acute Promyelocytic Leukemia: Can We Go Beyond Supportive Care? Front. Med. 8, (2021).
[2]. Abla, O., Coco, F. L. & Sanz, M. A. Acute Promyelocytic Leukemia: A Clinical Guide. (Springer, 2018).
[3]. de la Serna, J. et al. Causes and prognostic factors of remission induction failure in patients with acute promyelocytic leukemia treated with all-trans retinoic acid and idarubicin. Blood111, 3395–3402 (2008).
[4]. Takeshita, A. et al. CD56 Is an Unfavorable Prognostic Factor for Acute Promyelocytic Leukemia: Results By Multivariate Analyses in the JALSG-APL204 Study. Blood132, 2798 (2018).
[5]. Boccaccio, C. et al. The MET oncogene drives a genetic programme linking cancer to haemostasis. Nature434, 396–400 (2005).
[6]. Lou, Y. et al. Hypofibrinogenemia as a clue in the presumptive diagnosis of acute promyelocytic leukemia.Leuk. Res.50, 11–16 (2016).



