心脏生物标志物利钠肽家族应用范围与临床诊断价值
BNP/NT-proBNP临床应用已有近20年的历史,已是临床相关HF指南中诊断和预后监测方面Ia级推荐项目,已成为HF诊治方面不可或缺的生物标志物。尽管如此,人们对利钠肽家族的研究仍未停止,到目前为止,又从分子结构,实验室检测,相关新药研发等方面及又有了许多新发现。下面就临床应用拓展方面重点加以介绍。
Goetze JP,Bruneau BG,Ramos HR等在Nat Rev Cardiol. 2020年17卷11期发表的文章“Cardiac natriuretic peptides”中的Box1列举了关于BNP/NT-proBNP的应用范围已涉及到是cardiovascular disease,即房颤、肺动脉高压、心力衰竭、心肌纤维化、肥胖/代谢综合征/2型糖尿病和高血压等方面。



一、关于血中NPs
目前血中NPs临床主要用于心血管功能评价。主要有C端ANP或BNP,但由于其半衰期分别只有2-4min和20min会限制其临床应用。而相关裂解产物,如NT-proBNP和MR-proANP由于其半衰期约90min,故可作为血中诊断方面的ANP和BNP代言人。当前,临床指南建议用于诊断急性失代偿心衰的生物标志物是BNP和NT-proBNP,并用于预测预后及监测治疗效果,同时用于急性心源性呼吸困难的排除。现有的检验方法由于方法间使用抗体来源不同、加之缺乏参考标准品及单位不同,故不同检测系统间结果不能比较。另外,对结果解读时,一定要结合性别,年龄,种族,肥胖程度及肾功能。ANP和MR-proANP作为生物标志物的诊断价值尚未得到广泛的研究。但有研究发现,针对HFpEF患者,MR-proANP比NT-proBNP更敏感。高水平MR-proANP与10年全因死亡率及STEMI 5年死亡率相关。基于全基因相关研究发现是ANP而非BNP是血压调节器,未来针对其细胞处理过程,受体亲和力及降解不同研发高敏感性方法检测血浆ANP,MR-proANP,BNP和NT-proBNP是有必要的。由于NPs间不同的分子构型,引起一些临床命名的混乱。ANP(也称为ANP-28)和BNP(也称为BNP-32)应该容易识别。而NT-proANP和NT-proBNP容易引起误解,因为免疫方法检测的是proANP或proBNP的N段区域片段,故proBNP完整形式也可以检测到。在心脏NPs表达高度增加慢性HF患者中,血中存在形式主要是proBNP,这种情况在大多数用N端片段中进行校准的临床应用方法中并没有被考虑规避。因此,出现分析偏倚是常见的,而且这种偏倚受心脏疾病程度的影响。
除了在HF方面的成熟应用,NPs同样可用于AF,ACS,心肌炎,sepsis和心脏移植后排斥反应等方面。此外,血浆NPs水平可能由遗传决定,其涉及NPs血浆异常低浓度和高血压患者的相关疾病指标。除了明显的种族差异,血浆NPs浓度也可能受糖尿病、代谢综合征或肥胖等因素影响。新发现NPs也涉及到肺动脉高压(PAH)的治疗。
二、关于房颤(AF)
AF患者出现中风的重要原因是由于左心耳的形态与功能,心肌细胞内其含有高致密性的分泌颗粒。针对持续性AF患者和非AF患者但具有相同心血管病理学因素(包括缺血性心脏病,高血压性心肌病,特发性扩张性心肌病,瓣膜性疾病或Chagas病)发现AF患者左房更大。另外,有卒中风险AF个体左心耳顺行血流峰值速度较慢(<20cm/s),且有炎症和血栓前症状,CRP,纤维蛋白原和NT-proBNP升高且独立于HF症状表现。因此,炎症环境和血流动力学应力可能是后续AF和左心耳血栓形成的重要基础,这两个因素都会刺激NPs的产生。针对AF患者的大型临床研究中发现,血浆NT-proBNP升高大于75%者,其可以作为预测中风或全身性血栓和心源性死亡标志物。CUTOFF值设为>1250ng/L的预测能力与四分群最低组<370ng/L相比,结合CHA2DS2VASC score其预测能力有很大提高。同样,特发性阵发性AF(未知有心脏病),其NT-proBNP水平可作为阵发性AF潜在预测标志。
三、关于肺动脉高压
尽管目前关于1组PAH的指南和共识都承认一些用于诊断和预后判断的生物标志物,但仅推荐BNP和NT-proBNP。PAH是一种严重进行性疾病,且成活率显著降低。其中最重要的因素是右室功能异常,原因是由于肺血管阻力的增加,随后是右室肥大及扩大,三尖瓣返流,右心压力增加及右房扩大。同时使用侵入性手段检测压力和检测血浆BNP水平表明两者直接相关,即肺动脉平均压升高和血浆BNP浓度升高,当超声心动图测量右房扩大时死亡率显著升高。REVEAL研究显示,如果BNP<50ng/L或NT-proBNP<300ng/L时具有较高存活率。相反,如果BNP>180ng/L或NT-proBNP>1500ng/L,则意味高死亡率。Box1中为目前指南建议CUTOFF值。PAH治疗主要集中在内皮素受体拮抗剂的使用,结合内皮素受体A型、B型或两者,和5型磷酸二酯酶抑制剂,其阻断cGMP的水解与失活。当前,使用内皮素受体拮抗剂包括,安立生坦,波生坦和马昔腾坦,5型磷酸二酯酶抑制剂包括,西地那非,他达拉非和伐地那非。但这些通道被抑制时,在肺血管床ADP介导的信号通道会增加,血浆cGMP水平增加,降低血管收缩及通过抑制转化生长因子-β诱导的成纤维细胞向肌纤维母细胞的转化以防止纤维症进展,使得右心功能改善。在一项涉及到PAH急性期患者的Ⅱa期临床试验中,100mg消旋卡多曲(一种脑啡肽酶抑制剂,最初用于治疗分泌性腹泻),伴有血浆ANP浓度增加79%,cGMP增加106%,及肺血管阻力下降16%。此外,在14天的治疗中,每天两次给予100mg消旋卡多曲,ANP浓度增加14%,没有副作用或低血压发生。其他研究也显示出消旋卡多曲治疗PAH的类似效果,且不管是否有伴有肺纤维化。
四、关于心力衰竭
建议针对怀疑急性HF患者检测BNP或NT-proBNP以排除其他原因引起的呼吸困难和评估慢性HF患者预后。新HF治疗药是血管紧张素受体-脑啡肽酶抑制剂的复合物,即血管紧张素受体阻滞剂(缬沙坦)和脑啡肽酶抑制剂(沙库巴曲)。该药主要针对HFrEF治疗有效。在PARADIGM-HF研究中发现,沙库巴曲-缬沙坦降低心血管病死亡率20%,21%的HF住院率,对于任何病因的心衰(缺血性或非缺血性心脏病),与依那普利标准治疗相比具有明显优势。这一获益原因归于脑啡肽酶抑制而引起的血浆BNP适度的增加,加之血管紧张素受体阻滞剂的作用改变了心血管性能。然而,考虑到BNP检测有几种方法,故其获益是否是由于脑啡肽酶抑制BNP裂解而引起的获益并不确定,因为,有三个裂解位点,而不同的检测试剂使用不同的捕获抗体且针对不同的抗原表位。正因为如此,有些研究发现血浆BNP水平升高,而有些显示降低或无变化。这些发现与脑啡肽酶具有的ANP和CNP亲和力高于BNP相一致,这意味着脑啡肽酶抑制对血浆ANP水平的影响超过BNP。新研究也证明沙库巴曲对ANP提升效果优于BNP。一组HFrEF患者服用sacubitril-valsartan不同剂量50mg,100mg或200mg每天2次连续监测显示ANP随服药剂量增加而浓度相应增加。而BNP初始阶段显示适度升高。随后则缓慢降低,但不同的检测试剂具有不同的性能表现,降低同样见于NT-proBNP,proBNP和MR-proANP这些非脑啡肽酶底物的物质。与这一研究相一致的PARADIGM-HF研究显示血浆BNP浓度在30天内是增加的,但依那普利对照组未见升高;8个月后血浆BNP浓度趋向下降,但对照组未见变化。平均NT-proBNP浓度在30天和8个月sacubitril-valsartan治疗组都有下降。需引起关注的是,不考虑治疗手段(依那普利或sacubitril-valsartan),30天如果NT-proBNP<1000ng/L,则患者会更少发生心血管疾病终点事件(心血管死亡和HF入院),尽管整个研究只有27个月,sacubitril-valsartan事件发生率是依那普利的近一半(17%比31%)。对于sacubitril-valsartan治疗引起的ANP与BNP间表现的明显差异的解释仍不明了。尽管相对增加,HF患者BNP会高于ANP,但血浆绝对值水平ANP会高于BNP。举例,一组终末期HF患者,血浆ANP为356±21ng/l(n=77),血浆BNP为259±57ng/l(n=76)。两者都是脑啡肽酶底物,但ANP血浆浓度高于BNP,由于脑啡肽酶的抑制会导致两者升高,但血浆ANP浓度的绝对值与相对值仍高于BNP。另外,HF患者也涉及到血浆促炎细胞因子,如IL-1β,IL-6和肿瘤坏死因子,这些都会引起BNP升高,而非ANP。由于sacubitril-valsartan治疗引起血流动力学和体液状态改变,血浆ANP水平会维持较高水平且高于BNP。同样,血浆BNP水平会降低,这是由于非sacubitril-valsartan治疗相关机制,受炎症因素影响所致,而ANP则不受体液炎症因素影响。同样,非脑啡肽酶底物的生物标志物不会受sacubitril-valsartan的影响,但血流动力学状态改善时,其血浆水平会下降。除了作用于NPs外,脑啡肽酶还影响几种重要的血管扩张底物,包括缓激肽、P物资和肾上腺髓质素,以及血管收缩肽。如血管紧张素Ⅰ和血管紧张素Ⅱ及内皮素。特别是sacubitril抑制脑啡肽酶介导的缓激肽降解可以增加血管通透性,引起不良反应,如血管水肿(使用奥马曲拉omapatrilat也观察到此现象,该药抑制可使缓激肽分解的氨肽酶P)。另一副作用是低血压,是由于P物质的部分效应所致,因为P物质具有强效的一氧化氮介导的血管舒张效应。在PARADIGM试验中发现低血压占14%,而依那普利治疗组只占9.2%(p<0.01)。另外,在老鼠脑中发现脑啡肽酶可以降解淀粉样蛋白β,因此需防止其沉积进而发展为阿尔茨海默病。因此,有人担心sacubitril-valsartan治疗由于抑制了脑啡肽酶会导致淀粉样蛋白β的脑中累积,但在人类未见这种副作用的发生,且与依那普利治疗组相比其认知能力未见显著差异。患者认知恶化更加重心血管系统病变,如AF,CAD,stroke,增加血浆中NT-proBNP水平,损伤肾功能及增加失代偿HF入院率,故这些因素也与大脑功能退化相关。
五、关于心脏重构逆转
沙库巴曲-缬沙坦治疗可以解释HFrEF患者心脏重构的逆转。有两项研究支持这一结论。PROVE研究评估了HFrEF患者接受沙库巴曲-缬沙治疗组NT-proBNP水平与12个月内心脏重构情况发现NT-proBNP只是适当降低就伴有左室射血分数的增加及左室舒张终末容积指数(LVEDVI),左室收缩终末容积指数(LVESVI),左房容积指数(LAVI)及早期舒张灌注压环型速率(E/e)降低,这些参数变化都意味着心脏容积与功能的改善。EVALUATE研究显示,针对HFrEF患者12个月沙库巴曲-缬沙治疗与依那普利比较主动脉特征性阻抗未见显著降低。然而,沙库巴曲-缬沙治疗组所有心脏重构指数,如LVEDVI,LVESVI,LAVI和E/e全部显著降低。进一步讲,血浆NT-proBNP浓度沙库巴曲-缬沙治疗组显著低于依那普利治疗组,且尿cGMP、肌酐指数增加。另外,血浆NT-proBNP水平与心脏容积降低显著相关。这些研究提示沙库巴曲-缬沙坦针对HFrEF治疗有利于心脏重构的恢复及促进内源性心脏NP激活。
六、关于心肌纤维化
心肌纤维化是进行性HF另一个重要机制。心肌纤维化组织学定义是过度的纤维组织(胶原纤维Ⅰ型和Ⅲ型)心脏内弥散性沉积。在心肌病变过程中,促纤维化与抗纤维化间平衡会受到血流动力学,体液及代谢因素影响。醛固酮,ST2蛋白,galectin3和TIMPI会促进胶原合成。在胶原处理过程中,N端和C端区域被清除掉。最终,胶原被MMP2和MMP9处理和/或降解。这些所有蛋白质,包括检测血中N端Ⅰ型前胶原前肽(PINP)和N端Ⅲ型前胶原前肽(PⅢNP)可以用于发现心肌纤维变性的激活。人类PARADIGM-HF试验发现>65%的HFrEF患者心肌纤维化标志物升高。血浆ST2,TIMPI和PⅢNP高于基础水平者直接与心源性死亡及再入院率增加相关。经过8个月沙库巴曲-缬沙坦治疗与依那普利治疗组相比,血浆醛固酮,ST2,TIMP1,PIMP和MMP9有显著降低。该研究中有稍多于50%患者接受盐皮质激素拮抗剂,要么是螺内酯或依普利酮的治疗,这两者治疗手段同样会降低PⅢNP水平及死亡和再入院率。针对ANP的结构基础,其作为脑啡肽酶主要靶标是由于其结构性高亲和力,沙库巴曲会增加血浆ANP浓度会起到阻止心肌纤维化并防止心肌重构的作用。同时沙库巴曲-缬沙坦也会降低由于抑制醛固酮和纤维化引起的心源性猝死。最后,在MEAS研究中,1334位个体进行了血浆NT-proBNP水平检测和心脏核磁共振T1定量判断心肌纤维化。磁共振图像显示血浆NT-proBNP水平与亚临床弥漫性纤维化呈正相关,这显示NT-proBNP与心脏纤维化密切相关。
七、关于肥胖和代谢综合征及糖尿病
肥胖,代谢综合征或2型糖尿病个体血浆NPs会随着肥胖程度而进行性降低。这涉及到机制之一是脂肪组织中和单核细胞内NPR-C丰富。与正常体重指数者相比,高胰岛素血症NPR-C表达增加将会增加NPs在血中的清除。因此,人体脂肪组织中NPR-A和NPR-B表达水平高会引起脂肪组织内NPs激活。因此,肥胖个体,脑啡肽酶表达水平高,会引起NP快速降解。人体试验发现高胰岛素血症,而非体重指数是与血浆NP水平和胰岛素抵抗逆相关关键因素,这种逆相关同样可在评价体重指数个体稍微偏胖的个体内观察到。NP激素原N端衍生片段不是脑啡肽酶底物区域,但任然在肥胖个体(如BMI<30kg/m2)血中低浓度存在。ProBNP可能存在有9个糖基化位点,包括71苏氨酸残基,该位点最接近裂解点,其对ProBNP翻译后裂解非常重要。NT-proBNP可用商业试剂使用抗体直接针对proBNP中央区域,该区域涉及到80%以上的糖基化区域。从化学计量学角度看,Thr71糖基化并不是一个完整的事件,它阻碍了产生BNP的NT-proBNP的裂解发生,因此,这种情况下相关肽浓度会低于预期。三种检测血浆糖基化和非糖基化(总)proBNP,另一种试剂检测的是血浆proBNP水平,其Thr71非糖基化,第三种试剂检测的是中央去非糖基化血浆proBNP显示出HF患者高水平proBNP与对照组比,与BMI无关,但血浆NT-proBNP水平BMI>30kg/m2显著低于BMI≤30kg/m2者。肥胖HF患者,Thr71糖基化高于非肥胖HF患者,这可以解释为什么血浆肽片段,如NT-proBNP非脑啡肽降解作用底物,肥胖个体其水平会低。因此,目前指南定义诊断HF的CUTOFF值针对肥胖患者要下降50%。针对肥胖HF患者检测血浆proBNP比NT-proBNP或BNP更加准确。白色脂肪含甘油三酯是能量储备的来源,而棕色脂肪具有产热和消瘦作用。在人脂肪组织中NPs激活降脂作用。肥胖个体,代谢综合征或2型糖尿病,棕色脂肪组织质量和活化会通过多种机制显著降低血浆NT-proBNP水平。然而,一些生理学或药理学刺激会诱导血浆NPs增加并激活“棕色”脂肪组织并有制热现象,这方面仍需进一步研究。与上述发现相一致。PARADIGM研究实验发现HFrEF患者和糖尿病患者接受沙库巴曲-缬沙坦治疗者血糖控制有显著改善(检测HbA1c),可能不太需要胰岛素治疗,且在三年随访中发现血浆HDL-C水平升高,与依那普利治疗组相比。这些获益在BMI增加组更加明显。此外,我们推测由于脑啡肽酶抑制使血浆ANP和BNP增加降低了胰岛素抵抗,其结果是机体能更好地进行处置碳水化合物和脂质代谢。同样由于营养状态的改变减轻了伴随的促炎状态。在PARADIGM-HF生物标志物亚组研究中发现,伴发糖尿病者NT-proBNP水平基础水平会低于非糖尿病患者。尽管没有显著性差异,但糖尿病个体血浆cTnT会显著高于非糖尿病个体,这提示其存在慢性心肌损伤。结合血浆cTnT>18ng/l和NT-proBNP四分群最高值(>1342ng/l)具有最强的全因死亡预测价值。最后,严重肥胖个体(BMI>40kg/m2)具有低水平NPs;减肥手术后,体重减轻和糖尿病,血压控制后血浆水平将恢复。
八、关于高血压
NPs水平改变与高血压及其并发症发生密切相关。有大比例的高血压个体出现血浆ANP,BNP及完整proBNP低水平。高血压初始阶段(高血压前期和1阶段高血压),血浆NT-proANP,NT-proBNP和BNP水平高血压个体会显著低于血压正常者,而完整proBNP会略低,而ANP水平没变化。相反,2阶段高血压,血浆BNP和NT-proBNP水平会高于血压正常个体。合理解释是,在高血压初始阶段,由基因决定低水平NPs可以防止尿钠增多,利尿及血管扩张,而随着高血压病情严重程度的发展,完整proBNP分泌增多以试图维持心血管内稳态及防止或代偿发展为左室肥大及纤维化。
九、关于NPs用于临床治疗方面
由于NPs良好的药效学方面的作用,其针对心血管疾病治疗的主要策略有三:使用天然NPs,使用改良的NPs以增加其生物半衰期,单独或联合使用的治疗药物降低内源性NPs的分解代谢率。NPs自身作为治疗药物,但它们是小分子肽,会被组织蛋白酶迅速降解,且需要在医院持续静脉注射。尽管如此,1995年日本批准了carperitide,一种重组ANP用于治疗急性HF或急性失代偿HF。Nesiritide一重组BNP,2001年FDA批准用于治疗急性HF。ASCEND-HF试验显示患者接受静脉内注射后出现低血压,因此该药并未能常规用于治疗急性HF。其皮下注射可以用于严重不受控制高血压治疗。设计修饰NP以增加其半衰期的例子是共价结合一短两性分子低聚体。动物实验显示其能增加血浆cGMP水平并显著降低血压大约60min。其他延长半衰期的策略包括NPs融合入白蛋白,免疫球蛋白或聚乙烯乙二醇。ANP-HSA组合鼠静脉注射可使血浆cGMP水平升高并降低血压80min,天然ANP降低血压大约只有5min。使用药物减少内源性NPs分解的策略已用于临床,如通过沙库巴曲抑制脑啡肽酶并联合应用缬沙坦已成功用于治疗动脉性高血压,慢性充血性心力衰竭及心肌纤维化。
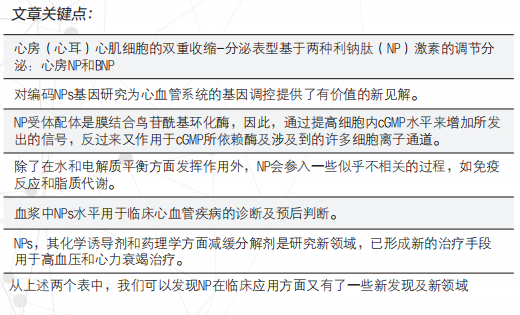
结论:通过研究看似形态怪异的心房心肌细胞发现心脏其具有的内分泌功能,特征是调节和分泌的多肽激素,ANP和BNP。这些激素的标志性效应是维持钠及电解质平衡和细胞外液量调节显著作用,并引起人们用于临床治疗方面的极大关注,如高血压和慢性充血性心力衰竭。当然,目前关于有更多的文献提出其检测标准化的重要性,以利于不同研究的直接比较。
在分子水平方面对NPPA和NPPB表达的调控获得独特的了解,这反过来验证了其在心血管基因调控方面的核心价值。G-蛋白-配对信号,细胞因子受体-介导信号和机械牵拉-介导信号控制NPs的分泌,因此,NPs细胞释放是多种刺激的整合。NPs是两种具有鸟苷酰基环化酶激活的细胞膜受体配体,其存在于多种细胞中。因此,NPs的作用是通过靶细胞内cGMP的浓度增加来介导调节。对NPs在体液和电解质平衡中的作用初步研究后,发现其参入其他重要且通常出乎意料的过程,如炎症、脂质代谢和癌症。最后,由于NPs良好的药理效应导致其天然肽被用作治疗HF和高血压的药物,并发展嵌合肽和融合蛋白来增加天然NPs的半衰期。组合制药的例子是沙库巴曲(血管紧张素Ⅱ受体拮抗剂)加缬沙坦(脑啡肽酶介导的NPs分解代谢抑制剂)已经证明能有效治疗HFrEF。针对NPs的持续报道说明针对其生理和病理生理过程广泛研究值得深入下去。
参考文献
1. Goetze JP, Bruneau BG, Ramos Hret, al. Cardiac natriuretic peptides. Nat Rev Cardiol IF: (20.26) 2020, (17) 11: 698-717.





