全球疫情下新型冠状病毒抗原检测的临床应用
作者:何书宇 康可人
【摘要】新型冠状病毒肺炎疫情仍在全球肆虐,对于具有传染性的感染者及时检出,是有效实现疫情防控的关键。抗原快速检测作为一种快速、便捷的新冠病毒检测手段,已经成为世界卫生组织(WHO)在内的多个国家和组织的主要手段之一,应用于对早期感染者的检出。并且随着抗原研究深入和国内相关试剂上市,抗原快速检测有望在国内疫情防控中成为核酸检测的重要互补手段。
新型冠状病毒肺炎(COVID-19)大流行是全球性公共卫生问题,对于大众健康、社会、经济产生了巨大的影响。而得益于有力的防疫措施,我国的疫情防控取得显著成效。但具有更强传染性的病毒变异体在全球范围不断出现,COVID-19疫苗的普及应用尚待时日,国内仍可能会面临疫情散发或局部聚集发生的风险。核酸检测作为COVID-19的检测金标准,在疫情防控中发挥了重要价值。但因其检测时间较长、对于检测人员和检测条件要求较高等特点,对于核酸检测能力薄弱或检测周转时间要求高的情况,仍存在一定短板,例如农村/乡镇基层医疗、急诊入院等。抗原快速检测作为一种检测快速、操作便捷的新冠病毒检测方法,在欧美、亚洲、非洲等多地区获得广泛应用,与核酸检测共同成为COVID-19疫情防控的重要检测手段。
一、新型冠状病毒与抗原快速检测
1. 新冠病毒抗原快速检测:抗原快速检测是指应用新型冠状病毒特异性抗体直接检测样本中的病原体,其结果可作为早期确认该病原体感染与否的直接证据,且具有操作简便、报告时间短等优势[1]。对于新型冠状病毒,抗原快速检测所检测的抗原主要是N蛋白和S蛋白,其中N蛋白在β属冠状病毒之间相对保守、合成数量多,具有很强的抗原性,其抗原决定簇是特异性抗体结合的主要位点,同时也是目前上市抗原快速检测试剂选择最多的靶点。
它与核酸检测类似,抗原检测的样本类型一般为感染部位的样本,如鼻咽拭子、口咽拭子等。而相较于核酸检测4-6小时的报告时间,抗原快速检测无需专门检测设备,15分钟即可快速报告结果。值得关注的是,基于唾液等采样更为便捷、安全的样本类型也逐步开展验证和应用,有望进一步提高抗原快速检测的便捷性和安全性,在机场入境点等非医疗机构内快速人员排查尤其具有价值[2, 3]。
2. 对于抗原快速检测的性能评估:截止2021年1月26日,共有13款新冠病毒抗原检测试剂获得美国食品药品监督管理局(FDA)的紧急使用权(EUA),另外有3款抗原检测试剂进入世界卫生组织(WHO)紧急使用清单(EUL)。在国内也有3款抗原快速检测试剂获得中国国家药品监督管理局(NMPA)批准上市应用。同时,对于抗原快速检测的应用性能评估也在各国逐步开展。
(1)抗原快速检测灵敏度差异较大,但特异性均优异:对于检测性能,WHO以灵敏度≥80%和特异性≥97%作为抗原快速检测的最低性能要求[6]。此前欧洲疾病预防与控制中心(ECDC)对于9种抗原快速检测试剂研究分析显示,与RT-PCR方法对比,灵敏度为29%-93.9%,特异性为80.2%-100%[4],与其他系统分析研究相似[5]。不同临床验证中抗原快速检测灵敏度差异较大,特异性普遍高,检测结果受到样本质量、感染部位及病毒表达量等因素影响较大。抗原检测灵敏度往往与病毒载量正相关,在高病毒载量(Ct≤25或>106个基因组病毒拷贝数/毫升)的患者中,抗原快速检测最可能表现良好,这些患者通常处于症状前(症状出现前1-3天)和疾病的早期症状阶段(疾病的前5-7天内)[6]。同时,值得注意的是,作为WHO实验室加强和诊断技术评估合作中心的FIND的评估研究中,万孚生物等国内厂商的试剂性能优异,与雅培等国际厂商产品性能相当。
(2)抗原快速检测可满足疫情防控核心需求:高传染性个体检出和高频次检测:虽然对于低病毒载量的患者,抗原快速检测的灵敏度可能低于核酸检测,但病毒复制常呈指数级增长,早期病毒由103cp/ml增长至105cp/ml时间短暂,如SARS、流感病毒约为1天,核酸检测高灵敏度对于患者检出率提升有限,而传染性与高病毒载量相关(Ct<25-30),恢复期患者低载量病毒检出,传染性相对较低,对于疫情传播防控影响较小[6,7]。对于具有传染性的病毒分离阳性样本,抗原检测与核酸检测灵敏度相当,并且相较于核酸检测,抗原检测与病毒培养一致性更高[8]。同时,相较于灵敏度,检测频率、周转时间短等对于疫情防控更具价值[9],抗原快速检测可通过促进检测人群增加、检测频率增加、报告时间缩短,提高对于感染者的检出能力,而在疫情防控中发挥关键价值。
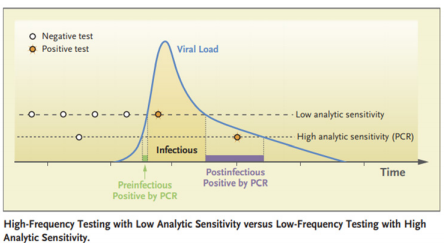
图1. 较高灵敏度/低频次检测与较低灵敏度/高频次检测的差异[7]
二、世卫组织和各国对于抗原快速检测的应用规范与建议
随着试剂获批上市应用,抗原快速检测成为世界范围疫情防控的重要手段之一。2020年9月11日WHO发布《使用快速免疫测定法检测抗原以诊断SARS-CoV-2感染》的指导文件,11月19日,欧洲疾病预防与控制中心(ECDC)推出在欧盟/欧洲经济区和英国对于抗原快速检测的使用建议。同时,美国、加拿大、南非、日本、马来西亚、巴基斯坦、尼泊尔等国家相继也推出针对性规范与建议,以指导抗原快速检测的应用[11-17]。而抗原快速检测在疫情防控中已发挥了重要价值,例如斯洛伐克曾采用抗原快检进行公共卫生筛查,在两周时间内筛查80%人群,发现5万例病例,结合针对性防控手段,在两周内将发病率减低82%[10]。
表1. 各国抗原快速检测应用建议与规范
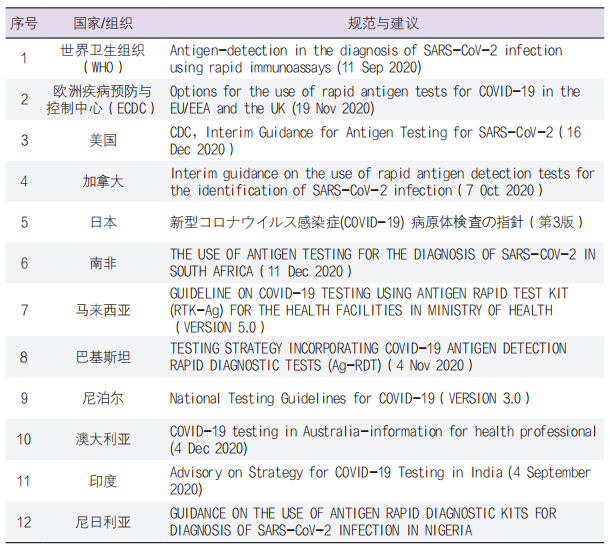
抗原快速被认为可通过早期发现病例、追踪接触者、全人群检测实现传播控制和特定环境下疫情爆发识别,并通过入院时分诊、早期发现和隔离,促进入院患者的临床管理,减轻COVID-19在医疗和社会保健环境中的影响。对于检测的应用,一般基于检测性能、检测结果及时性、对于检测条件和人员适用性以及检测人群流行情况综合评估。
根据各国规范和建议,对于抗原快速检测的应用主要在核酸检测可及性不足或对于检测结果周转时间要求较高的场景。
1. 疑似患者:鉴于抗原快速检测在发病早期灵敏度较好,普遍建议于发病5-7天内检测,部分地区有所放宽,如日本厚生劳动省建议可于发病9日内检测[4,6,11,13]。根据检测人群的预期患病率,对于抗原快速检测应用和结果解读有不同的建议。
(1)在高流行情况下,抗原快速检测可应用于疑似患者的快速排查,尤其是核酸检测能力不足、已有核酸确诊病例的封闭环境(如监狱、学校、疗养院、游轮、工作场所等)等场景,促进及时发现患者,以指导及时隔离与治疗。在这种情况下,抗原快速检测成为医务人员对于入院患者快速排查和分流的重要手段,可提升患者管理效率。抗原检测阳性结果可提示感染者,阴性结果需进一步核酸检测确认,在缺乏核酸检测能力情况下,ECDC等建议可在2-4天后进行再次抗原快速检测[4]。同时,WHO等强调了对于患者平行进行流感等常见呼吸道病原体检测的必要性,以在流感季节叠加情况下,更好对于患者鉴别[6,11]。
(2)在低流行情况下,虽然鉴于阳性率较低,大多数情况下核酸检测仍是推荐首选,但抗原快速检测可凭借较低检测成本和较快检测周转时间,用于排查高传染性的患者,并可促进核酸检测资源聚焦于必要场景下应用。同时,对于核酸检测能力不足的偏远基层地区或封闭环境下的疑似患者,也可考虑应用抗原快速检测。在此情况下,抗原快速检测有助于识别高传染性病例,并迅速发现新的疫情,同时对于抗原检测阳性患者进行核酸检测确诊。
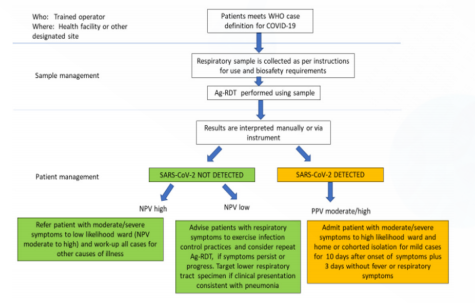
图2. WHO对于广泛传播且核酸检测能力不足地区的抗原应用建议[6]
2. 高危人群(如无症状密切接触者):虽然抗原快速检测尚未授权用于无症状病例接触者检测,但考虑到无症状病例已被证明具有与有症状病例相似的病毒载量,抗原快速检测也被推荐进行应用[4,6,18]。
(1)对于已知确诊病例的密切接触者,应尽快进行抗原快速检测,在明确暴露时间的情况下,尽量在暴露7天内检测,以及时检出高传染性感染者,对于抗原阴性病例需核酸检测确认。
(2)对于封闭环境下(如长期护理机构),抗原快速检测可用于筛查低风险接触者,抗原检测阴性需核酸检测确认。当核酸检测能力不足时,可于2-4天后进行抗原检测确认[4]。
(3)在高流行情况下(如广泛社区传播),抗原快速检测可用于人群广泛筛查与定期监测,以排查高传染性病例,并减低医疗机构压力。
(4)对于医疗保健、家庭护理、长期护理设施、封闭环境(例如监狱、移民拘留和接待中心)的工作人员,由于其感染风险增加,可能扮演超级传播者的角色,建议采用抗原快速检测进行筛查和连续检测(如每2-3天)。
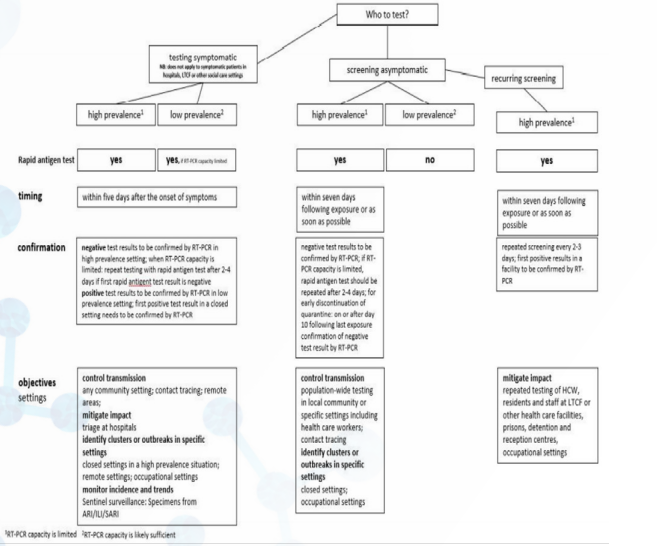
图3. ECDC对于抗原快速检测的应用建议[4]
3. 入境点筛查:对于如空港等入境点的过境旅客,因预期感染率较低,一般推荐进行核酸检测。但核酸检测成本较高且检测周转时间较长。对于此种情况,在有来自高质量研究数据证实抗原快速检测试剂的特异性>99%情况,WHO有条件推荐抗原快速检测[6]。而鉴于输入性病例的严峻形式,南非、日本等部分地区已开展入境点的抗原快速检测应用[11,12]。如南非,建议对于未进行核酸检测抵达的无症状旅客进行抗原快速检测筛查,另外,对于豁免清单上的旅行者(如卡车司机、往返学生)进行抗原检测监测(如每周一次),抗原检测阳性者建议核酸确认[12]。
4. 工作场所、学校等场所的常规筛查:对进入学校和工作场所等人员进行检查可能是很多国家重新开放经济的关键战略。考虑到抗原检测快速、便捷的特点,而使用核酸检测成本较高且周转时间较长,通过成本更低、可及性更高的解决方案(如基于抗原快速检测)被认为是合理的[12]。在有来自高质量研究数据证实抗原快速检测试剂的特异性>99%情况,WHO有条件推荐抗原快速检测[6]。与此相似,对于急诊入院/手术病例,抗原快速检测可促进对于潜在高传染性病例快速检出,及时为处置提供指导。
三、对于国内抗原快速检测应用的建议
虽然国内疫情防控卓有成效,并且在城市地区核酸检测能力较为充足,但在全球疫情仍在蔓延的情况下,对于疫情防控仍不能松懈。国内各地区医疗检测能力存在一定差异,并且在疫情逐步呈现常态化趋势的情况下[19],抗原快速检测对于弥补基层疫情防控短板,并提升常态化防控效率可具有重要价值。
1. 抗原快速检测可成为核酸检测能力薄弱的基层地区的重要补充手段:对于疫情防控的关键在于及时检出感染者,尤其是高传染性病例。此前在东北、华北地区出现的疫情,多以农村、乡镇等基层地区为主,而核酸检测对于检测条件要求较高,对于基层检测能力构建存在一定短板。抗原快速检测可作为补充手段,在核酸检测能力薄弱地区,快速建立新冠病毒检测能力,完善疫情防控体系。
2. 抗原快速检测可有助于急诊、发热门诊的快速患者分流与管理:在目前疫情防控下,对于院内感染的控制至关重要,对于发热门诊、住院患者一般要求进行核酸检测以排除感染。但随着冬春季节,呼吸道感染患者增加,发热门诊患者压力增加,而对于急诊入院/手术患者,核酸检测周转时间较长,可能对于患者处置产生一定延误。抗原检测可快速反馈结果,于发热门诊就诊患者分流,降低院内感染风险,并提高患者管理效率,并通过高传染性个体检出,可为急诊手术/入院患者的及时干预处置提供支持依据。
3. 对于抗原快速检测应用完善的建议:(1)国内临床验证进一步完善:在国内和国际机构基于疑似患者评估抗原检测与核酸检测符合率的临床研究中,抗原快速检测体现出较好的检测性能,尤其是对于高传染性患者。后续仍需要进一步对于入境点筛查、入院筛查等无症状人群检测价值的临床评估,以更为准确指导抗原检测的应用。(2)多种呼吸道病原体联合快速检测开发:与流感季重叠情况下,通过多种病原体快速联合检测,促进对于患者快速、便捷的鉴别与管理,提高诊疗效率,并减轻医务压力,提升患者体验感。(3)完善POCT信息化管理:通过手机端、云平台等信息化管理体系搭建,结合POCT检测应用范围广且散点的特点,实现对于广泛地区的覆盖与监管预警,并通过智能化平台,提高受检者检测规范性,也可促进居家自测等实现,补足疫情防控短板。
参考文献
徐英春, 胡继红, 王瑶, 等. 新型冠状病毒实验室检测专家共识[J]. 协和医学杂志, 2021, 12(01): 18-26.
Kashiwagi K, Ishii Y, Aoki K,et al. Immunochromatographic test for the detection of SARS-CoV-2 in saliva. J Infect Chemother. 2021 Feb; 27(2): 384-386.
Mattiuzzi C, Henry BM, Lippi G. Making sense of rapid antigen testing in severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) diagnostics. Diagnosis (Berl). 2020 Nov 26:dx-2020-0131.
ECDC,Options for the use of rapid antigen tests for COVID-19 in the EU/EEA and the UK, 19 November 2020
Dinnes J, Deeks JJ, Adriano A, et al; Cochrane COVID-19 Diagnostic Test Accuracy Group. Rapid, point-of-care antigen and molecular-based tests for diagnosis of SARS-CoV-2 infection. Cochrane Database Syst Rev. 2020 Aug 26; 8: CD013705.
World Health Organization (WHO). Antigen-detection in the diagnosis of SARS-CoV-2 infection using rapid immunoassays. Geneva: WHO; 2020 [updated 11 September 2020].
Mina MJ, Parker R, Larremore DB. Rethinking Covid-19 Test Sensitivity - A Strategy for Containment. N Engl J Med. 2020 Nov 26; 383 (22): e120.
Andrew Pekosz, Charles K. Cooper, Valentin Parvu et al. Antigen-based testing but not real-time PCR correlates with SARS-CoV-2 virus culture. medRxiv.Oct 2020
Larremore DB, Wilder B, Lester E, et al. Test sensitivity is secondary to frequency and turnaround time for COVID-19 screening. Sci Adv. 2021 Jan 1; 7(1): eabd5393.
Martin Pavelka, Kevin Van-Zandvoort, Sam Abbott,et al. The effectiveness of population-wide, rapid antigen test based screening in reducing SARS-CoV-2 infection prevalence in Slovakia. medRxiv 2020. 12. 02. 20240648;
日本病原体検査の指針検討委員会.新型コロナウイルス感染症 (COVID-19) 病原体検査の指針 (第3版),22 Jan,2021.
Health department of republic of south Africa. THE USE OF ANTIGEN TESTING FOR THE DIAGNOSIS OF SARS-COV-2 IN SOUTH AFRICA,11 Dec 2020.
US CDC. Interim Guidance for Antigen Testing for SARS-CoV-2. 16 Dec 2020.
Government of Canada. Interim guidance on the use of rapid antigen detection tests for the identification of SARS-CoV-2 infection. 7 Oct 2020.
Government of Pakistan. TESTING STRATEGY INCORPORATING COVID-19 ANTIGEN DETECTION RAPID DIAGNOSTIC TESTS (Ag-RDT), 4 Nov 2020
Government of Pakistan. National Testing Guidelines for COVID-19. Version 3
Ministry of Health Malaysia. GUIDELINE ON COVID-19 TESTING USING ANTIGEN RAPID TEST KIT (RTK-Ag) FOR THE HEALTH FACILITIES IN MINISTRY OF HEALTH VERSION 5.0. 27 Jan 2021
Lee S, Kim T, Lee E, et al. Clinical Course and Molecular Viral Shedding Among Asymptomatic and Symptomatic Patients With SARS-CoV2 Infection in a Community Treatment Center in the Republic of Korea. JAMA Internal Medicine. 2020.
梁万年, 姚建红, 吴敬, 等. 我国新型冠状病毒肺炎疫情防控常态化阶段的经验与思考. 中华医学杂志, 2021, 101(00): E001-E001





