肝药酶CYP2C19基因的变 异特点与基因多态性检测技术
细胞色素P450酶系(cytochrome P450,CYP)是Ⅰ相药物代谢酶中的一个重要酶系,它是一组结构和功能相关的超家族基因编码的同工酶,主要存在于肝脏、肠道中,多位于细胞内质网上,催化多种外源性和内源性物质的合成和代谢。其中CYP1,CYP2和CYP3是P450酶系中最重要的家族,它们在许多内源性和外源性物质的代谢中扮演着重要角色[1]。药物在体内的代谢主要经过Ⅰ相反应和II相反应两个过程。其中,生物转化的Ⅰ相反应所包括的氧化、还原、水解反应所涉及的酶系主要为细胞色素氧化酶P450超家族,在该家族中CYP2是最大的家族,有15个亚家族,而CYP2C是其中最大的亚家族。CYP2C9和CYP2C19是细胞色素P450酶大家族CYP2C亚家族中两种最重要的药物代谢酶。其中CYP2C9约占人肝微粒体CYP酶总量的20%,有大约10~16%临床常用药物经由CYP2C9氧化代谢[2]。CYP2C19作为细胞色素P450的另一个重要成员,许多内源性底物、环境污染物以及临床上大约10%的药物都由其催化代谢[1]。许多细胞色素P450酶具有多态性,其中最常见的多态性是单个碱基发生突变(即单核苷酸多态性),另外还存在部分的碱基插入、缺失以及基因的复制。这些多态性是酶活性产生种族及个体差异的重要原因。根据酶活性的不同,可分为三种不同的代谢表型:正常表型、快代谢型(Extensive metabolism,EM)和慢代谢型(Poormetabolism,PM)。快代谢者具有多个P450基因的拷贝或者突变引起酶活性的增加,造成药物在体内迅速被清除,血药浓度达不到稳态血药浓度,从而造成药物治疗的失败;对慢代谢者而言,药物在体内的清除减慢,引起血药浓度显著升高,容易引起蓄积中毒。
一、CYP2C19基因多态性及其频率分布
CYP2C19基因位于第10号染色体长臂(10 q 24.1-10 q 24.3)上(如图1),包括9个外显子和5个内含子,编码区共编码490个氨基酸,分子量约为55KDa,其中第421至432位氨基酸为血红素结合位点[41,42]。
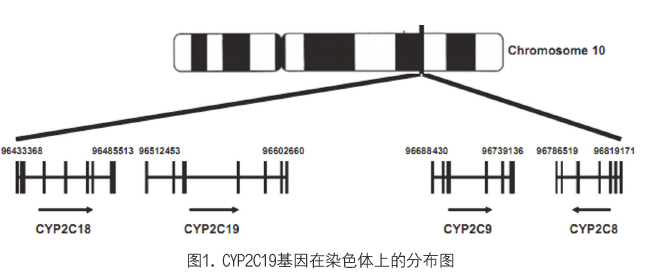
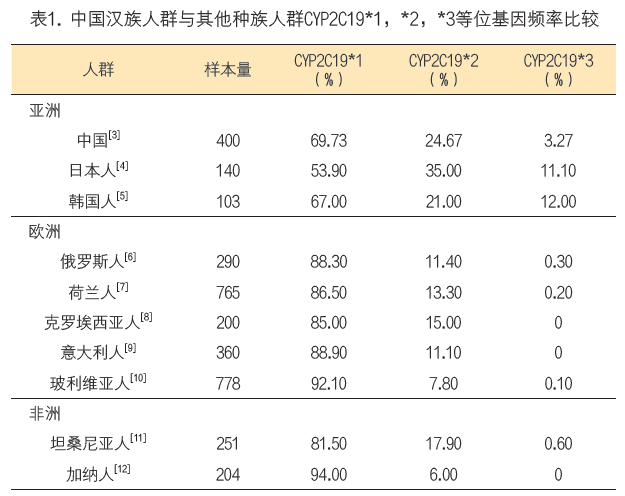
1994年,De Morais等先后发现了CYP2C19的两个等位基因:CYP2C19m1(2型等位基因)和CYP2C19m2(3型等位基因),并证明了S-美芬妥英氧化代谢多态性与该二等位基因有关[43,44]。CYP2C19基因具有遗传多态性,迄今为止,国际上已经命名的等位基因共有39种(https://www.pharmvar.org/gene/CYP2C19),除野生型外,其他突变类型均引起了CYP2C19基因编码区氨基酸发生改变。当前,研究较为深入的等位基因主要包括3种:CYP2C19*1(野生型),CYP2C19*2(681G>A)和CYP2C19*3(636G>A)。CYP2C19*2在基因外显子5中发生G>A突变,从而产生了一个异常的剪接位点,引起40bp的碱基缺失,改变了mRNA的阅读框,使蛋白的合成过早被终止,生成了一个缺乏血红素结合位点的无功能酶蛋白[43]。CYP2C19*3在外显子4的636位处发生G>A突变,产生了未成熟的终止密码子,该终止密码子代替了色氨酸,导致蛋白合成提前终止,该突变产生了211个氨基酸的蛋白,该蛋白因缺乏血红素及底物结合区而无活性[44]。研究表明CYP2C19*2和CYP2C19*3两种突变等位基因可解释超过99%的东方人和87%的白种人的慢代谢(PM)表型,其中2型突变是引起慢代谢(PM)的主要原因,该突变主要存在于亚洲人群,在高加索人群和黑种人群中比较罕见。不同人群和国家之间CYP2C19主要等位基因频率分布的比较见表1。
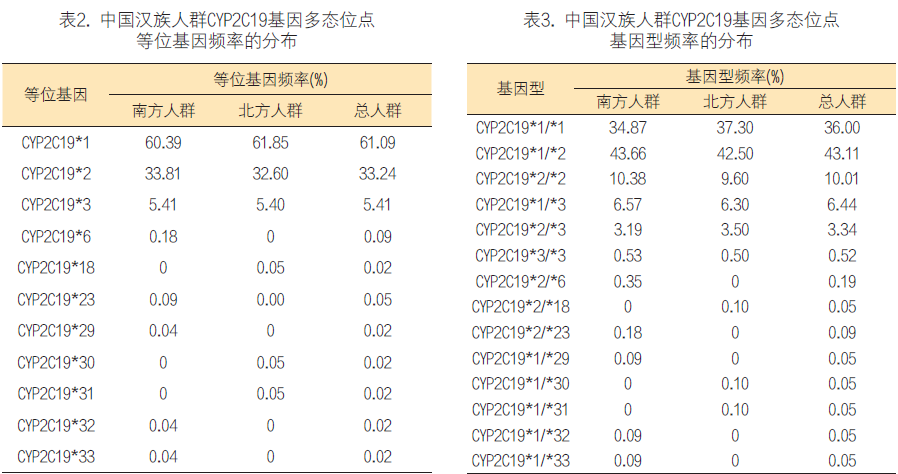
北京医院蔡剑平和温州医科大学胡国新研究团队基于2000余份人群血样,对CYP2C19基因的9个外显子进行扫描分析共发现44个SNP位点[13]。结果表明,在中国人群中分布6种等位基因,包括CYP2C19*1,CYP2C19*2,CYP2C19*3,CYP2C19*6,*18,*23等。结果表明CYP2 C 1 9 * 1(野生型)是最常见的等位基因,其频率为61.09%,CYP2C19*2和CYP2C19*3是最常见也是最重要的突变型等位基因,它们的等位基因频率分别是33.24%和5.41%,该团队首次在亚洲人群中发现CYP2C19*6等位基因。另外,研究首次发现了34种新突变,在这些新突变中有23种为非同义突变(突变引起编码区氨基酸改变),其中11种非同义突变已经被人类细胞色素P450命名委员会所命名,分别为CYP2C19*2E-CYP2C19*2J,CYP2C19*3C和CYP2C19*29-CYP2C19*33。此外,以往的研究并没有报道CYP2C19基因存在插入突变,本研究首次发现一
例样本在CYP2C19基因的第一外显子中插入了5个碱基。这些突变都属于罕见变异,等位基因频率均小于0.1%。
研究还发现了另外两种报道频率较低的等位基(0.05%)。在各种检测到的基因型中,南北地区没有显著性差异。对于野生型等位基因CYP2 C 1 9 * 1,36%的个体是纯合基因型CYP2C19*1/*1。对于缺陷型等位基因C Y P 2 C 1 9 * 2 和C Y P 2 C 1 9 * 3 , 4 3 . 1 1 % 的个体属于杂合基因型CYP2C19*1/*2,10.01%个体属于纯合基因型CYP2C19*2/*2,6.44%携带杂合基因型CYP2C19*1/*3,3.34%携带基因型CYP2C19*2/*3,0.52%携带纯合基因型CYP2C19*3/*3。
二、CYP219药物代谢酶检测的临床意义
随着药物遗传学的发展,人们已认识到各种族间和个体间用药剂量的差异与药物代谢酶的遗传多态性相关。由于不同个体存在药物代谢方面的差异,因而给药后可能会出现严重的不良反应或药物剂量不足,从而导致治疗的失败。CYP2C19酶参与几十种临床常用药物代谢,包括血小板聚集药、抗抑郁药、五羟色胺再摄取抑制剂(SSRI)、镇静催眠药、抗真菌药、抗疟疾药等。表4列出了部分CYP2C19代谢的药物。
表4 CYP2C19代谢的药物
|
分类 |
药物 |
|
抗血小板药 |
氯吡格雷 |
|
普拉格雷 |
|
|
噻氯匹定 |
|
|
质子泵抑制剂(PPI) |
奥美拉唑 |
|
艾司奥美拉唑 |
|
|
兰索拉唑 |
|
|
泮托拉唑 |
|
|
巴比妥类药 |
环己巴比妥 |
|
甲基苯巴比妥 |
|
|
苯巴比妥 |
|
|
苯二氮卓类药 |
地西泮 |
|
氟硝西泮 |
|
|
夸西泮 |
|
|
氧异安定 |
|
|
咪达唑仑 |
|
|
三唑仑 |
|
|
阿普唑仑 |
|
|
艾司唑仑 |
|
|
抗癫痫药 |
苯妥英钠 |
|
五羟色胺再摄取抑制剂(SSRI) |
西太普兰 |
|
氟西汀 |
|
|
舍曲林 |
|
|
帕罗西汀 |
|
|
三环类抗抑郁药 |
阿米替林 |
|
丙咪嗪 |
|
|
氯米帕明 |
|
|
多虑平 |
|
|
抗真菌药物 |
伏立康唑 |
|
抗疟疾药 |
氯胍 |
三、CYP2C19基因多态性检测技术
单核苷酸多态性(SNPs)主要指在基因组水平上由单个核苷酸的变异所引起的DNA序列多态性,占所有已知多态性的90%以上。SNP在人类基因组中广泛存在,平均每500-1000个碱基对中就有1个。SNP作为不同个体在某一特定位置上的核苷酸差异,它具有数量大、分布广及高度稳定性、易于批量检测等特点,作为第三代的遗传标记在临床检验、病原学检测、法医学、分子诊断、新药研发以及遗传疾病等方面具有重要应用价值。目前常见的SNP检测技术有如下几种。
1. 基于酶或PCR的方法:这类方法是目前SNP检测中最常用的一类方法,和杂交基础上检测方法
相比增加了一步酶催化反应。因此提高了检测的忠实和可靠性。(1)ARMS:又称等位基因特异性PCR(PCR amplification of specific allele,PASA), 此类方法是根据PCR过程中要求引物和模板间的严格互补配对来实现对SNP位点的检测。(2)双向等位特异法(Bi-PASA):是在等位基因特异性PCR法的基础上发展起来的[18]。其原理是在PCR反应体系中,所设计的引物3’端与一条待测等位基因的序列互补,而与另一条等位基因的序列不互补。该方法虽然可检测出SNP,但实验步骤繁琐,对引物设计要求较高。其优点为操作简单易行、经济,缺点是该方法在液相中进行,因此多重平行反应数量有限,难以实现SNP的高通量检测。(3)荧光定量PCR技术(TaqMan技术):也称为核酸外切酶法,是在PCR过程中实现等位特异性杂交,而不需以往等位特异性杂交中样品PCR后分离及洗涤等步骤。TaqMan探针基于杂交原理,是按常规方式进行体外基因扩增,在反应体系中加入针对位点及侧翼序列设计的探针,该探针只有一个碱基的差异,分别对应于不同的等位基因,并用荧光标记探针。这种检测方法的优点是闭管进行,因而
减少了PCR污染的风险,但探针标记的成本较高,且因其采用荧光淬灭及双末端标记技术,淬灭难以彻底,本底较高[19]。
2. 分子内标法:该方法利用荧光染料内标寡核苷酸制成探针,探针与互补的DNA序列杂交时,发出的荧光强度比未杂交的单链高许多。荧光强度的变化可以用来监测实时聚合酶链式反应(PCR)反应进程和链熔解曲线,从而识别SNP的变化。
3. DNA芯片技术:基因芯片是在固相支持介质上进行分子杂交并原位荧光检测的一种高通量SNP分析方法。根据核苷酸的碱基配对原理,设计两种或多种探针,在优化操作后,探针只与其完全互补的序列杂交,不与含有单个错配碱基的序列杂交[20]。待测基因经提取扩增、荧光化学标记后,与固定的探针进行杂交。可根据荧光强弱或荧光的种类检测出被检序列的碱基类别。由于该技术可以将大量的探针同时固定于支持物上,所以一次可以对大量的生物分子进行检测分析,从而解决了传统核酸印迹杂交技术复杂、自动化程度低等问题,包括杂交型芯片、电促核酸杂交芯片等。
4. 变性高效液相色谱法(DHPLC):该检测方法的原理为:纯合双链DNA分子的分离类似于阴离子交换层析,离子对反相高效液相色谱法借助吸附在固定相表面的三乙氨基乙酸离子的正电荷与DNA分子的磷酸二酯基团的负电荷间的相互作用,对双链DNA分子按长度进行分离。DHPLC检测方法可全自动化操作,筛检SNP的效率优于各种电泳法[21]。
5. 质谱检测技术:基质辅助激光解吸附电离飞行时间质谱(MALDI-TOF-MS)在SNP的检测中已得到应用[22]。引物延伸法结合MALDI-TOF-MS是利用质谱技术检测SNP中常用的一种形式,其原理是将变性的单链产物通过与硅芯片上的化合物共价结合后,在硅芯片上进行引物的退火、延伸反应、突变部位配对的碱基与正常配对的碱基不相同。根据引物在延伸反应中所结合的不同碱基的不同质量在质谱仪上显示不同峰。可批量检测,具有快速、准确、自动化程度高和高通量等特点,但主要的问题是需对分析样品进行纯化后才能检测。
6. 焦磷酸测序技术(pyrosequencing):焦磷酸测序技术是由4种酶催化的同一反应体系中的酶级联化学发光反应,焦磷酸测序技术的原理:引物与模板DNA退火后,在DNA聚合酶(DNA polym erase)、ATP硫酸化酶(ATP sulfurytase)、荧光素酶(1uciferase)和三磷酸腺苷双磷酸酶(Apyrase)4种酶的协同作用下,将引物上每一个dNTP的聚合与一次荧光信号的释放偶联起来,通过检测荧光的释放和强度,达到实时测定DNA序列的目的 。
7. 多元焦磷酸测序:该方法在焦磷酸测序的基础上发展起来的一种SNP检测方法,目前该方法已实现自动化,适合于高通量SNP的检测。
四、展望
我国已经步入老龄社会,衰老导致机体药代动力学和药效动力学改变,老年患者具有特殊的药代动力学及药效学点,是多病共存和多药共用的特殊群体药物相互作用及药物不良反应的主要受害者。药物相互作用包括药物之间的协同作用和拮抗作用,可以发生在药代动力学和药效学的任何阶段,研究最多的是细胞色素P450氧化酶(cytochrome P450 oxidases,CYP450),而其中又以CYP2C19最为常见。CYP2C19显著的多态性容易改变药物的药动学特征,导致药效的增强或减弱,从而引起相关的不良反应或者药物治疗的失败。同时CYP2C19基因突变不仅影响酶活性,而且也影响CYP2C19酶的抑制和诱导,对于治疗窗狭窄的药物,这将引起严重的临床后果。随着个体化用药基因检测技术的日新月异,必将促进我国的合理用药水平提升新的台阶。




