WHO丙型肝炎病毒自我检测指南 (2021) 解读与分析

康可人,博士,高级工程师,南方科技大学业界导师,广东食品药品职业学院客座教授,国家科技部评审专家,广州市高级专业技术资格评审委员会入库委员。现任广州万孚生物技术股份有限公司高级副总裁。荣获2017年度国家科学技术进步奖二等奖、2018年度广东省科技进步奖二等奖。近年来负责及参与的国家、省、市级科研课题30余项,发表SCI论文及国内核心期刊论文20余篇,授权专利4项,参与《即时即地检验技术与应用》等多部行业教材及专著编写。

邹嘉琪,广州万孚生物技术股份有限公司医学中心主管。2018年毕业于华南农业大学动物科学学院,分子遗传与育种方向农学硕士,曾参与撰写2019-2020年卷《中国体外诊断产业发展蓝皮书》。
丙型肝炎病毒(Hepatitis C virus,HCV)感染是世界范围内慢性肝病的主要病因。根据世界卫生组织(Word Health Organization,WHO)估计,现有约5800万人感染HCV,这种疾病对于低收入和中等收入国家负担是非常高的[1]。WHO启动了2016-2021年全球卫生部门肝炎战略,提出“2030年消除病毒性肝炎公共卫生威胁”的战略目标[2-3],具体指标包括:新发感染率降低90%,病死率降低65%。为消除病毒性肝炎作为公共卫生威胁,需要90%的感染者得以诊断以及80%确诊的患者得以治疗[4]。然而,当前在全球范围内,只有不到20%的HCV感染者接受检测,不到四分之一的确诊患者得到治疗[1]。截止2019年,全球HCV感染者的诊断率只有21%;而我国HCV的累积确诊率为30%,累积治疗率仅9%[5],距离2030年消除HCV的目标仍有很大差距,因此消除HCV迫在眉睫。
当前,HCV感染者的抗病毒治疗已经进入直接抗病毒药物(Direct Antiviral Agents,DAA)的泛基因型时代,使得HCV成为可治愈的疾病。且国内外指南推荐的HCV一线DAA治疗药物来迪派韦/索磷布韦、索磷布韦/维帕他韦以及艾尔巴韦/格拉瑞韦已经进入国家医保目录,药品价格的大幅度降低增加了我国丙肝患者DAA药物的可及性,可以提高丙肝患者的治愈率。因此,有效筛查HCV感染者成为消除HCV的重要环节,但也是目前的问题所在。要达到2030年消除HCV这一目标,就需要采用创新的方法和服务模式,帮助人群了解HCV,并使他们获得治疗和护理服务。HCV自测(Hepatitis C virus Self-Testing,HCVST)是提高筛查HCV感染者的一种有效策略,可以加速实现全球消除丙肝病毒目标的进程。因此《丙型肝炎病毒的自我检测指南建议》(以下简称2021指南)[6]应时而生,该指南由WHO发布于2021年7月,主要针对丙型肝炎病毒的自我检测提供建议和指导。本文将从HCVST检测流程、实施HCVST的可行性和实施HCVST的注意事项三方面对《丙型肝炎病毒的自我检测指南建议》进行解读。
一、HCVST检测流程
HCVST指的是检测者通过收集自己的血液或唾液样本,应用快速诊断检测试剂盒进行检测,然后在一个私密的空间内,单独或者和他们信任的人一起解释他们的检测结果。它与艾滋病毒自我检测(HIV Self Testing,HIVST)一样,HCVST不能提供直接的诊断结果,需要额外的检测来确诊。所有HCVST检测结果需要由训练有素的专业人员根据国家算法进行检测和诊断确认是否HCV感染以及是否需要接受治疗(图1)。同时,WHO还建议受检者进行核糖核酸(RNA)或丙型肝炎病毒核心抗原(HCV cAG)检测,以确定是否HCV感染,并在开始治疗前进行临床评估。
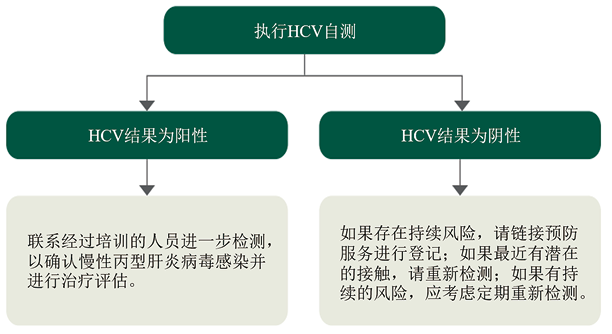
图1. HSVST检测流程
WHO于2017发布了首个全面的乙肝和丙肝检测指南(以下简称2017指南)[7],2017指南建立在HIVST在一系列环境中成功实施的经验基础上。它主要侧重基于设施和社区的检测方法,并强调HCVST是未来减少HCV诊断差距的潜在方法。2017指南建议的检测方法基于不同的流行病学背景,并对特定的地区和特定人群采取重点检测,比如慢性病毒肝炎的家人、小孩、性伴侣以及医疗人员等。2017指南的制定对HCV和其他病毒感染(包括乙型肝炎、艾滋病毒、结核病、性传播感染等)或面临感染风险的人群起着非常重要的作用。然而,2017指南建议使用的是一种单一、质量保证的血清学体外诊断(IVD)试验或者实验室免疫分析法来检测HCV抗体。HCV抗体是通过定性/定量的RNA测试判定HCV感染,但该方法具有局限性,容易漏检初期HCV感染患者。2021指南将弥补2017指南HCVST检测的空白,并将HCVST作为HCV检测的附加方法。2021指南建议,根据国家标准,HCVST需要与适当的检测后服务挂钩,包括确认病毒感染、治疗、服务、转诊服务等。HCVST服务的提供与支持也应适应国家和当地环境,包括社区偏好。社区应积极有效地参与HCVST项目的开发、调整、实施和监测。
二、实施HCVST的可行性
1. 实施HCVST的利与弊:根据2021指南,WHO研究小组对HCVST和HIVST进行了系统评价,然而由于缺乏HCVST相关研究证据,只能将HIVST研究证据作为间接证据对HCVST进行评价。2021指南在对HIVST进行系统性评价时,纳入了27项随机对照试验,将HIVST与标准实验室的HIV检测进行了比较,结果表明,无论在重点关注人群还是一般人群,HIV检测的接受率持续增加。一项荟萃分析也发现使用HIVST进行HIV检测的总体比例比使用标准实验室的HIV检测服务高出77%。而在一项针对注射吸毒者的观察性研究表明,实施HIVST后,HIV检测增加了两倍多[8]。这些研究表明,HIVST比基于标准实验室的HIV检测在人群中的接受度更高,也提高了HIV检测率。
2021指南还对HIVST确诊后护理和不良事件进行了调研。研究发现,它与HIV护理相关的比例可与基于实验室的HIV检测相媲美;而与标准实验室的HIV检测相比, HIVST的社会危害或不良事件的发生率是没有统计学差异的。
基于以上HIVST相关研究,WHO研究小组评估了HCVST的适用性和相关性,并确定:(1)在许多情况下,HIV和HCV的优先人群是重叠的,包括男男性行为者和注射吸毒者;(2)HIVST在人群中接受度更高;(3)自我检测后的干预和随访步骤足够相似;(4)HIVST审查的结果与HCVST高度相关并适用。综上所述,WHO研究小组确定HCVST的总体好处大于其潜在危害,由此建议HCVST作为HCV的附加检测,以消除现有的HCV检测覆盖范围大的差距,向消除HCV提供有力武器。
2. HCVST可用性评估:WHO研究小组也找到了在对多国对HCVST可用性和可行性的相关研究,总的来说HCVST在人群中具有高接受度;大部分参与者也表示会像朋友和家人推荐HCVST;在进行HCVST时,大多数参与者能够正确使用HCVST试剂盒,大多数参与者也表示自检包很容易使用,包括样本采集和实时检测。由于HCVST尚未大范围推广,在推广初期可考虑现场演示、协助或视频指导,这有利于人们在自检过程中减少操作失误,从而提高检测结果的可信度。
对HCVST的检测成本和成本效益进行评估发现,HCVST每次诊断使用的费用比基于实验室的HCV检测更有效,实施HCVST会使更多感染者被诊断和治愈。如果考虑降低HCVST价格,可能更有利于HCVST的大范围推广,HCVST在人群中的可及性也会更高。
综上所述,HCVST是值得大范围推广和使用的,如果将HCVST使用者与确认性检测和治疗联系起来,并优化转诊途径,将会大大降低HCV治疗的成本,也将大大提高HCV治疗的可及性。
三、实施HCVST的注意事项
在全球范围内,对HCV的公共卫生应对措施正在演变,各国和各地区之间存在重大差异。虽然越来越多国家正在制定国家病毒性肝炎规划和计划,但是很多低收入或中等收入国家和地区往往没有足够的资金支持。因此,2021指南推荐应该从战略上实施HCVST,以实现消除HCV的总体目标。
2021指南还指出,对于任何HCV检测,都应将重点放在负担最大、检测和治疗覆盖面差距最大的地区和人群。因此首先要分析和评估现有的国家HCV检测规划,以确定差距,使HCVST能够更好地补充现有的服务并解决这些差距。而当决策者在引入HCVST时需要考虑的注意事项如下:
1. 审查方案数据,了解检验差距,确定优先人群:(1)需要提供有利的政策环境:首先审查现有国家政策,以更新现有政策,增加支持HCVST作为HCV检测的补充手段。也可根据需要指定标准的操作程序和培训手册。其次审查国家体外诊断产品(In Vitro Diagnosis,IVD)的监管和注册政策,消除获得有质量保证的HCVST产品的障碍。最后审查现有的WHO资格预审合格的产品以及使用WHO合作注册的产品,加快国家注册程序,构建采购、物流和供应链解决方案。(2)社区动员:使其参与贯穿整个设计、实施和检测方法,制定适当的和特定情况的信息、资源和工作助手。(3)需求产生和动员活动:提高人群对HCVST的认识,可通过开展社会营销和推广活动来促使人群对HCVST产生需求。(4)资源考虑:建立可持续发展的人力和财力资源。
2. 设计检测交付模型,将模型和重点人群相匹配:交付模型的合理设计可以提高HCVST产品的可及性和HCVST的使用率,因此模型设计至关重要,在设计检测交付模型时,需要考虑如下几点要素:(1)HCVST的预期目标用户:HCVST的目标人群应该包括一般社会人群、特定年龄组人群、有性接触的群体以及注射吸毒群体等。(2)工具包的分发地点:可在设施、社区、场地和固定或移动的服务站点。(3)工具包分发时间与方式:可实行持续、偶然或基于某次事件/活动进行安排分发工具包的时间和频率。(4)工具包分发者:面对面分发可由供应商、同行、客户作为分发者;非面对面分发可采用自动售卖机让用户自行购买,或者由快递员为用户提供送货上门服务。
除设计检测交付模型外,还需要优化支持工具和选项,即在自检期间和自检之后为自检人群提供一个支持包,该支持包可通过多种方式提供,例如现场、视频、虚拟或电话等。此外,需要开发高效有用的转诊途径,为确诊感染HCV的患者提供治疗、护理以及前期预防等服务。为降低成本,可考虑与HIVST方案(视流行病学情况而定)等其他服务相结合的模式。
3. 数据收集:用于方案监测、评估的指标和数据收集系统:在可行和适当的情况下,使用和加强现有的数据收集系统,对方案监测和评价是很有必要的。数据收集系统可通过适当的信息来减轻风险、危害和不良事件的发生;必要时可监测HCVST的潜在伤害并建立补救方法;定期审查数据也可以帮助完善方案,优化设施;最重要的一点是可在上市后对HCVST工具包进行监督。
四、小结与分析
当前,HCV感染仍是一个主要的公共卫生问题[9]。DAA出现彻底改变了HCV治疗领域,推动了2030年消除HCV的进程[10-11]。为实现消除HCV的战略目标,需要创新的方法,许多国家和地区都需要安全且对用户友好的HCV服务提供模式。HCVST的出现,将改变现有的格局。尽管没有确定关于HCVST益处和危害的直接证据,但来自HIVST系统评价的证据发现,与基于标准实验室的HCV检测相比,HCVST提高了HCV的检测率和总体阳性率;与额外检测的关联、护理/治疗的关联或不良事件的关联率没有统计学差异。测试误用和不良事件的发生率也较低,基于以上证据,WHO研究小组决定不降低间接性证据的可信度,表示HCVST的可行性总体是中等的。
综上所述,HCVST可以像目前HIVST一样被人群接受,作为传统HCV检测的补充方法,可以有效地应用到现实世界的公共卫生防控当中。
参考文献
[1]World Health Organization. Progress report on HIV, viral hepatitis and sexually transmitted infections 2019: accountability for the global health sector strategies, 2016-2021[R]. World Health Organization, 2019.
[2]Hutin YJ, Bulterys M, Hirnschall GO. How far are we from viral hepatitis elimination service coverage targets? J Int AIDS Soc. 2018; 21(Suppl 2(Suppl Suppl 2)): e25050.
[3]World Health Organization. Global health sector strategy on viral hepatitis 2016-2021. Geneva: WHO; 2016.
[4]中华医学会肝病学分会, 中华医学会感染病学分会. 丙型肝炎防治指南(2019年版)[J]. 中华传染病杂志, 2020, 38 (01): 9-28. DOI:10.3760/cma.j.issn.1000-6680.2020.01.004.
[5]https://cdafound.org/dashboard/polaris/dashboard.html.
[6]Recommendations and guidance on hepatitis C virus self-testing [Internet]. Geneva: World Health Organization; 2021 Jul. PMID: 34370425.
[7]Guidelines on hepatitis B and C testing. Geneva: World Health Organization; 2017 (https://apps.who.int/iris/handle/10665/273174, accessed 29 June 2021).
[8]Kravchenko N, Denisiuk O, Kuznetsova J, et al. Engaging people who inject drugs and their peers in HIV testing and harm reduction in Ukraine: do they make a difference?[J]. The Journal of Infection in Developing Countries, 2019, 13(07.1): 118S-125S.
[9]WHO. Global hepatitis report, 2017. Geneva: WHO; 2017.
[10]WeiL, LimSG, XieQ, et al. Sofosbuvir-velpatasvir for treatment of chronic hepatitis C virus infection in Asia: a single-arm, open-label, phase 3 trial[J]. Lancet Gastroenterol Hepatol, 2019, 4(2): 127-134. DOI:10.1016/S2468-1253(18)30343-1.
[11]ZeuzemS, FosterGR, WangS, et al. Glecaprevir—pibrentasvir for 8 or 12 weeks in HCV genotype 1 or 3 infection[J]. N Engl J Med, 2018, 378(4): 354-369. DOI:10.1056/NEJMoa1702417.
作者单位:510641广州市, 广州万孚生物技术股份有限公司
通讯作者:康可人,510000广州市,广东省即时检测(POCT)企业重点实验室




