微流控技术在病原诊断中的应用

王永成,现为浙江大学医学中心/良渚实验室研究员、博士生导师,浙江大学医学院附属第一医院双聘研究员。于2020年获得哈佛大学化学与生物化学博士学位,师从美国三院院士David Weitz教授,主要从事微流控技术的开发及应用,目前的研究重点是开发基于微流控平台的单细胞和单细菌分析技术。总共发表了31篇论文,其中有7篇论文入选ESI高引用论文,论文共被引用3435次。以第一或共同第一作者在影响因子大于10的期刊上发表了10篇文章,总影响因子约177,被引用1637次,其中有3篇论文入选ESI高引用论文,有3篇被选为封面文章。已申请10项专利,部分成果得到转化。
【摘要】微流控分子诊断技术是通过将样本处理,核酸扩增,结果判断集成到一台仪器或芯片上,实现从“样本-结果”的全流程自动化操作。在病原的检测上,成熟的微流控检测设备不仅可以最大限度的缩短检测时间,降低对专业技术人员的要求,避免环境污染以及操作人员感染,因此在即时检验(point-of-care testing,POCT)领域的应用前景广阔。本文综述了现阶段不同微流控分子检测仪器的技术原理,包括现有的商业化微流控检测仪器和实验室阶段的研究进展。希望能够加深对于微流控病原菌分子检测技术的了解,并对未来微流控技术的发展提供一些展望。
【关键词】微流控;病原微生物;分子检测
病原微生物包括细菌、真菌、病毒等,微生物感染会导致结核病、肝炎、脑炎和败血症等感染性疾病。随着经济贸易、人口流动频率增加,感染性疾病已严重威胁人类的身体健康。在新冠疫情爆发中,人员流动和经济活动给疫情防控带来极大的挑战,而对病原菌及时、准确的诊断是阻断和治疗感染性疾病的前提条件。
目前鉴定和检测病原体的方法很多,如培养法、基质辅助激光解吸电离飞行时间质谱(MALDI-TOF MS)、抗体检测、聚合酶链式反应(PCR)等。然而,最经典的方法是培养法,但该方法需要设备齐全的实验室及3到7天的培养时间,不适合现场快速检测病原菌[1]。飞行时间质谱是近年来快速发展起来的一种检测生物大分子的重要手段,被认为是快速鉴定临床微生物的新利器,但仍然离不开微生物培养步骤。抗体检测的敏感性受检测方法、采样时间、疾病的严重程度等因素影响较大。此外,由于DNA污染,PCR有时也容易产生假阳性结果[2, 3]。因此,开发简便、灵敏度高、不受环境条件限制的病原检测技术显得尤为重要。
微流控技术以其便携、小型化、自动化等优点被广泛应用于细菌、分子、重金属等不同物质的检测中[4, 5]。微流控芯片通常由聚碳酸酯、玻璃、石英或热塑性材料制成,然后利用微处理技术将微阀门、微泵、微混合器、微电极集成到微米、纳米级芯片上,形成一个网络状系统,可实现样品的预处理、混合、反应、分离和检测[6]。在液体的驱动上,形成了以活塞驱动、气阀驱动和离心驱动等不同的动力模式,使处理液能够在不同的腔室中按照预设的路线进行流动;病原菌核酸释放上,也有电击破碎、化学试剂裂解、物理撞击和超声破碎等形式;此外,微流控技术可以与多种检测技术相结合,包括PCR、LAMP、质谱、荧光光谱等,真正实现样本进、结果出的一体化操作系统[7-10]。因此,该技术在分子诊断领域受到了广泛的关注,并在point-of-care(POC)检测中得到了进一步的发展[11-13]。本文将综述微流控技术在病原诊断产品中的应用及相关的案例报道。
一、微流控技术在商业化诊断产品中的应用
微流控(Microfluidics)指的是使用微管道 (尺寸为数十到数百微米)处理或操纵微小流体的系统所涉及的科学和技术,在生物医学、分析化学、疾病诊断、药物筛选等领域有广泛的应用。微流控技术的应用极大促进了临床上的病原菌检测效率,使得基于核酸的“即时检验(point-of-care,POC)”成为可能。其中,较为典型商业化的微流控检测设备往往都包含一个一次性的“检测盒(袋)”,可以在系统内部完成所需的机械传动、加热和信号读取等操作[14]。以下分别介绍了三种常见的商业化微流控设备以及它们的检测原理。
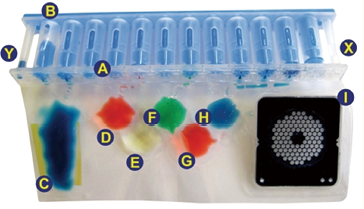
图1. Filmarray检测袋结构图。
A:试剂储存管;B:柱塞;C:细胞裂解腔;D和E:核酸纯化腔;F和G:第一步PCR扩增区;I:第二步PCR检测室;X:复溶液加入管;Y:样本加入管
1. 生物梅里埃—FilmArray™系统:Filmarray检测袋分别为试剂储存区、细胞裂解腔、DNA或者RNA纯化腔、第一扩增室和包含了102个微整列的第二步扩增检测室[15]。储液区(图1 A)中以冻干粉的形式储存了裂解、清洗和PCR反应所需的试剂,储液管保持真空状态。外接的气动阀通过连接“B”驱动各反应液进入到检测袋中,而另一个气动装置直接作用于各个腔室的气囊,调节液体在各个腔室之间的流动。
使用前,将复溶液从“X”中注入到各贮液管中,而样本从“Y”口注入到检测袋中进入到装裂解腔“C”,在陶瓷破碎珠和外接装置的机械力学作用下破碎病原菌释放核酸。核酸释放液在核酸腔室“E”中,被提前装载的磁珠固定,并在检测袋外的磁场作用下与缓冲液配合对核酸进行清洗。核酸进入到腔室“F”并与其中的PCR/RT-PCR试剂进行混合,气动阀操作液体在“F”和“G”腔室中来回混匀,在外接温度控制模块的控制下进行逆转录和第一步PCR扩增。之后产物在经过稀释后被分配到“I”的微阵列中进行检测并收集荧光信号,整个鉴定的时间大约为1h[16]。
2. 赛沛公司的GeneXpert分子诊断系统:GeneXpert是一种由程序驱动的盒式检测控制仪器[17],并安装了荧光检测和热循环控制系统(图2 A),与一次性的检测盒连接。基于微流控的GeneXpert检测盒内部设置多个腔室,用于储存裂解液、纯化和洗脱所用的缓冲液以及所有RT-PCR所需的引物探针、酶和缓冲液,同时设置了1个腔室专门储存样品处理废物。检测盒中心是一个注射器筒,它通过注射器与GeneXpert连接,利用注射筒的拉动驱动液体在不同的腔室之间流动,同时注射筒的拉动也可以对溶液起到混匀的作用。旋转阀则控制着液体在各个腔室中的流动。微生物的裂解步骤主要在检测盒底部进行(图2 B),当进入微生物裂解步骤时,GeneXpert的超声发生装置连接到检测盒底座,从而将病原菌裂解释放核酸[18]。核酸扩增与检测部分,检测盒连接一个检测和主体的类三角形PCR管,管中提前储存了qPCR检测所需的试剂。当插入GeneXpert系统时,PCR管在温度控制模块的控制下进行加热或者冷却,以达到核酸扩增的目的,同时利用光学检测模块收集信号,对PCR产物进行实时检测[16]。GeneXpert集成了样本预处理、微生物破碎、核酸纯化、以及qPCR检测,实现了从样本到结果的全自动化流程[19-20]。
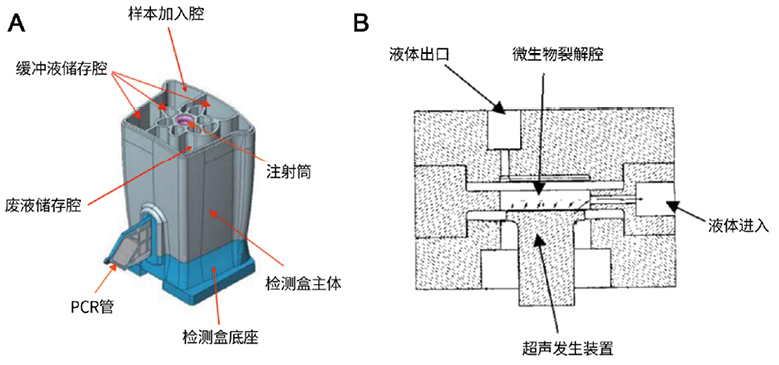
图2. Genexpert检测盒示意图。
A:检测盒结构示意图;B:微生物裂解室示意图
3. 博奥晶典-新型冠状病毒2019-nCoV核酸检测试剂盒(全集成碟式芯片法):博奥微流控核酸分析仪由离心式微流控检测芯片、离心、加热和光学检测模块组成(图3)。离心式微流控芯片具有2个平行的反应组件,可同时分析2个样品[21]。每个模型包括3个主要模块,即核酸提取、逆转录-预扩增和扩增检测部分。通过将灭活样本直接插入到芯片中,在外界离心装置的驱动以下液体逐渐由中心流经各个腔室,并释放核酸,多余的废液被收集到图中“8”的废液收集腔中,核酸利用RT-RPA的方式进行逆转录和恒温扩增,得到的样本再进行稀释被分配到LAMP区域扩增并收集光学信号。实现在45min之内对2019-nCoV多位点的检测的目的。
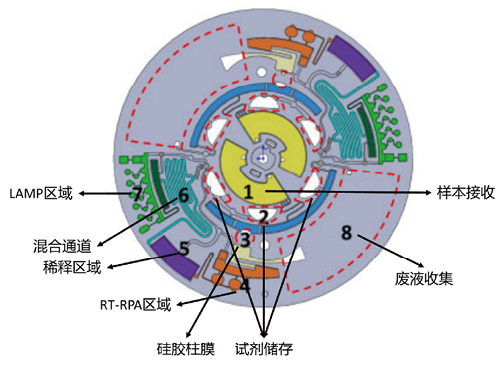
图3. 微流控核酸分析仪结构俯视图
二、实验室阶段应用案例
Schulz等介绍了一种基于离心方式的微流控即时检测系统[22],可直接从鼻拭子样本中快速检测耐甲氧西林金黄色葡萄球菌(MRSA)、甲氧西林敏感金黄色葡萄球菌(MSSA)和耐甲氧西林凝血酶阴性葡萄球菌(MR-CoNS)。这种新方法可以在一小时取得实验结果。这种完全自动化的离心微流控平台被称为LabDisk。LabDisk包括取样拭子腔、试剂预存储、样本分配、葡萄球菌特异性酶解和菌种耐药基因鉴定等操作单元(图4),可以对试剂进行定量释放,通过离心、气泵实现液体转移,进一步使用葡萄球菌特异性降解酶对样本进行裂解,采用微流控分液技术将产物分离成上万个液滴,最后通过RPA恒温扩增采集荧光信号。通过对临床分离物和鼻拭子样本进行LabDisk分析,可将MRSA的检测限(LOD)降至3±0.3 CFU/ul。
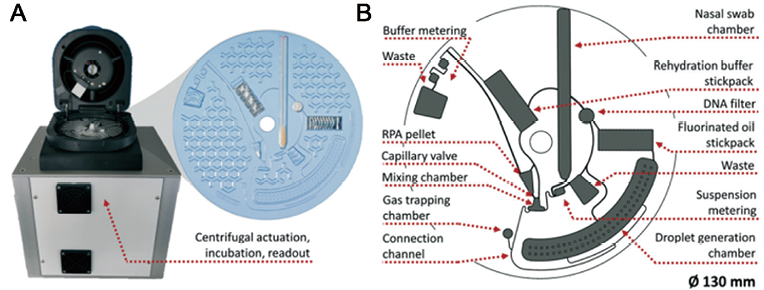
图4. POCT系统示意图
A. 用于放置LabDisk的仪器;B. LabDisk结构示意图
Abafogi等报道了一种3D打印模块化微流体装置(3DpmµFD)[23],该装置可预浓缩全血中的细菌并纯化其基因组DNA。整个微流体装置由W形微通道和锥形微室组成(图5)。在该装置中,抗体偶联磁性纳米颗粒在W形微通道中以5mL/min的速度从血液中磁性捕获靶标细菌,而在锥形微室中以2mL/min的速度用磁性二氧化硅珠获得预浓缩细菌的纯化基因组DNA。在锥形微室与微通道连接处设计旋转阀,可以减少磁性二氧化硅珠暴露于血液中,减少其对DNA纯化的干扰。2.5mL血液的预处理过程可以在50分钟内完成。通过使用微流体装置3DpmµFD对大肠杆菌进行测试,其最低检测限可达10CFU/mL。
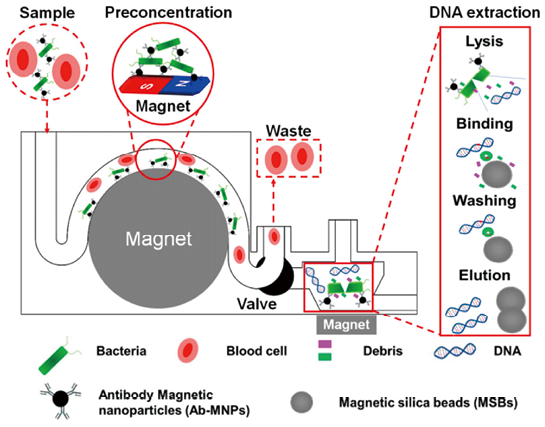
图5. 3DpmµFD法预浓缩细菌和纯化血液中细菌基因组DNA的示意图
Yu-Dong Ma等研究开发了一种自驱动微流控装置(图6)[24],通过反转录环介导等温扩增(RT-LAMP)方法快速检测H1N1流感病毒。该装置可实现特异性磁珠结合分离H1N1病毒、病毒裂解、等温核酸扩增、病毒比色检测。检测限仅为3×10-4血凝单元/反应,对于临床应用具有足够的灵敏度。通过新型聚二甲基硅氧烷表面处理与疏水软阀配合,整个过程在毛细管力的作用下仅需40分钟即可完成。这是首次证明一种简单的、自驱动的无源微流控芯片能够在单个芯片上进行样品预处理、RT-LAMP和H1N1病毒检测。
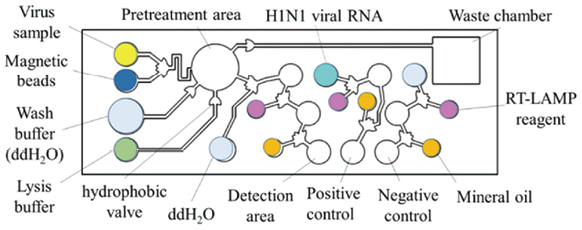
图6. 检测H1N1病毒微流控芯片组成部分示意图
三、总结与展望
全球化的今天,如2019冠状病毒病(COVID-19)疫情和埃博拉疫情等公共安全危机越来越威胁到人们的安全。而随着抗生素的普及,细菌和真菌对于现有抗菌药物的耐受性提高等现象也不容忽视。结合了微流控技术的分子检测手段在应对病原体感染方面可以大大降低对于专业技术人员的需求,使得病原菌的检测过程得到简化,检测成本大幅降低,同时避免了检测过程中环境微生物的感染以及对检测人员自身的威胁。因此,该技术不仅适用于医院,而且适用于地处偏远和资源有限的地区,能够为传染病防控提供有力的工具。
尽管如此,目前商业化的病原微生物微流控检测方案都有着一定的局限性:检测的灵敏度有限,对于痰液等病原菌含量较高的呼吸道样本有着良好的检测效果,但是对于取样困难、菌量浓度低(如血流感染)的样本还需要借助于血培养等传统的检测方法;分子检测都会预设检测靶标,导致现有的商业化的检测产品检测靶标数量有限,不能检测靶标以外的病原菌及未知病原菌;最后,微流控产品检测的通量较小,需要在未来的发展过程解决。
在本篇文章中,我们综述了微流控技术在病原菌分子检测中的应用,对市面上现有的三种常见产品及文献中提及的部分微流控检测原理进行了详细的阐述,以期对微流控技术在病原菌分子检测方面的应用和发展提供参考。
参考文献
Wei C, Zhong J, Hu T, Zhao X. Simultaneous detection of Escherichia coli O157:H7, Staphylococcus aureus and Salmonella by multiplex PCR in milk. 3 Biotech. 2018 Jan; 8(1): 76.
Zhao, X.; Zhao, F.; Wang, J.; Zhong, N. Biofilm formation and control strategies of foodborne pathogens: Food safety perspectives. RSC Adv. 2017, 7, 36670-36683.
Zhong J , Zhao X . Isothermal Amplification Technologies for the Detection of Foodborne Pathogens[J]. Food Analytical Methods, 2018, 11(22): 1-18.
Holmes D, Gawad S. The application of microfluidics in biology. Methods Mol Biol. 2010; 583: 55-80.
Yujie L I , Huo Y , Di L I , et al. Technology,application and development of microfluidics[J]. Journal of Hebei University of Science and Technology, 2014.
Wen N, Zhao Z, Fan B, Chen D, Men D, Wang J, Chen J. Development of Droplet Microfluidics Enabling High-Throughput Single-Cell Analysis. Molecules. 2016 Jul 5; 21(7): 881.
Ghaemmaghami AM, Hancock MJ, Harrington H, Kaji H, Khademhosseini A. Biomimetic tissues on a chip for drug discovery. Drug Discov Today. 2012 Feb; 17(3-4): 173-81.
Marre S, Jensen KF. Synthesis of micro and nanostructures in microfluidic systems. Chem Soc Rev. 2010 Mar; 39(3):1183-202.
Mu X, Zheng W, Sun J, Zhang W, Jiang X. Microfluidics for manipulating cells. Small. 2013 Jan 14; 9(1): 9-21.
Zhao, Dong, Liu, et al. Large lateral shift in complex dielectric multilayers with nearly parity-time symmetry[J]. OPTICAL AND QUANTUM ELECTRONICS, 2018, 50(8).
Trinh TND, Lee NY. A rapid and eco-friendly isothermal amplification microdevice for multiplex detection of foodborne pathogens. Lab Chip. 2018 Aug 7; 18(16): 2369-2377.
Trinh TND, Lee NY. A foldable isothermal amplification microdevice for fuchsin-based colorimetric detection of multiple foodborne pathogens. Lab Chip. 2019 Apr 9; 19(8): 1397-1405.
Trinh KTL, Trinh TND, Lee NY. Fully integrated and slidable paper-embedded plastic microdevice for point-of-care testing of multiple foodborne pathogens. BiosensBioelectron. 2019 Jun 15; 135: 120-128.
Li Z, Bai Y, You M, Hu J, Yao C, Cao L, Xu F. Fully integrated microfluidic devices for qualitative, quantitative and digital nucleic acids testing at point of care. BiosensBioelectron. 2021 Apr 1; 177: 112952.
Poritz MA, Blaschke AJ, Byington CL, Meyers L, Nilsson K, Jones DE, Thatcher SA, Robbins T, Lingenfelter B, Amiott E, Herbener A, Daly J, Dobrowolski SF, Teng DH, Ririe KM. FilmArray, an automated nested multiplex PCR system for multi-pathogen detection: development and application to respiratory tract infection. PLoS One. 2011; 6(10): e26047.
Sparks R, Balgahom R, Janto C, Polkinghorne A, Branley J. evaluation of the BioFire Blood Culture Identification 2 panel and impact on patient management and antimicrobial stewardship. Pathology. 2021 Jun 10: S0031-3025(21)00133-1.
Raja S, Ching J, Xi L, Hughes SJ, Chang R, Wong W, McMillan W, Gooding WE, McCarty KS Jr, Chestney M, Luketich JD, Godfrey TE. Technology for automated, rapid, and quantitative PCR or reverse transcription-PCR clinical testing. Clin Chem. 2005 May; 51(5): 882-90.
Taylor MT, Belgrader P, Furman BJ, Pourahmadi F, Kovacs GT, Northrup MA. Lysing bacterial spores by sonication through a flexible interface in a microfluidic system. Anal Chem. 2001 Feb 1; 73(3): 492-6.
Petersen, K. and McMillan, W. (2002) IVD systems in bioterrorism response. IVD Technology May, 35.
Kost CB, Rogers B, Oberste MS, Robinson C, Eaves BL, Leos K, Danielson S, Satya M, Weir F, Nolte FS. Multicenter beta trial of the GeneXpert enterovirus assay. J Clin Microbiol. 2007 Apr; 45(4): 1081-6.
Xing W, Wang J, Zhao C, Wang H, Bai L, Pan L, Li H, Wang H, Zhang Z, Lu Y, Chen X, Shan S, Wang D, Pan Y, Weng D, Zhou X, Huang R, He J, Jin R, Li W, Shang H, Zhong N, Cheng J. A Highly Automated Mobile Laboratory for On-site Molecular Diagnostics in the COVID-19 Pandemic. Clin Chem. 2021 Mar 31; 67(4): 672-683.
Schulz M, Calabrese S, Hausladen F, Wurm H, Drossart D, Stock K, Sobieraj AM, Eichenseher F, Loessner MJ, Schmelcher M, Gerhardts A, Goetz U, Handel M, Serr A, Haecker G, Li J, Specht M, Koch P, Meyer M, Tepper P, Rother R, Jehle M, Wadle S, Zengerle R, von Stetten F, Paust N, Borst N. Point-of-care testing system for digital single cell detection of MRSA directly from nasal swabs. Lab Chip. 2020 Jul 14; 20(14): 2549-2561.
Abafogi AT, Kim J, Lee J, Mohammed MO, van Noort D, Park S. 3D-Printed Modular Microfluidic Device Enabling Preconcentrating Bacteria and Purifying Bacterial DNA in Blood for Improving the Sensitivity of Molecular Diagnostics. Sensors (basel). 2020 Feb 21; 20(4): 1202.
Yu-Dong Ma, Yi-Sin Chen, Gwo-Bin Lee, An integrated self-driven microfluidic device for rapid detection of the influenza A (H1N1) virus by reverse transcription loop-mediated isothermal amplification, Sensors and Actuators B: Chemical, Volume 296, 2019, 126647, ISSN 0925-4005.





