免疫热点问与答
北京大学人民医院张正教授:D_二聚体的测定在我国内有两种报告方式:一为DDU模式,另一为FEU模式。任何一个具体报告方式都要按仪器使用说明书报告。FEU模式国内应用尚不是主流,但是为发展方向,其报告使用参考范围。
问题中所指测值为0,会发生在DDU模式仪器上(如:ACL-TOP),以ACL-TOP为例,该仪器具体检测线性范围为150-3500之间,21-150之间为非线性范围,0-21之间测值可信度不够,因此21以下报告时以21报告。每款机器还有差异,故具体要详细阅读说明书。另外,测值报告与医学决定水平还有一定不同,FDA已认证,就ACL-TOP而言,医学决定水平为230,测值小于230时对临床排除静脉血栓有较高价值。
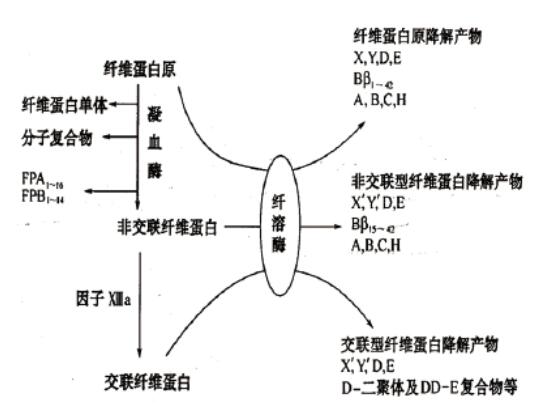
广州南方医院检验科裘宇容主任:D-二聚体(D-Dimer)是凝血系统激活后,形成的交朕纤维蛋白(Fb)在纤溶酶的作用下水解产生的特异性降解产物,其水平的升高反映高凝状态和继发纤溶亢进,D-二聚体的含量变化可以作为体内高凝状态和纤溶亢进的标志性物质。D-二聚体检测以简便、快捷、经济、安全、无创伤性为特点,其高度的敏感性和阴性预测值,在深静脉血栓和肺栓塞的排除,DIC 的诊断及溶栓治疗监测等方面具有良好的应用价值。
1972年,Gaffney首先提出D-dimer检测,可作为监测凝血性疾病的“有用的工具”。1983年,Rylatt等首先报道了用单克隆抗体(DD-3B6/22) 检测D-dimer(乳胶凝集法)。当时被誉为“金标准”。上世纪90年代,ELISA分析法、乳胶增强型免疫分析法等。90年代末到本世纪初,免疫比浊法在凝血仪上实现了自动化检测。目前有超过30种检测方法和20多种单抗被使用。各品牌试剂中的抗D-二聚体单克隆抗体是针对不同分子量的纤维蛋白降解片段制备的,不同试剂间差异非常显著。
D-二聚体的由于检测方法和生产厂家的不同,其检测的不精密度、携带污染率、线性范围、临床可报告范围各不相同。各实验室可结合试剂厂家说明书要求进行验证。不同品牌试剂,各指标性能有所差异。对于检测结果低于或高于线性范围或可报告范围的,如验证线性范围为0.18-9.70mg/L FEU,验证的最大稀释倍数为1:8,则临床可报告范围为:0.18-77.6 mg/L FEU。对于检测结果小于0.18的应当报告“<0.18 mg/L FEU”,大于77.6的检测结果应当报告“>77.6mg/L FEU”。
不同试剂,针对的D-二聚体抗原片段不同。因此,理论上,D-二聚体在检测过程中有可能出现结果为0的情况。实践中,也有极少数D-二聚体检测结果为0的情况。是否可以报告,各实验室需在质控在控的基础上,视实验室验室验证的可报告范围而定,同时样品等因素的干扰。不过,D-二聚体检测最主要的临床价值是用于排除静脉血栓性疾病(如 DVT和 PE 等),D-二聚体在低于CUT-OFF值范围内的波动,其临床意义不大。
丙肝抗体胶体金方法检测的假阳性如何避免?
张正教授:丙肝抗体临床检验使用胶体金方法判为假阴性应十分慎重。标准合格的抗—HCV试剂条本身应有:阳性质控带,检测时只有质控带出现后方能判定标本结果。
从检验方面避免假阴性首先要求试剂合格,买后应有验证,验证合格试剂贮存于要求条件下,使用时在效期内。另外标本应合格(无溶血、乳糜等,够量),运送条件无误。
特别需要注意,在慢性丙肝患者中,病程有间断发作的特点,慢性患者某次检测抗体由阳转阴应复测,并结合其他结果(HCV-RNA,转氨酶等)判断患者是否进入静止期,在此期内抗—HCV也会有一定程度下降。复测仍阴性应提醒临床注意患者是否出现其他致免疫功能低下疾病(如肿瘤、肾功能不全、SLE等免疫病)或使用免疫抑制剂,使患者产生抗体能力受影响而抗—HCV出现阴性,此类患者不属假阴性。
裘宇容主任:
1.试剂盒的选择:目前实验室用的丙肝抗体检测试剂盒都是第三代试剂,其包被的抗原片段是C+NS3+NS4+NS5或C+NS3+NS4,有研究显示NS5对于灵敏度提升有限但是会降低检测特异性,因此目前有些试剂盒不加NS5抗原。Core抗原中的N端保守区域易产生交叉反应,适度减少Core抗原的配比,可以减低非特异反应,降低假阳性率。因此试剂盒中包被抗原的比例的不同试剂盒的灵敏度和特异性也会不一致。因此选择一家好的试剂盒是非常重要的。
2.标本避免溶血。
3.标本完全凝固后再进行离心分离血清,避免血清中仍残留部分纤维蛋白原,导致假阳性结果。
4.最好使用一次性玻璃试管或真空管采血管,避免细胞污染。
5.操作时,一定要按试剂盒说明书要求进行操作,尤其是结果判读一定要在试剂盒规定的时间范围内进行。否则时间延长容易出现假阳性结果。
6.筛查试剂,都存在假阳性问题,我们只能尽可能地降低假阳性率。由于胶体金方法的局限性,阳性结果的标本最好用其它方法的试剂(ELISA法或化学发光法)进行复查,两者结果一致,结果发出,并建议做核酸确认试验,若两种方法的结果不一致时,可再选择一种方法学试剂进行复查。




