多变量指标分析用于检测早期卵巢癌的临床性能
前 言
卵巢癌是美国妇科癌症患者死亡的主要原因。美国癌症协会(American Cancer Society)估计:2013年,美国新增22,240例卵巢癌患者,约有14030名女性死于癌症。卵巢癌的死亡人数相当于所有其他妇科癌症的总和。卵巢癌成为美国女性因癌症死的第五大最常见因素。卵巢癌患者的总体存活率<50%。而且,超过三分之二的卵巢癌患者在疾病已经到了晚期疾病(III期或IV期)才被发现,其5年生存存活率约为30%,但是I期癌症患者的存活率为90%。被诊断出患有卵巢癌的女性中,只有不到40%能治愈。
对于这一群体来说,综合手术分期和选择性采用辅助化疗与提高存活率密切相关。妇科肿瘤专家更可能执行正确的手术并给予适应的化疗。因此,准确地转诊到亚专科护理是决定早期卵巢癌患者临床结局的重要因素。为了帮助初级护理提供者和普通妇科医生对附件肿块患者进行分诊,美国妇产科医师大会(ACOG)和妇科肿瘤学协会(SGO)于2011年联合发布了更新的转诊指南。这些指南在预测晚期卵巢癌方面效果不错,而预测早期卵巢疾病的准确性有限,尤其是在绝经前期女性中。相似地,CA 125是最广泛使用的卵巢癌肿瘤标志物,但只在50%的早期肿瘤中表达。所以,帮助附件肿块女性分诊的努力重点就放在了运用新型血清生物标志物的算法上。

多变量指标分析(MIA)(OVA1;Vermillion,Inc.,Austin,TX)是2009年获得美国食品药品监督管理局(FDA)批准的一种多项生物标志物试验,用作帮助预测附件肿块女性患卵巢癌的诊断分类试验。在2011年Ueland等人报道的关键临床效用试验中,发现OVA1结合医生评估比单独医生评估和CA 125的灵敏度和阴性预测值更高。2013年Bristow等人报道的预期应用人群确认试验证实了OVA1结合医生评估的性能稳定。两项研究与前瞻性收集的临床和病理学数据的选择标准完全相同(年龄≥18岁、有盆腔肿块且计划手术的女性)。本研究的目的在于在接受附件肿块手术的女性中,使用上述前瞻性临床试验的1000多名受试者的综合数据集,检验OVA1与临床评估、CA 125-II及修正ACOG指南相比鉴别早期卵巢恶性肿瘤的性能。
材料和方法
计划通过手术程序切除附件肿块的女性受试者被招募到2个前瞻性OVA1研究中,研究在美国44个地点执行。每个研究地点均获得了机构审查委员会批准。所有人口统计学、临床和病理学数据被收集到标准化病例报告表中,包括招募患者和为其手术的医生专业:妇科肿瘤学专科医生或非专科医生。入选标准如下:年龄≥18岁的知情同意女性,影像学检查(计算机断层扫描、超声检查或磁共振成像)显示附件肿块,手术前进行静脉切开术,影像学检查后3个月内执行手术。排除标准包括5年内被诊断为恶性肿瘤(非黑瘤皮肤癌除外),拒绝静脉切开术,未按计划在3个月内执行手术,或病例报告不完整而妨碍分析测试性能。自上一次月经后过了<6个月,女性被归类为绝经前期;自上一次月经后过了12个月,女性被归类为绝经后期。如果上一次月经在6-12个月之间发生或者如果没有给出时间,年龄≤50岁的女性被归类为绝经前期,年龄>50岁的女性被归类为绝经后期。
在Quest Diagnostics Inc(Chantilly,VA)或约翰•霍普金斯医学院病理学系临床化学部(Baltimore,MD)根据OVA1使用说明书执行生物标志物测量。OVA1是经过FDA批准的MIA,包含CA 125-II、转铁蛋白、转甲状腺素蛋白、载脂蛋白A1和β2-微球蛋白检测。使用专有多变量算法通过OvaCalc软件将生物标志物值转换成先前所述的卵巢恶性肿瘤风险评分0.0-10.0。OVA1评分≥5.0(绝经前期)或≥4.4(绝经后期)的受试者被归为高风险。
对于CA 125-II测量,用于OVA1计算的相同值用于个体分析,并根据已发布ACOG转诊标准的临床临界值≥200U/mL(绝经前期)或≥35U/mL(绝经后期),将其归为高风险或低风险,以便与OVA1相比。
经过医生评估,记录恶性肿瘤的临床预测,使用医生的常用方法为常规临床实践建立一个基准。临床评估始终包括体格检查和影像学检查,根据研究入选标准,如使用了CA125,还要包括CA 125。每个研究地点记录了手术后病理学诊断,并根据原发位点(卵巢或非卵巢)、国际妇产科联盟分期及组织学亚型对恶性肿瘤分类。所有病例报告表、病理学报告、诊断和肿瘤分类均独立判定,对OVA1结果不知情。
为了评估既定标准方法在增加OVA1之后的效果,Dearking修正的ACOG标准(需要与妇科肿瘤专家会诊)被用于鉴别满足以下一个及以上标准的受试者:
绝经前期女性
1. CA 125显著升高(>67 U/mL)
2. 腹水
3. 腹部或远端转移的迹象
绝经后期女性
1. CA 125升高(>35U/mL)
2. 结节性或固定盆腔肿块
3. 腹水
4. 腹部或远端转移的迹象
将病例报告表、生物标志物值和OVA1评分发送至Applied Clinical Intelligence进行统计学分析。根据受试者的绝经状态、外科病理学和恶性肿瘤分期,对结果进行统计学分层。计算了单独临床评估、OVA1、CA 125及修正ACOG标准或结合OVA1的临床诊断性能标准(灵敏度、特异性、阳性预测值和阴性预测值)。OVA1使用说明书指明了转诊应在医生评估与OVA1风险分层之间运用Boolean OR函数,以致于满足任一标准都会引起妇科肿瘤专家执行患者评估。相应地,运用OR函数模拟修正ACOG标准增加OVA1的情况,并将综合诊断预测结果与单独使用修正ACOG标准或OVA1预测相比较。在适当的情况下,建立95%置信区间(CI),并使用McNemar方法检测灵敏度或特异性差异的统计学意义。P值< 0.05具有统计学意义。用SAS 9.2(SAS Institute Inc,Cary,NC)执行统计学分析。
结 果
共1110位受试者符合所有招募标准,其中1016位患者可进行OVA1、CA 125-II和临床评估。研究群体的临床特征在表1中进行了概述。总体来说,86位患者(8.5%)具有原发性早期卵巢恶性肿瘤,70.9%的患者(n=61)具有I期卵巢疾病,以及29.1%的患者(n=25)具有II期卵巢疾病。在早期恶性肿瘤的患者中,79位患者(7.8%)存在上皮卵巢癌,7位患者(0.7%)被诊断为非上皮卵巢癌。这些受试者的组织学、分期和等级分布如表2所示。
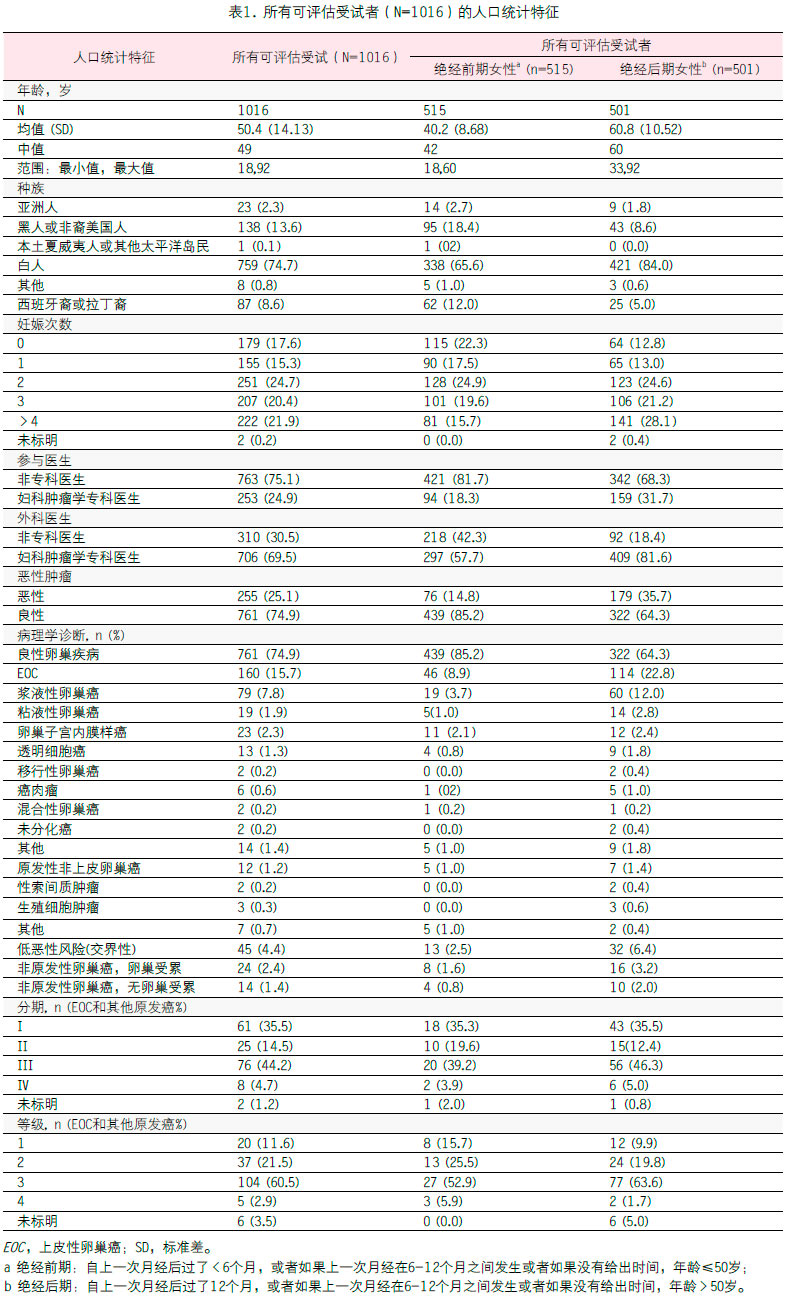
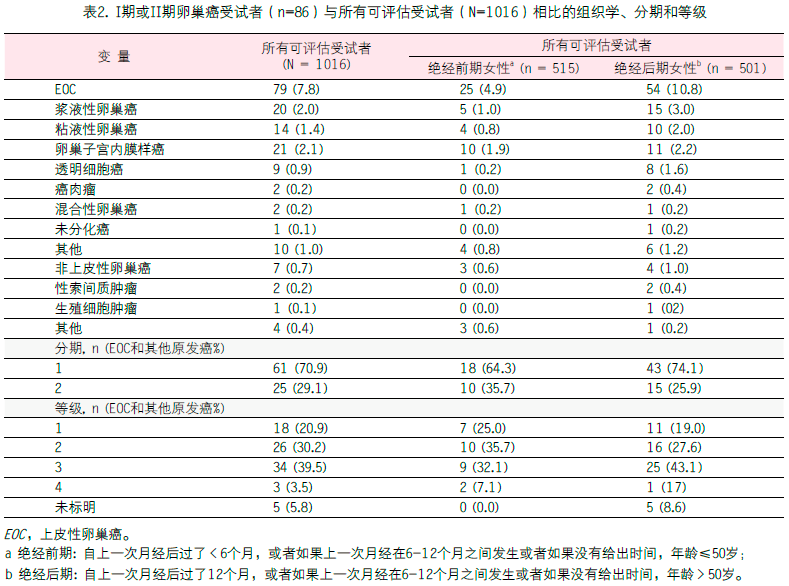
对于处于卵巢恶性肿瘤各个阶段的所有患者,OVA1结合临床评估的灵敏度是95.3%,而单独OVA1的灵敏度是92.2%,单独临床评估的灵敏度是74.5%(表3)。CA 125-II的灵敏度最低(70.6%),修正ACOG指南的灵敏度位于中间水平(80.0%)。OVA1结合临床评估的阴性预测值最高(96.6%),而单独临床评估(91.0%)、修正ACOG指南(91.9%)和CA 125-II(90.1%)的性能相似。与修正ACOG指南和CA 125-II相比,OVA1结合或不结合临床评估,其特异性和阳性预测值都更低。
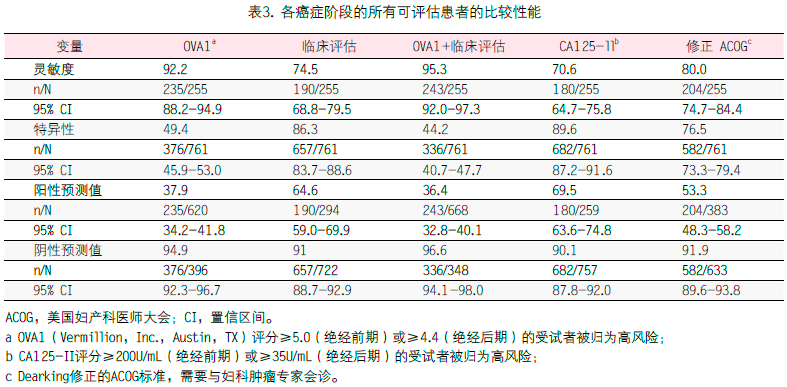
检测早期恶性肿瘤的测试性能分析表明,OVA1结合临床评估的灵敏度保持在95.3%(95%CI,88.6-98.2),在统计学上优于单独临床评估(68.6%;95% CI,58.2-77.4;P<0.0001)、CA 125-II(62.8%;95% CI,52.2-72.3;P<0.0001)及修正ACOG指南(76.7%;95% CI,66.8-84.4;P<0.0001)(表4)。单独OVA1正确鉴别了单独临床评估漏诊的85%(23/27)早期恶性肿瘤,CA 125-II漏诊的78%(25/32)早期恶性肿瘤,及修正ACOG指南漏诊的65%(13/20)早期恶性肿瘤。只有3例早期恶性肿瘤经临床评估正确鉴别但被OVA1漏诊。没有早期恶性肿瘤案例被CA 125-II或修正ACOG指南正确鉴别但被OVA1漏诊。
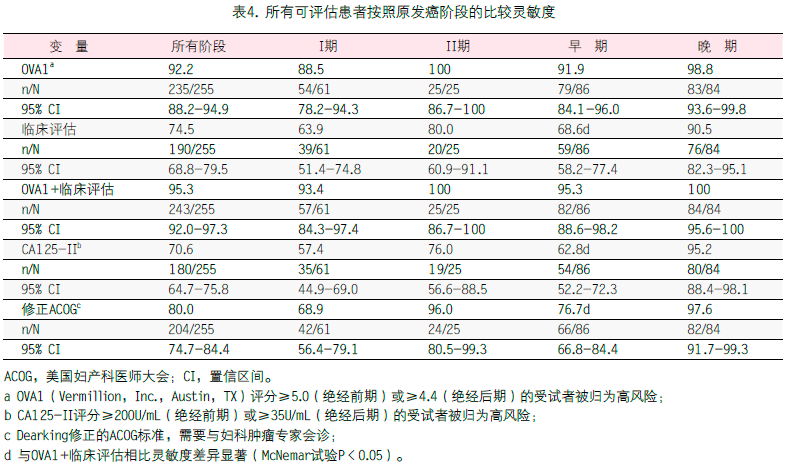
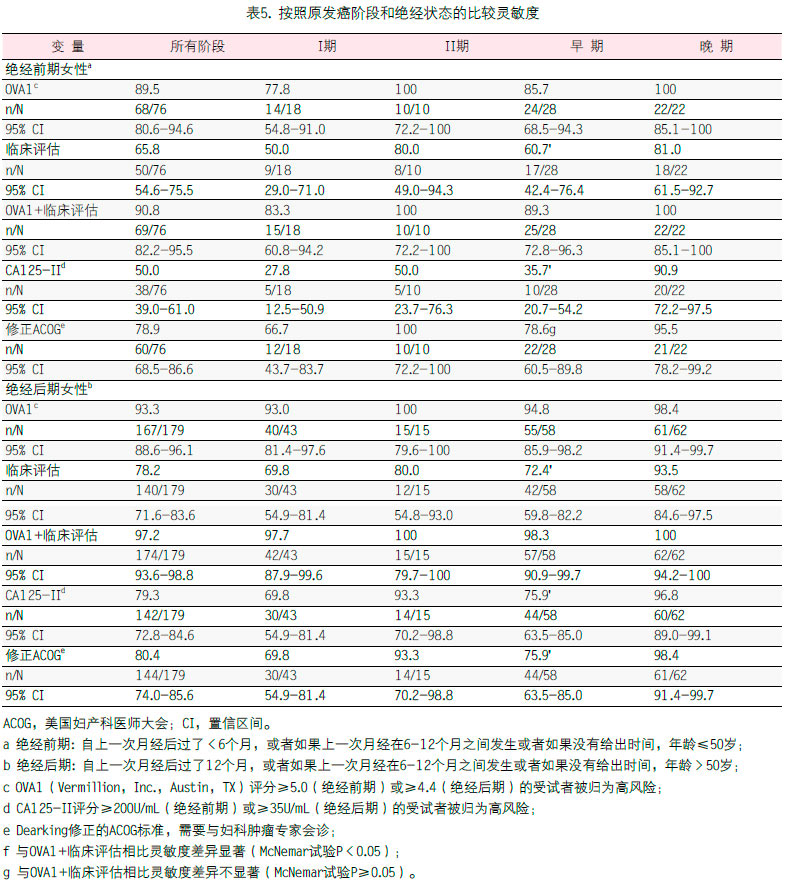
检测按照绝经状态分层的早期疾病的测试性能如表5所示。在515例绝经前期患者中,OVA1结合临床评估(89.3%;95% CI,72.8-96.3)比单独临床评估(60.7%;95% CI,42.4-76.4;P=0.0047和CA 125-II(35.7%;95% CI,20.7-54.2;P=0.0001)更有可能检出早期疾病。作为独立的风险分层试验,OVA1正确预测了单独临床评估漏诊的73%(8/11)恶性肿瘤和CA 125-II漏诊的78%(14/18)恶性肿瘤。只有1例早期恶性肿瘤经临床评估鉴别但被OVA1漏诊。OVA1结合临床评估与修正ACOG指南(78.6%;95% CI,60.5-89.8)之间的灵敏度差异没有统计意义(P=0.0833)。相似地,在绝经后期患者中,与单独临床评估(72.4%;95%CI,59.8-82.2;P=0.0001)、CA 125-II(75.9%;95% CI,63.5-85.0;P=0.0003)及修正ACOG指南(75.9%;95% CI,63.5-85.0;P=0.0003)相比,OVA1结合临床评估正确检出了98.3%(95% CI,90.9-99.7)的早期卵巢癌。
评 论
疾病控制和预防中心、美国卫生研究院、ACOG、SGO和美国综合癌症网络一致认为卵巢癌患者的治疗应包括妇科肿瘤专家的护理。外科肿瘤学协会指出,“为可能的卵巢癌患者做手术的外科医生应同时具备必要的专业技术和对疾病本身管理的透彻理解……并且最好在拥有经验丰富和协调的多学科团队的中心进行。”虽然达成这一共识,但多项基于人群的研究一致表明,不到40%的卵巢癌患者由妇科肿瘤专家提供手术。
虽然社会经济学和地理学因素确实对卵巢癌患者转向妇科肿瘤专家获取治疗不足产生一定影响,但主要的影响因素是手术前区分恶性还是良性附件肿块存在困难。早期疾病在这方面尤其具有挑战性,因为广泛使用的分诊工具,比如修正ACOG指南和独立生物标志物CA 125,均偏向晚期疾病的显著体征。近期一项研究提供了这一挑战的真实证据,研究发现21.4%明显为早期卵巢癌的患者没有进行分期,46.8%的患者没有进行节点采样。在手术前将绝经前期的卵巢癌患者转给适当的外科医生更没有那么简单,因为这些患者发生卵巢恶性肿瘤的概率较低,发生良性肿瘤的概率较高,并且CA 125特异性下降。实际上,在有附件肿块的女性中,年龄在40岁以下的人比40-70岁之间的人更不可能由妇科肿瘤专家护理。
高质量证据表明,接受综合分期的早期卵巢癌患者的复发率降低。尤其是,淋巴结评估与提高生存率具有统计学显著相关性。这是由于在手术时无法鉴别微小转移,因此,无法正确诊断疾病阶段。在妇科肿瘤学团队的经典研究中,对100位临床明显诊断为Ia-IIb期卵巢癌的患者进行系统重新分期,结果表明在考虑综合手术分期结果以后31%的患者处于疾病更晚期。四分之三以上分期升高的患者最终诊断为III期疾病。一项更近期的研究表明,三分之一以上宏观上局限于卵巢肿瘤的患者在最终病理学上都有卵巢外转移。作者发现初级手术标本存在或不存在高风险因素不能充分代替综合分期剖腹术。正如多篇系统综述所示,妇科肿瘤专家比其他外科医生更有可能执行全面分期。初期手术不是由妇科肿瘤专家执行的患者更有可能接受进一步分期手术,更不可能接受适当的以疾病为导向的辅助化疗。
考虑到在患者初期手术时做好卵巢癌准备的重要性,诊断分类试验应争取最大灵敏度。两个大规模、前瞻性的多机构试验表明OVA1结合医生评估检测卵巢癌的灵敏度为96%,在统计学上明显优于单独医生评估、CA 125和修正ACOG指南。结合这些确认试验的群体,当前的研究成效形成了一个扩展数据集,使最难获得的早期疾病患者子集包含有意义数量的受试者。在检测早期疾病中,OVA1比临床评估、CA 125-II及修正ACOG指南的性能更好。OVA1在与临床评估结合使用时,灵敏度增强,综合灵敏度达到95.3%,确定了其可用作这一挑战群体的风险分层手段。在按照绝经状态进一步分层后,OVA1结合临床评估仍保持优越性能。
本研究最重要的优势在于大规模、前瞻性招募的多机构患者群体,使我们将重点放在特别难得的绝经前期、早期疾病患者群体。其他优势包括独立的生物标志物确认,和包含所有卵巢肿瘤类型。研究局限性在于27%的患者在转诊到专科后由妇科肿瘤专家招募。因而,大家认为这个研究群体比预期使用群体的恶性肿瘤发生率高,潜在导致测试的阳性预测值假性升高和测试的阴性预测值假性下降。另一个局限性是无法询问医生评估的过程。这有碍于建立标准化实践算法,但的确是更现实的临床替代方法,因为没有其他转诊算法在美国获得一致认可。需要注意的是,本研究的目的不在于阐述MIA的成本效益或对转诊模式的影响。
尽管存在这些局限性,本研究仍确定与单独临床评估、CA 125-II及修正ACOG指南相比,OVA1结合临床评估可作为早期卵巢恶性肿瘤的灵敏风险分层手段。作为独立的分诊工具,OVA1正确鉴别了单独临床评估漏诊的85%早期恶性肿瘤,CA 125-II漏诊的78%早期恶性肿瘤,及修正ACOG指南漏诊的65%早期恶性肿瘤。对于检测按照绝经状态分层后的I期和II期卵巢癌,OVA1结合临床评估仍保持优越性能。
■ 摘自《Research》,版权归其所有,仅供内部参考。
编译:王小茜、张凯
审校:姜妤、方研、贲文锐




