POCT实施指南
本指南是2019年由澳大拉西亚临床生物化学家协会(AACB)最新制定的,AACB是推动澳大拉西亚地区临床生物化学进步的主要专业协会。本刊节选以下章节供大家参考,希望大家与前一篇国内专家共识对照学习。
目 录 表
POCT要求
组织机构
分析仪选择
人员培训和能力
质量控制
室间质评
安全性和废物处置
误差来源
信息技术
法律规定
帮助/支持
— POCT要求 —
本节概述了医疗保健中心引进和实施POCT所需的步骤。澳大利亚POCT从业者网络(APPN)提供了有用的信息,包括用一张流程图(图1)来说明如何实施POCT、如何选择分析仪和清单来帮助确定临床POCT需求。
在决定开展POCT之前,建议所有利益相关者都参与到规划过程中,包括医务人员和检测执行人。组建此利益相关者小组的目的在于选择适合检测目的的设备。
在引进POCT时需要考虑的步骤包括:
需要满足的临床需求
确定医疗保健中心内起带头作用和管理POCT服务的负责人
如果没有POCT,备用/备选方法是什么?
分析成本和效益
检索文献以评价相关仪器是否符合临床目的
评估医保报销资格
技术支持的可获得性
以电子方式获取结果的能力(接口)
采购检测设备和耗材
制定用户手册或从供应商获得用户手册
培训所有POCT用户
所有合格用户均将获得资格认证
对质量控制进行监控并记录性能结果
参加室间质评计划或在不可行的情况下参加分样检测计划
记录所有问题和纠正措施
为设备操作员提供继续教育和换发新证
对过程进行审计并采取适当的措施
应当认识到各类医务人员均会执行POCT,其中很多人并不具备评估POCT设备产生的结果质量的专业知识。尤其是,他们可能未经过质量控制和结果解释方面的培训。如其他医疗程序一样,正规培训和能力评估是运行POCT项目的基本组成部分。
某些机构仅允许员工在获得相关认证后才能运行POCT设备。为了成功执行POCT,执行检测的人员需要一个支持网络,包括标准操作规程、培训机会和可以咨询意见的专家。
任何打算引进POCT的医疗保健中心在开始检测之前应当考虑成本问题。POCT的直接成本通常高于实验室检测的成本,但POCT流程下游节省的费用、减少的门诊次数、较短的住院时间以及为患者带来的便利可能抵消了直接成本的增加。
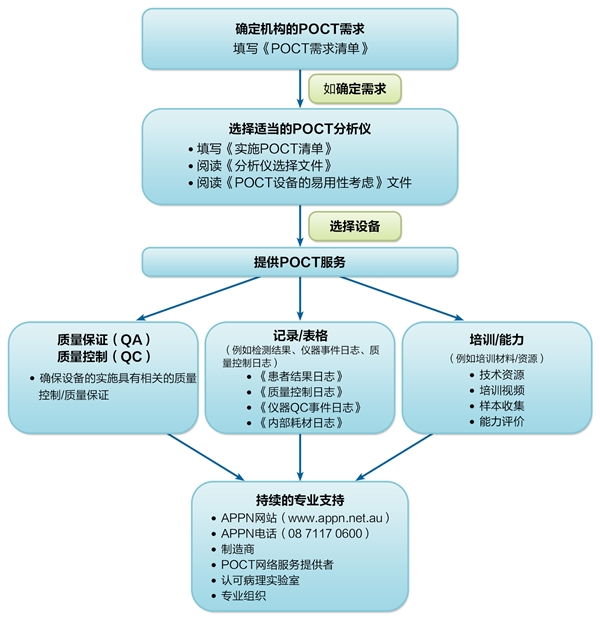
APPN,澳大利亚POCT从业者网络,2010-2019,由Syslinx设计<www.appn.net.au>
图1:如何实施POCT的流程图
— 组织结构 —
本节描述了在质量标准框架内的POCT服务组织结构,适用于采用POCT的任何地方。
一旦引进了POCT,就需要持续协调POCT活动,从实施POCT设备到系统的持续性能。检查质量控制、必要时执行校准、协调和审查室间质评计划、设备维护、与实验室方法进行定期比对以及成为POCT用户的资源等持续进行的任务,都是基本职责。要想成功提供POCT服务,必须有人带头管理POCT。
POCT应该成为医疗保健中心例会上的议程项目,以确保与提供服务有关的所有人员讨论POCT服务的各个方面。
— POCT最低要求 —
以下被认为是任何POCT服务的最低要求:
1、 选择一位合格的指定POCT负责人,这个人是所有利益相关者都接受的,且能够确保符合相关质量标准。
2、 选择的设备应当有评价报告。
3、 将执行的POCT检测应当符合预期临床需求。
4、 所有执行POCT检测的个体均应经过适当的培训并获得资格认证。
5、 POCT的各个方面均应有书面政策。包括组织结构、人员事宜、方法/仪器选择、检测程序、安全性/废物处置、质量控制、室间质评、维护、结果报告和患者教育。
6、 POCT设备的用户应当遵循制造商的建议计划和方案。
7、 应对POCT的各个方面进行完整、准确和及时的记录。
8、 每项POCT检测均应有书面检测程序。
9、 应当有常规监控仪器性能包括质量的过程。
10、必须定义并与相关专业人员及时沟通医学警告值/临界值/危急值。应维持完整、准确和及时的患者结果记录。可能的情况下,应采取电子传输POCT结果。
11、应确定备用和/或确证检测程序。
所有POCT设备应通过一个质量体系来管理以确保结果的质量,并且如果可能的话,还应包含在认可过程中。
— 分析仪选择 —
本节描述了医疗保健中心在选择POCT设备时需要考虑的事项。
很多不同的制造商提供各种各样的POCT设备,涵盖病理学各个领域的大量检测菜单。范围从相对简单的血糖仪,到类似于实验室分析仪的高度复杂设备。对于新手来说,这可能是一个潜在的雷区,包括数量和种类繁多的仪器造成困扰、不正确的决策和不恰当的应用。因而导致浪费金钱和最终用户错失机会。
为了避免这种情况,以下提供了一些简单的规则和建议来帮助选择POCT设备。
— 选择POCT设备时需要考虑的几点 —
以下为可取的POCT设备特性,在选择设备时应予以考虑:
足够的空间-应考虑仪器、耗材和书面工作所需的空间,包括耗材所需的冰箱/冰柜空间
易用性-是否便于用户或操作员使用?
电力/网络要求
维护要求
样本量
耗材的有效期-检测量能否保证在耗材到期之前使用?
检测量-是否足以发挥操作员的持续工作能力?
与当地实验室的结果可比性-这点在实验室结果与POCT结果共同用于患者管理时尤其重要
连通性-结果能否电子传输至患者病历?
精密度和准确度应适合临床需要
便携性-是否需要移动POCT设备,如是,设备是否足够轻便以满足检测需要?
是否有适当的质控物质?
是否有适当的室间质评计划?
资本成本-能否负担得起?
设备保修问题
服务合同-是否享有持续服务和支持,合同条款是什么?
运行成本(包括维护合约、耗材、质控物质(内部QC和外部QA)和连通性成本)是否可行?
公司是否提供培训和/或培训材料?
有没有供应商热线服务电话?
试剂和耗材供应的可靠性
是否有患者、操作员和耗材条形码功能
— POCT利益相关者规划过程 —
本节简要概述了如何规划和选择的过程。
在购买POCT设备之前,建议组建利益相关者“规划小组”。 该小组可能包括:
POCT执行人或最终用户代表(说明需求)
信息技术人员(提供软件界面和功能建议)
机构质量人员(注册、认证要求)
采购/合同管理人员(可选,取决于当地做法)
组建该小组的目的在于选择最能满足检测目的的设备。应按照项目范围,确定一个时间表。可以向制造商描述适合评估的仪器。选择一个产品,请制造商演示,并且可能的话,在购买前提供一台仪器用于评估。
应在成本和时间限制内,选择最佳应用仪器。
— 人员培训和能力 —
本节描述了如何设立和管理POCT培训计划的基本原则。
POCT应仅由医疗专业人员执行:这些人员经过相关初始培训和能力认证,定期接受能力水平评估,参加常规再培训和再认证活动。
这是在任何医疗场所进行POCT的首要原则。
POCT负责人应承担起全面监督和管理POCT活动的责任,确保符合政策和质量标准。
— 培训手册 —
应向参加培训的所有POCT操作员提供纸质版和/或电子版培训手册。
培训手册的内容将由所执行POCT的性质以及开展POCT的组织的需求来决定。最重要的是,其内容应易于未经实验室培训的医疗专业人员理解。
包含如何对患者执行POCT检测以及如何进行质量管理(QC和EQA)检测程序的简单分步说明的层压海报,也可以有效地用作培训包的一部分。
— 培训课程 —
培训应涵盖POCT理论和实践。POCT理论教学应包括以下最低要求:
说明检测的临床背景(疾病过程和病理生理学)
检测的临床实用性和意义
建议执行检测的频率
临床决定限或参考区间
POCT仪器的性能特征及其技术局限性
患者准备和样本收集要求(包括正确的防腐剂或抗凝剂)
试剂制备和储存
如何在设备上执行检测(包括校准)
如何解读、报告POCT结果并采取相应措施(包括超出设备测量范围以及检测预定临床决定限的结果)
质量控制和室间质评的原则和实践
维护和常见的故障排除
职业健康和安全问题,包括感染控制实践、废物管理
符合认可要求(如适用)
培训实践应包括由POCT负责人完整地展示如何使用设备和执行检测、如何运行QC和EQA样本以及如何执行基本维护程序,然后请每个人动手操作。
— POCT能力 —
正规培训完成后,应通过书面评估和实际操作来判定受训者能力。
受训者能力应通过两个方面来评估,一是POCT负责人在场的情况下,成功执行常规POCT检测(不仅仅是分析程序,而是整个检测过程);二是通过一系列简答题进行书面评估,以确保其掌握了重要的理论概念。
合格的受训者应在完成初始培训后获得资格证书。
资格证书应包括证书编号、受训者姓名等详细信息,概述具备的POCT检测和设备技能,具有固定的有效期限(一般为签发之日起一年或两年),并且由培训机构签字盖章和注明日期。
一旦POCT操作员开始常规患者检测,应通过以下各种途径定期审核操作员的能力:
监控质量控制和室间质评测试的性能
参加教育活动比如会议、阅读教育材料和参加大型会议
再培训-尤其是仪器/软件更新时
持续评估,包括书面评估和/或实际观察操作员的操作过程
执行检测的频率
必须保留所有操作员的能力评估记录并每年审核。
参加再培训活动应被视为强制性的。这些活动可以在现场、区域研讨会、年度研讨会上进行,也可以通过视频会议(如果机构在地理位置上比较偏远)进行。如果POCT操作员未通过能力审核(例如,他们的QC/EQA性能一直较差,测试活动水平未达到最低要求,或测试出现很高的分析误差率),那么应在接受再培训之后才能获得重新认证。
POCT负责人应登记并保留获得初始和重新资格认证的所有人的信息。
政府合同或认可机构可能需要保留的资格认证信息。
— 质量控制 —
本节描述了医疗保健中心如何设立和管理POCT质量控制(简称质控)计划的基本原则。
定期监控或检查一个POCT设备的检测(或分析)性能的质量是POCT质量框架的强制规定。质量检查是指“内部质控(QC)”和室间质评(EQA)测试。后者在下一节中阐述。澳大利亚的每个病理实验室均被要求将QC(和EQA)测试作为实验室认证的不可或缺和强制组成部分。重要的是,在实验室外执行POCT时应遵循同等实践标准。
执行QC和EQA测试的基本原则是相似的。QC样本应被当作患者样本一样处理。一般来说,该测试不是检测患者样本,而是由POCT设备制造商提供人为样本进行内部QC测试,或由认证的外部质量保证计划提供者提供人为样本进行外部QA。针对每个POCT检测,质量样本通常具有一个定值或“靶值”,以及围绕该靶值的固定可接受限。无法获得人为样本时,可通过与认可实验室方法进行直接患者比对来代替,但仍应具有固定可接受限。
测试时,完全按照患者样本来处理质控样本。对于大多数类型的质控测试,首先将QC样本转移到一个包含测量所需试剂的测试容器(例如试条、试剂卡、试剂盒、试管或类似容器)中,然后将容器插入POCT设备,待检测完成后结果将显示在设备上。
由制造商生产的QC试剂盒,一般包含对应不同检测浓度的一个、两个或三个QC水平。如果制造商提供两个QC水平,一般一个值或浓度位于“正常”范围,而另一个水平或浓度通常位于“病理学”范围。
可以现场比较QC测试结果与POCT负责人和/或供应商对每个QC水平设定的定值和可接受性能限。大多数POCT设备将以电子方式保存QC结果,但在列出了每个QC水平定值和可接受限的结果表中手动记录QC结果也是一个好主意;POCT协调员可以帮助设计一个适当的结果表。
记录执行QC测试的日期、操作员的姓名(或首字母缩写),以及至少包括QC结果是否可接受或相关意见很重要。如果QC测试结果超出了可接受限,那么应由POCT协调员制定出处理这些结果的方案。有一些通用规则概述了处理方案,APPN和AACB或POCT供应商等组织可提供关于这些规则的建议。
完成一项QC测试后,POCT操作员应能够比较测试结果与定值和固定QC限,从而对POCT设备的性能和是否继续患者测试进行及时的内部评估。
QC测试的关键性能指标是不精密度。随着QC样本结果不断累积,可以计算POCT设备上QC测试的不精密度(或重现度)。
不精密度即变异系数[CV%]的计算公式如下:
CV% =(标准差 [SD] / 平均值)x 100%
一般规则是,不精密度越低,设备的性能越好。
根据涵盖大多数实验室检测(包括某些常见POCT检测)的一系列国际认可分析目标,当地实验室或专业POCT供应商可帮助您评估设备的性能是否符合可接受的分析标准。
— QC测试频率 —
AACB POCT立场声明指出:
质控样本必须用每批新试剂进行测试。
最低要求是每个月必须测试一份质控样本。在这种情况下,建议被测样本的值在病理学范围内。
电子QC也可以检查一部分POCT检测过程。
尽管上文概述的程序是大多数POCT设备所共有的,但是还有其他形式的QC可以检查POCT检测过程的选定部分。电子QC,顾名思义,评估POCT设备的电子测量电路。它使用替代材料(例如参考试剂盒、有色滤光片、有色溶液或条形码)生成电信号,该电信号通常在传感器感受到患者样本中的分析物时产生。因此,电子QC仅测试整个检测过程中的“读取”步骤。它不测试分析过程。
— 室间质评 —
本节描述了执行POCT室间质评(EQA)的基本原则。EQA也被称为能力验证。
— 原 则 —
EQA是保证检测过程质量的基本组成部分。它是一个系统,通过比较不同方法和不同检测站点的性能,主要是同行比较来客观评估获得的结果。
参与EQA的所有POCT用户在其POCT设备上分析完全相同的未知标本,并将结果发送给EQA提供者。EQA提供者向医疗保健中心发送一份报告,详述其性能。
EQA是对内部质控的补充,有助于向POCT操作员和患者保证测试结果有效。
— EQA提供者 —
应由第三方向POCT供应商提供EQA以确保结果的客观性。EQA提供者应通过ISO/IEC 17043认可。
如果无法参与EQA计划,则POCT用户应参加分样计划,即同时使用POCT和正常实验室方法分析同一份样本。然后将这两种方法的结果与预设的可接受限进行比较,以评估性能。
— 如何执行 —
医疗保健中心参加所开展检测的EQA计划。QAP将定期发送标本给POCT操作员进行测试。按照时间表(到期日)进行测试,并将结果返回EQA提供者。然后将每个返回结果与其他参与者的结果相比较。EQA提供者会设定一个结果“靶值”。其次,医疗保健中心将收到一份报告,概述其结果与“参考答案”和/或同行的比较情况。
— 审核EQA性能 —
由POCT负责人审核这份报告,报告显示了POCT仪器的分析性能是否为临床可接受,及其是否可与该仪器的其他用户的性能相当。该报告还可用于长期监控分析性能,以便及早发现问题。
如需要,必须采取纠正措施。包括停止使用POCT分析仪或对操作员进行再培训。所有纠正措施必须记录下来。
— 安全性和废物处置 —
本节描述了在临床环境中实施POCT需要考虑的安全性问题。
所有实验室、医院病房和全科医师(GP)办公室遵循相同的安全性和废物处置标准很重要。
以下程序仅供参考,不能代替您所在工作场所已经过认证认可的既定标准。
— 安全性 —
所有POCT程序均应在不损害患者或设备操作员的安全性或健康的情况下执行:
应按照制造商的说明操作设备;
在首次使用仪器之前应检查所有电气元件的安全性;
应在规定时间或出现任何过量血液或体液污染后立即按照制造商的说明清理设备,以及按照制造商或当地法规的建议定期清理设备。
— 卫 生 —
防止可能的感染在POCT站点传播很重要,通常认为洗手是实现这一目标的最重要措施。
应按以下方式或在以下情况下洗手:
使用普通肥皂或含酒精的洗手液
在接触患者之前
在接触患者之后
在接触体液之后,不管有没有戴手套
在脱掉手套之后
手套应作为采集POCT样本时手部卫生的辅助手段,因为手部可能会被血液或体液污染。每接触一名患者应更换手套并洗手。
— 去 污 —
仪器工作区域应当每天清理,并立即清理溢出的所有血液和体液。
应使用热肥皂水擦洗工作区域,以保持清洁。这将去除而不是杀死微生物,因此对整个区域进行强力擦洗非常重要。
在血液或体液污染的情况下,必须对工作区域进行去污。需要使用产生氯的漂白剂(家用漂白剂)执行更严格的程序。
使用1:10的漂白剂与水溶液
戴手套
使用吸水毛巾和肥皂水清除大部分染物
上漂白剂
搁置10分钟
冲洗并干燥
— 尖锐物和临床废物 —
尖锐物是指能够划破或穿透皮肤的物体或设备,例如注射器针头、碎玻璃或硬塑料物品和自动刺血针。所有的尖锐物都有可能通过割伤或刺伤而造成伤害。另外,许多尖锐物被血液或体液污染,如果它们刺入皮肤,则有感染或患病的危险。因此,在使用和处置尖锐物时必须遵循安全程序。应使用符合相关标准的大小合适、黄色、耐刺穿(防渗漏)的尖锐物容器,例如澳大利亚标准AS4031关于收集医疗区所用的尖锐医疗物品的非重复使用容器要求,或澳大利亚/新西兰标准AS/NZS 4261。处置容器应位于靠近尖锐物产生的地方,并应遵循感染控制指南。所有的尖锐物容器必须至少每周检查一次,并在达到标记的最高线时更换。必须将所有完全密封的容器从场所中移出,并由经批准的污染废物承包商处置。
— 废物处置 —
参与POCT的每个人都有责任确保工作场所产生的所有废物得到安全和正确的处置。法律严格禁止将废物排向下水道、地方当局的垃圾收集站或大气的不当和不负责任处置。应按照相关指南保存和处置所有危险材料,例如NHMRC国家卫生保健行业废物管理指南。样本采集针和试剂(杯/试条)应视为危险的“尖锐物”,并放到经批准的尖锐物容器中。每个设备操作员都应对他们使用的“尖锐物”负责。
其他废物,例如被血液或体液污染的组织或拭子,应放在传染性材料塑料袋(黄色)中进行焚化。
在处理废物时应考虑使用适当的个人防护设备,参考相关的《材料安全数据表》(MSDS)。
— 误差来源 —
本节描述了可影响POCT结果质量的潜在误差来源。
POCT误差可能是设备特有的或由于分析前或分析后误差所致。
在选择POCT设备后,确保高质量POCT的第一步是制定易于非实验室人员遵守的书面程序。同样重要的是,该书面程序应同时反映制造商和各个POCT站点的建议。
误差来源包括未遵循制造商的说明,使用过期试剂,结果记录不充分,以及未进行QC和EQA。
可通过以下方式降低误差发生的概率:
正确识别患者和/或检测人员
正确的样本采集
检查试剂没有过期
按照制造商的说明进行分析
在适当的时间执行质控(QC)和外部QA
审核QC/EQA结果
合理应对失控情况
定期评价操作员的持续能力
遵守所有安全性要求
通过选择包含适当安全措施的检测设备,可以很容易地避免或排除很多此类误差来源。
— 标本采集 —
适用于实验室标本的注意事项同样适用于POCT标本。此外,毛细管或指尖血样的质量对结果具有决定性的影响,因此关于此类标本采集技术的培训至关重要。
— 毛细管血样采集 —
样本采集的潜在误差来源包括:
较浅的皮肤穿刺导致血流缓慢
未按照制造商的说明使用正确的血滴
挤压太用力
沿着皮肤吸取从穿刺部位流出的血液
从脚后跟或脚趾“挤血”
穿刺位置不当
采集偏离穿刺部位的血液
样本采集装置的填充不正确或不足,例如空气进入或填充不足
采集血滴的时间太长
— 动脉血样采集 —
动脉血样采集在技术上是困难的,也是对分析前误差最敏感的。动脉血采集或处理不当会导致错误的pH和血气结果。
动脉血样采集的潜在误差来源包括:
样本中存在气泡
室内空气污染
在分析之前没有混合样本
溶血
在分析之前未除去最初的血滴
使用错误类型或数量的抗凝剂
分析延迟
— 信息技术 —
信息技术(IT)在医学的各个领域中都变得越来越重要,对于POCT也是一样。
— 数据收集和报告结果 —
研究表明实验室医学的很大一部分误差发生在检测过程的分析前和分析后阶段。
POCT检测结果至少应记录下来,而更恰当的做法是将其记录到患者病历中。就其性质而言,POCT检测结果应可以作为及时采取措施的依据,但是通常其结果会被丢弃,而不是保留在患者档案中。
关于连通性,有一个国际标准,且很多机构只会引进能够与临床软件包或医院信息系统(HIS)或一般信息系统进行网络连接的POCT设备。
— POCT设备的基本IT功能特征 —
双向数据通信—从设备到软件以及从软件到设备的通信
使用现有基础设施—利用现有通讯设施来收集/传输结果的仪器将节省重新布线的费用。高度希望所有POCT结果均可通过电子方式传输至适当的数据库。可以将POCT设备的无线连接添加到IT愿望清单,其中可能包括:
数据和访问的安全性对于确保患者机密性至关重要。如果要将结果传输到外部用户,则应考虑对结果进行内联网加密。
设备应即插即用-即能够连接到任何数据库/LIS/HIS系统。
设备应使用常见的程序坞(docks)、端口和接线进行通信。
可以扫描患者条形码(如有),以输入患者信息。
能够定期监控QC数据以评估系统性能。
— 法律规定 —
本节描述了当前澳大利亚对病理学检测的法律规定。
澳大利亚的病理学是根据《健康保险法》(1973)进行管理的,根据该法,如果实验室的服务符合医疗保险福利条件,则实验室必须获得认可。国家病理学认可咨询委员会(NPAAC)负责制定和维护病理实验室认可的标准和指南。
NPAAC的作用包括:
制定病理实验室的认可政策;
在澳大利亚范围内引进和保持统一的病理实验室实践标准;
在提供病理学服务方面采取协调一致的立法和行政行为;
发起、促进和协调有关病理实验室实践的教育计划。
NPAAC标准和指南获取链接:https://www1.health.gov.au/internet/main/publishing.nsf/Content/health-npaac-index.htm
目前,澳大利亚有两套POCT标准或指南草案正在最终定稿。第一套由NPAAC起草,获取链接为:https://www1.health.gov.au/internet/main/publishing.nsf/Content/35DE5FC4786CBB33CA257EEB007
C7BF2/$File/Guidelines%20POCT%201st%20Ed%202015
这些标准自2015年起可用,目前正在大范围修订中,但预计将在2019年底最终确定。
澳大利亚皇家全科医师学会(RACGP)制定了第二套标准,获取链接为:https://www.racgp.org.au/running-a-practice/practice-standards/standards-for-other-health-care-settings/view-all-health-care-standards/ point-of-care-testing
两套标准均记载了本实施指南中描述的所需质量过程。两者之间没有显著差异,并且有可能最终统一成一组标准,以指导澳大利亚所有POCT的实施。
目前,在一级和二级保健部门中,有相当数量的POCT未经认可而进行,除了对某些检测质量的担忧外,任何一项都不能享受医疗福利计划(MBS)。
少量的GP(<20)已建立了所谓的M级实验室,并通过了基于常规实验室的NATA认证系统的认可,因此这类检测可享受MBS。
— 帮助/支持 —
本节描述了开展POCT的医疗保健中心可获得的帮助和支持来源。
POCT结果的质量与正确执行检测的能力有关。许多人认为POCT产品非常简单,能够“防白痴”。毫无疑问,设备变得越来越易于使用,以至于非实验室受训人员也可以使用,但是并没有所谓的防白痴设备。因此,POCT服务的管理人员需要确保向操作员提供维持连续优质服务所需的必要帮助和支持。由于POCT设备的操作员主要为非实验室人员或经过培训的人员,他们的需求有所不同,因此POCT支持至关重要。这里的支持或帮助是指在日常操作中以及引进和运用POCT设备之后用户可获得的信息。
关键利益相关者(可能包括供应商、病理实验室、其他POCT支持网络和最终用户)之间需要建立合作伙伴关系,以在适当的短时间内按要求提供帮助。澳大利亚和国外监管机构现在要求POCT制造商向用户提供简单易用的使用说明以及适当的规范,以确保系统能够按预期用途运行。鼓励供应商积极与最终用户合作以实现不间断的服务,并鼓励用户与APPN联络以获得进一步的独立支持。
在澳大利亚,大多数POCT供应商都建立了呼叫中心,其具体目的是回答POCT用户或代表最终用户的实验室人员提出的任何问题。这样的呼叫中心配备了训练有素的知识丰富的员工,可以回答有关其特定产品的问题的询问。此外,大多数澳大利亚POCT供应商还准备提供关于产品附加培训和正规文件记录等方面的支持。许多澳大利亚POCT供应商通过CD、DVD或专门网站的形式提供了有用的培训材料,涵盖基本仪器使用、维护和基本故障排除等许多领域。
以下方面可能需要帮助/支持:
POCT设备的常规操作
材料管理
质控和质量保证审核
基本故障排除以获得可靠结果
鉴别可能影响结果的分析前和分析后影响
设备不符合规范
了解分析要求和适用性
运行有效POCT项目的最大挑战之一就是确保最终用户能够区分出由于缺少训练、分析和非分析因素引起的问题。这方面的支持可以从几个来源来提供外部建议和指导,比如当地实验室、APPN、RACGP POCT标准、AACB和POCT供应商。这种支持包括:
与相关POCT用户(既包括参与实际检测的人也包括利用结果管理患者的人)保持联系,以确保其需求得到满足
定期反馈特定区域的质量保证性能以及其他沟通项目(例如产品规格变化、材料管理等)
考虑制作“常见问题”文件。大多数POCT制造商都会乐意帮助准备这些材料
定期到访POCT站点以提升形象和与最终用户建立信任
提供适当的联系信息
医疗保健中心花时间与当地实验室建立良好的工作关系很重要,后者可以成为开展POCT的医疗保健中心的重要知识和支持来源,同样实验室也应反过来积极支持开展POCT的医疗保健中心。
患者管理基于POCT和实验室检测结果的结合,所以POCT用户需要与病理实验室合作,以了解两个结果来源可能出现差异,并且在比较这些结果时不会损害患者护理。
POCT用户应充分利用专业机构的资源,比如澳大拉西亚临床生物化学家协会(AACB),通过其POCT工作组致力于开发教育材料并为对POCT感兴趣的医疗保健提供者组织教育会议,而APPN旨在支持POCT用户。
— 延伸阅读 —
ISO/IEC 15189, Medical Laboratories-Particular requirements for quality and competence. Geneva, Switzerland: International Organization for Standardization, 2003.
Price CP, St John A, Hicks JM. Point-of-Care Testing, 3rd edition, Washington DC: AACC Press, 2010
Price, Christopher P., St John, Andrew “Point-of-Care Testing for Managers and Policymakers: From Rapid Testing to Better Outcomes”. 2006 AACC Press ISBN: 1-59425-051-0.
Shephard, Mark, A practical guide to Global Point-of-Care Testing. CSIRO Publishing (ISBN: 9781486305186)
NPAAC Guidelines for Point of Care Testing (First Edition 2015) https://www1.health.gov.au/ internet/main/publishing.nsf/Content/health-npaac-poctguid
RACGP POCT Standards, https://www.racgp.org.au/FSDEDEV/media/documents/Running%20 a%20practice/Practice%20standards/Standards-for-point-of-care-testing.pdf
IFCC, Thinking of Introducing POCT - Things to consider, https://www.ifcc.org/media/253664/20i4%2003%2020%20Thinking%20of%20lntroducing%20POCT%20-%20Things%20to%20Consider.pdf
Clinical and Laboratory Standards Institute. Point-of-Care In Vitro Diagnostic (IVD) Testing; Approved Guideline—Second Edition. Clinical and Laboratory Standards Institute document POCT4-A2 (ISBN 1-56238-618-2).
APPN: https://www.appn.net.au/Data/Sites/i/appn/oiscoping/selectionofanalyser/ analyserselection.pdf
ISO/FDIS 22870. Point-of-care testing (POCT) - Requirements for quality and competence. Geneva: International Organisation for Standardization; 2005.
NCCLS. Quality management for unit-use testing; Approved guideline. NCCLS document EP18-A. Wayne, PA; 2002.
Sawchuk ME. Ensure staff competency with point-of-care testing. Nurs Manage. 2004;35:24.
Wood JF, Burnett D. Chapter 11. Training and certification for point-of-care testing. In: Price CP, St John A, Hicks JM, editors. Point-of-care testing. 2nd ed. Washington DC: AACC Press; 2004. p. 117-25.
Price CP, St John A. Chapter 12. Point-of-care testing. In: Burtis C, Ashwood E, Bruns D, editors. Tietz textbook of clinical chemistry and molecular diagnostics. Washington DC: AACC Press; 2005. p. 299-320.
AACB Point of Care Testing Position Statement, January 2007. Available from: www.aacb.asn. au
APPN https://www.appn.net.au/Data/Sites/i/appn/02implementation/quality/qualitycontrol- qualityassurance.pdf
Bullock David G Chapter 13 Quality Control and Quality Assurance in Point-of-care testing in Price CP, St John A, Hicks JM. Point-of-Care testing, 2nd edition, Washington DC: AACC Press, 2004
AACB Point of Care Testing Position Statement http://www.aacb.asn.au/web/Resources/
Standards for Point of Care Testing in General Practice Quality Management for Unit-Use Testing; Approved Guideline CLSI EP18A V0I22 No.28
Point-of-care Testing - Requirements for quality and competence ISO/FDIS 22870
Garner J, Favero M (1985) ‘Guidelines for Hand Washing and Environmental Control', CDC Guidelines for the Prevention and Control of Nosocomial Infections.
McGill Laboratory Biosafety Manual Second Edition, 1997.www.hoslink.com/sterilisation.htm
NH&MRC Document ‘National Guidelines for Waste Management in the Health Industry' endorsed March 1999. NHMRC Publications Department.
3rd Edition RACGP Sterilisation/disinfection Guidelines for General Practice www.nhmrc.health. gov.au
POCT in General Practice Trial, Training Manual for Point of Care Devices. Australian Government Department of Health and Ageing, 2006.
编译:王小茜
审校:李卫东




