“她”已经成为死亡率最高的妇科恶性肿瘤,CA125+HE4联合检测刻不容缓!
转自“体外诊断网”
由于卵巢癌的临床症状不明显,早期肿瘤在盆腔检查中难以察觉,导致70%-75%的卵巢癌患者在确诊时已属晚期,并已扩散到其他器官,错过了最佳治疗时机,卵巢癌因此被称为“沉默的杀手”。
因此,早期诊断是改善卵巢癌患者预后的关键。
目前,临床上常用的卵巢癌筛查方法包括卵巢癌标志物的血清学检测、经阴超声(TVU)为代表的影像学检查等。其中,血清学肿瘤标志物(主要是CA125、HE4)的检测由于简便、快捷且无侵入性,在临床上得以广泛应用。
CA125是一种来源于胚胎发育期体腔上皮的大分子糖蛋白,其在卵巢癌临床诊断中的应用已达30余年,被认为是目前卵巢癌生物标志物检测的“金标准”。临床上当发现盆腔肿块伴CA125升高时,尤其对于绝经后妇女,应考虑卵巢癌可能。Medeiros等[1]的一项系统性回顾显示,CA125对卵巢癌诊断的灵敏度达80%。
在治疗反应评价、预后评估及复发监测领域,CA125同样具有较高的应用价值[2]:
然而CA125作为卵巢检测“金标准”也并不完美,CA125在I期卵巢癌中阳性率很低,仅30%-50%;此外还存在组织特异性差,受绝经状态影响大等缺点。
HE4即人附睾蛋白4,其最早发现于人的附睾远端上皮细胞中,属于乳清酸性蛋白家族。相比于CA125,后起之秀HE4的指标性能可能更具优势:
当然,HE4也并非全能,在部分已确诊卵巢癌(常见于粘蛋白型卵巢癌或生殖细胞型卵巢癌)的患者中,HE4可能并无水平异常;HE4的检测特异性同样未达到100%,HE4在子宫内膜癌中也有较高阳性率[8]。因此,HE4在卵巢癌筛查诊断中的应用依然存在较大的局限性。
CA125+HE4——联合检测!
CA125与HE4的联合检测,尤其是在两指标基础上算出的风险预测模型(ROMA指数、RMI-II等)或许是更佳的筛查策略。
CA125与HE4的表达相互独立,两者在卵巢癌患者中的分布具有显著差异。例如,Wong等人[9]的研究显示,CA125阴性的卵巢癌患者中仍有32%的HE4阳性;Zheng等人[10]发现卵巢癌患者中,66.67%的CA125阴性样本呈HE4阳性,而同时88.0%的CA125阳性样本为HE4阴性。此外有研究认为[11],在子宫内膜样癌组,CA125 的阳性率显著低于HE4,而在粘液性腺癌组,CA125的阳性率则显著高出HE4。因此,两指标可互为补充,从而增大卵巢癌的检出。
为了充分应用现有卵巢癌检测指标的准确性,大量学者提出了ROMA的概念。

ROMA指数是对HE4和CA125采用特定的公式计算得到的值。公式综合了绝经状态参数,同时降低了单一因素所致的假阳性率,因此其诊断灵敏度和特异性相比任一单项的检测均有显著提高。
Molina等[12]研究显示,HE4诊断卵巢癌的灵敏度、特异度、AUC值分别为79.3%、98.9%、0.936,CA125的对应值分别为82.9%、70.9%、0.853,而ROMA的相应值为90.1%、87.7%、0.952(如下图)。同时Anton等、Kalapotharakos等及Sandri等的研究均得到了类似的结论。国内的研究结果也多与这些研究结果一致。目前ROMA指数已经被 FDA 批准用于女性盆腔包块的诊断和鉴别诊断。
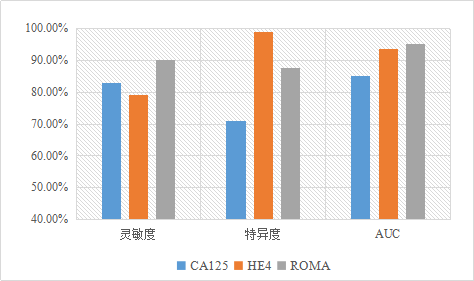
CA125、HE4、ROMA指数的灵敏度、特异度及AUC值比较
ROMA指数通过将盆腔肿块患者分为罹患卵巢癌的高危和低危人群,为临床上卵巢癌的早发现、早诊治以及提高卵巢癌患者的预后提供了新的路径。
尽管多年来卵巢癌筛查的技术方法不断发展,但目前没有一种单一筛查的模式可以作为一种理想的筛查方法。近年来陆续新发现了多种卵巢癌相关血清标志物,如SMRP、Opn、CA725、B7-H4等,但均不能达到临床应用要求。
因此,CA125与HE4的联合检测以及在此基础上ROMA指数的模型计算仍然是目前最简单高效的卵巢癌早期筛查手段之一。


透景生命在高端体外诊断检测领域潜心多年,持续专注于产品的研发创新和品质提升,肿瘤标志物系列产品项目齐全,上述卵巢癌两项标志物CA125及HE4均被覆盖。
其中全自动流式荧光平台(TESMI)上的肿标检测由于具有多重联检优势,一次检测可出7项结果,检测速度高达840 T/h。化学发光平台的肿瘤标志物检测采用吖啶酯发光,打破进口免疫平台封闭性,开发出可兼容雅培ARCHITECT i2000SR的21项指标,溯源至雅培,质量过硬。
产品热线:400-035-8689
![]()



