沈锋教授:勇攀高峰!ASAP模型不断突破中国肝癌风险人群筛查的深度和广度
编者按 我国是肝癌大国,肝癌的发病率和死亡率约占全球一半,及早识别高危人群并对肝癌做出早期诊断是提高患者总体生存率的关键。自1929年维生素K发现以来,研究者们陆续证实因其缺乏产生的血清异常凝血酶原在肝癌诊断上的重要作用。2019年,海军军医大学第三附属医院(上海东方肝胆外科医院)沈锋教授及团队携手国内其他顶尖医院团队,建立并验证了ASAP风险预测模型[1]。此后,ASAP模型不断突破乙肝病因相关肝癌的预测限制,在丙肝相关肝癌预测以及非酒精性脂肪肝相关肝癌预测以及在早期肝癌复发诊断上捷报频传。
01 ASAP模型发展概览
1929年,丹麦生物学家Henrik Dam发现维生素K,并因此获得1943年诺贝尔奖[3]。1968年,Ganro PO和Niléhn JE发现维生素K缺乏会产生血清异常凝血酶原(PIVKA,Protein Induced by Vitamin K Absence or Antagonist,DCP,Des-gamma-carboxy [abnormal] prothrombin,脱-γ-羧基凝血酶原)[4]。1984年,Liebman HA首次发现大多数肝细胞癌(HCC)患者PIVKA-Ⅱ水平升高,可作为HCC诊断的生物标志物[5]。1994年,Suehiro T首次证实PIVKA-Ⅱ可作为HCC预后预测的生物标志物[6]。2011年,中国卫生部颁布的《原发性肝癌诊疗规范(2011年版)》,推荐PIVKA-Ⅱ作为辅助诊断肿瘤标志物之一[7]。2014年,日本肝病学会建议对极高危肝癌人群采用甲胎蛋白(AFP)、PIVKA-Ⅱ、甲胎蛋白异质体(AFP-L3)联合影像检查作为监测方案[8]。2016年,雅培在中国上市PIVKA-II检测标志物。2018年,雅培PIVKA-II检测标志物的中国人群参考区间发布,95分位上限为40.38 mAU/ml。2019年,沈锋教授团队携手中国11家知名三甲医院共同研究并成功开发ASAP肝癌风险评估模型,纳入年龄(Age)、性别(Sex)、血清甲胎蛋白(AFP)水平、血清异常凝血酶原(PIVKA-II)水平四个因素,相关内容发表在检验学顶刊Clinical Chemistry杂志(IF:11.13)[1]。2020年,经沈锋教授、杨田教授许可,ASAP在线运算小程序上线,将这一重大科研成果无偿推广至临床实践中(网址为:http://www.asapcalculate.top/test.html)。2020年,中国《原发性肝癌的分层筛查与监测指南(2020版)》建议联合PIVKA-Ⅱ检测以提高早期肝癌的检出率(B2级推荐)[9]。2022年,中国国家卫健委颁布的《原发性肝癌诊疗规范(2022年版)》推荐PIVKA-II作为肝癌早期诊断标志物用于临床(1A级推荐)[10]。2022年,赫捷院士等发布的《中国人群肝癌筛查指南(2022)》建议PIVKA-II等血清标志物可作为补充筛查技术,但尚不能完全替代超声(US)联合AFP检测(证据质量:中;推荐强度:强)[11]。2022年,上海东方肝胆外科医院沈锋教授、杨田教授团队陆续在SCI期刊发表文章,将ASAP逐步推向全部肝癌风险人群的筛查应用。2023年6月,ASAP肝癌风险评估模型因在中国的优秀实践而荣获“Univants卓越医疗奖”[2],该奖项由全球领先的7家医疗学会组织(IFCC、AACC、EHMC、Modern Healthcare、HIMSS、NAHQ、IHE)共同评选并颁发。
中国是乙肝大国、也是肝癌大国,我国年新发肝癌患者约占全球一半。对我国HCC患者而言,约有84%由乙型肝炎病毒(HBV)感染所导致。我国一般人群HBsAg流行率为6.1%,慢性HBV感染者为8600万例[12]。因此,建立有效的评估模型,监测HBV感染者疾病发生与发展风险,实现疾病早筛、早诊、早治,进而避免HCC的发生非常重要。


1、AFP+PIVKA-II预测丙型肝炎病毒(HCV)相关HCC[13]
HCV感染者进展为HCC的5年风险为7%~14%,早期治疗5年总体生存(OS)率可达50%~80%,若进展到晚期,则不足10%。因此HCV-HCC的早筛、早诊能给患者带来极大获益。目前临床中最常用的生物标志物为AFP,诊断HCV-HCC的灵敏度为41%~65%和特异度为80%~94%。此外,PIVKA-II和AFP-L3也是临床研究中热门的检测方案。沈锋、杨田教授团队开展相关研究,在上述三种检测手段中寻找合适方案,以提升检测的灵敏度。

研究纳入172例HCV对照者和105例HCV-HCC患者。HCV-HCC患者的AFP、AFP-L3和PIVKA-II水平较HCV患者显著升高(P<0.001)。于BCLC和TNM分期定义的早期HCC患者中,在单独检测时,PIVKA-II显示出最佳的预测性能(AUC:PIVKA-II vs. AFP vs. AFP-L3=0.90 vs. 0.80 vs. 0.69,P<0.001);在搭配检测组中,PIVKA-II+AFP显示了最好的预测性能(AUC:PIVKA-II+AFP vs. AFP+AFP-L3 vs. PIVKA-II+AFP-L3=0.93 vs. 0.78 vs. 0.89,P<0.001),与三者组合的预测性能(AUC:AFP+AFP-L3+PIVKA-II 0.93,P=0.277)相比没有差异。因此,在常规AFP检测中加入PIVKA-II检测可能是更适合的检测手段。
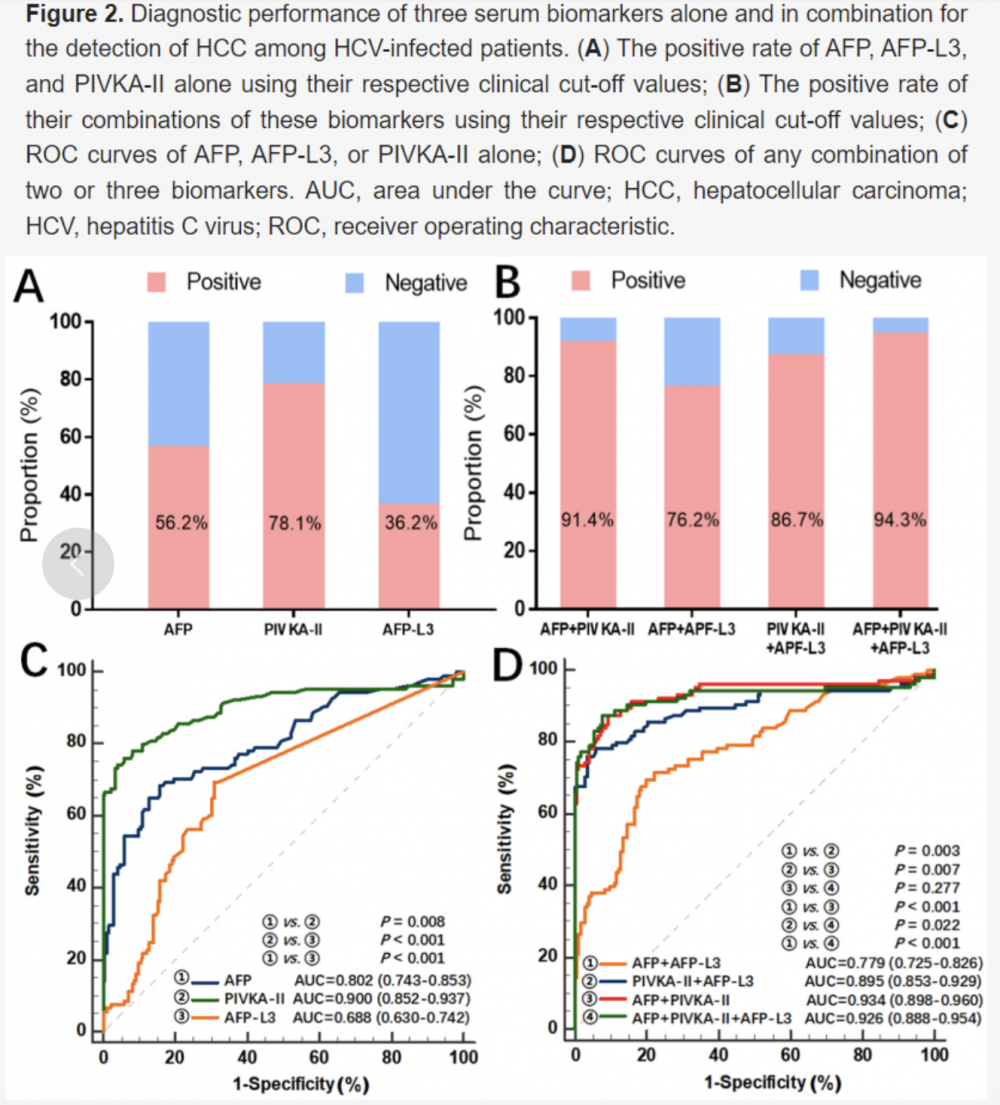
图2. 三种血清生物标志物单独和联合评估HCV感染患者HCC的诊断性能[13]
2、ASAP模型可作为国人HCV-HCC预测手段[14]
在HCV-HCC的预测中,目前较为熟知的GALAD模型——由性别(Gender)、年龄(Age)、甲胎蛋白异质体(AFP-L3)、甲胎蛋白(AFP)和异常凝血酶原(DCP,即PVIKA-II)组成——较ASAP模型多了一个AFP-L3变量。沈锋、杨田教授团队对不含AFP-L3变量的ASAP模型诊断HCV-HCC的具体效能进行了分析。
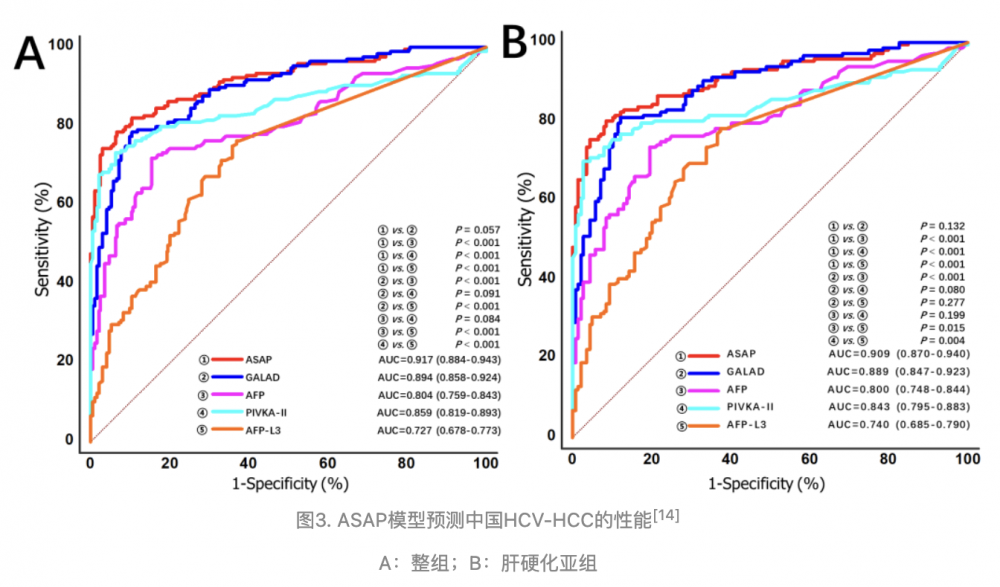
 研究纳入193例HCV对照者和168例HCV-HCC患者。HCV-HCC组与HCV对照组在年龄、性别、Child-Pugh分级和肝硬化、AFP、PIVKA-II和AFP-L3单一生物标志物方面以及ASAP和GALAD的评分方面均存在显著差异。与单一肿瘤标志物相比,ASAP评分和GALAD评分均表现出更好的诊断性能;且在全人群及肝硬化人群中,ASAP评分的诊断效能较GALAD评分存在优势趋势(AUC:0.917 vs. 0.894,P=0.057);进一步的早期HCC亚组、AFP阴性亚组分析中,ASAP评分同样展示了不劣于甚至优于GALAD的诊断效能。因此,ASAP评分可能更加适合于中国慢性丙型肝炎患者进行肝癌筛查和监测,更具有卫生经济效益。
研究纳入193例HCV对照者和168例HCV-HCC患者。HCV-HCC组与HCV对照组在年龄、性别、Child-Pugh分级和肝硬化、AFP、PIVKA-II和AFP-L3单一生物标志物方面以及ASAP和GALAD的评分方面均存在显著差异。与单一肿瘤标志物相比,ASAP评分和GALAD评分均表现出更好的诊断性能;且在全人群及肝硬化人群中,ASAP评分的诊断效能较GALAD评分存在优势趋势(AUC:0.917 vs. 0.894,P=0.057);进一步的早期HCC亚组、AFP阴性亚组分析中,ASAP评分同样展示了不劣于甚至优于GALAD的诊断效能。因此,ASAP评分可能更加适合于中国慢性丙型肝炎患者进行肝癌筛查和监测,更具有卫生经济效益。
 3、AFP+PIVKA-II预测非酒精性脂肪性肝病(NAFLD)相关HCC[15]
3、AFP+PIVKA-II预测非酒精性脂肪性肝病(NAFLD)相关HCC[15]
NAFLD已成为全球HCC的主要病因之一,而当前以超声为主的肝癌监测策略在肝炎、肝硬化以及NAFLD等高危人群中的筛查效能仍不理想。肝癌生物标志物检测在临床的广泛应用为风险检测带来了极大助益。杨田教授团队评估了中国患者使用AFP、PIVKA-II和AFP-L3三种生物标志物单独或联合诊断NAFLD-HCC的诊断性能。

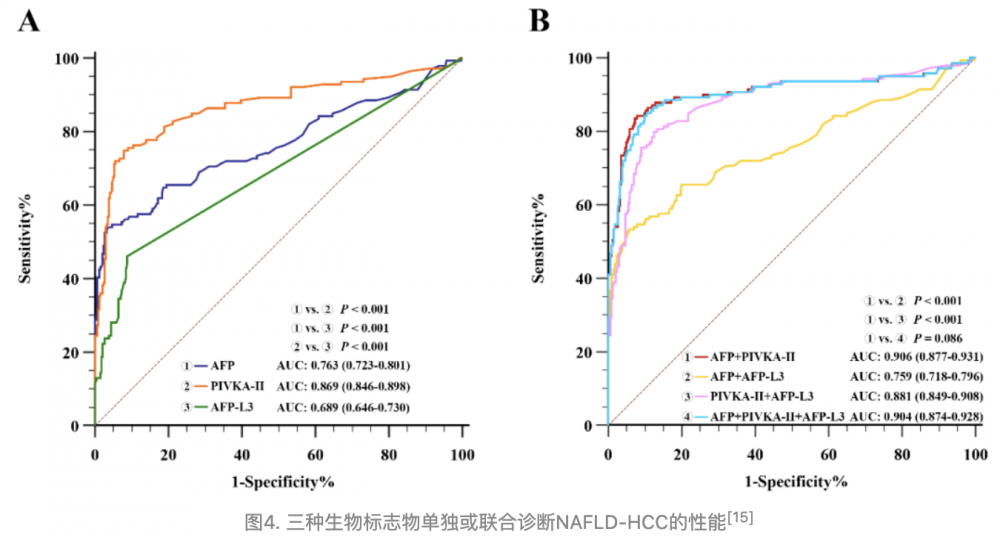
研究纳入345例NAFLD对照者,139例NAFLD-HCC者。研究显示,NAFLD-HCC者较NAFLD患者的AFP、PIVKA-II和AFP-L3的中位数水平更高,P<0.001。在单个生物标志物检测中,PIVKA-II的诊断性能优于AFP(AUC:0.869 vs. 0.763,P<0.001)和AFP-L3(AUC:0.869 vs. 0.689,P<0.001);在组合检测中,AFP+PIVKA-II的表现最佳(AUC:AFP+PIVKA-II vs. AFP+PIVKA-II+AFP-L3 vs. PIVKA-II+AFP-L3 vs. AFP+AFP-L3 0.906 vs. 0.904 vs. 0.881 vs. 0.759),AFP-L3的加入并未提高诊断性能(AUC:0.904,P=0.086)。此外,在非肝硬化亚组和早期肝癌亚组的分析中也得出了类似的结果,从而弥补了中国人群数据的空白,为临床提供了新的检测组合。
此外,沈锋、杨田教授团队还比较了ASAP模型与GALAD模型用于NAFLD-HCC的诊断效能,包括灵敏度、特异度、阳性预测值、阴性预测值、诊断准确率等指标。在2022年第31届亚太肝脏研究学会(APASL)年会上,杨田教授应邀以口头报告的形式对该项研究进行了介绍[16]。
 该研究结果表明:两个联合诊断模型对中国人群NAFLD-HCC(无论所有分期还是早期)的诊断效能均高于任何单一肝癌血清标志物(AFP、AFP-L3、PIVKA-II);更重要的是,ASAP模型对中国人群NAFLD-HCC的诊断效能优于或不劣于GALAD模型。鉴于ASAP模型比GALAD模型还可以少一个AFP-L3的检测,这大大降低了检测成本,且ASAP模型得到的诊断效能与GALAD模型表现同样优异,因此,ASAP模型更加适合于中国NAFLD患者进行肝癌筛查和监测。
该研究结果表明:两个联合诊断模型对中国人群NAFLD-HCC(无论所有分期还是早期)的诊断效能均高于任何单一肝癌血清标志物(AFP、AFP-L3、PIVKA-II);更重要的是,ASAP模型对中国人群NAFLD-HCC的诊断效能优于或不劣于GALAD模型。鉴于ASAP模型比GALAD模型还可以少一个AFP-L3的检测,这大大降低了检测成本,且ASAP模型得到的诊断效能与GALAD模型表现同样优异,因此,ASAP模型更加适合于中国NAFLD患者进行肝癌筛查和监测。
4、PIVKA-II和ASAP预测未经治疗CHB患者1年内HCC风险[17]

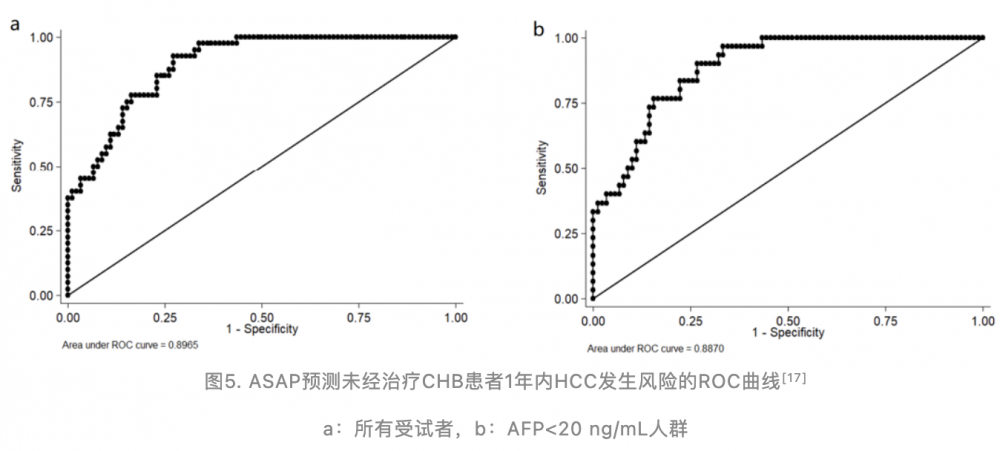
研究者自中国台湾大学医院纳入接受随访的未经治疗的非肝硬化CHB患者,包括69例HCC患者(HCC组)和102例非HCC患者(对照组),检测HCC发生前1年、HCC确诊时或最后一次随访时的血清样本中的PIVKA-II水平。HCC组的基线PIVKA-II水平显著高于对照组(36 vs. 24 mAU/mL,P=0.013),HCC组的ASAP评分亦显著高于对照组(0.48 vs. 0.25,P<0.001)。PIVKA-II水平和ASAP评分均可预测1年内HCC的发生,PIVKA-II的AUROC为0.76(95%CI:0.68~0.94),ASAP评分的AUROC为0.90(95%CI:0.85~0.95),ASAP评分在AFP水平<20 ng/mL患者中的AUROC为0.89(95%CI:0.83~0.95),详见图5。PIVKA-II预测1年内HCC发生的最佳临界值为31 mAU/mL,灵敏度为65%,特异度为83%;ASAP评分预测1年内HCC发生的最佳临界值为0.31,灵敏度为92.5%,特异度为71.7%。
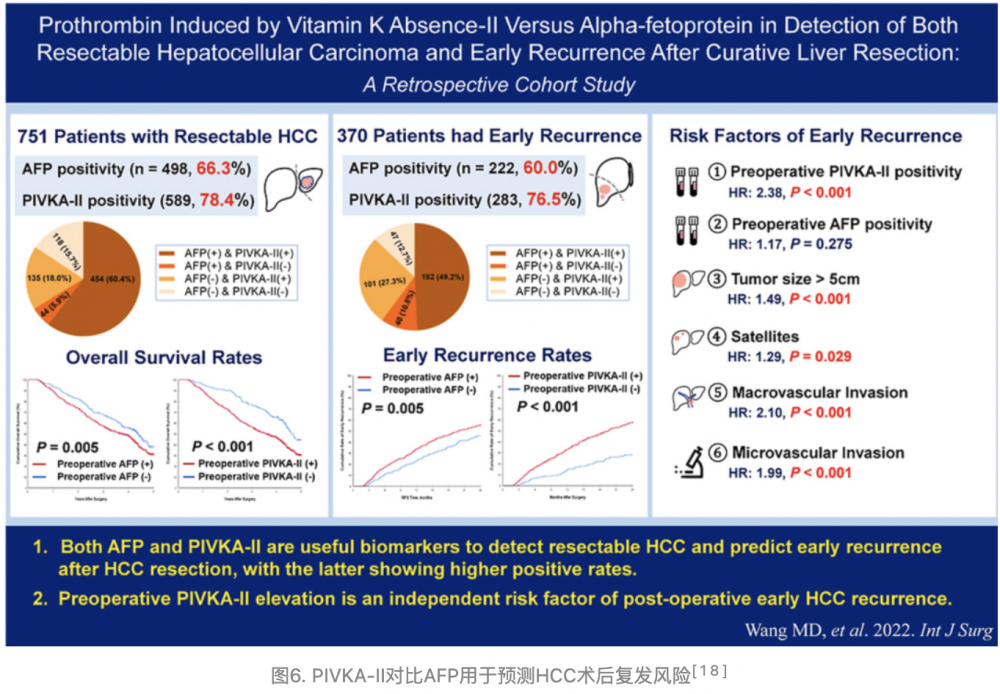
5、PIVKA-II预测术后复发风险[18]

沈锋、杨田教授团队进一步探索PIVKA-II预测术后复发风险的可能性,纳入接受HCC手术治疗的患者,于术前一周内或检测到复发时检测患者血清AFP和PIVKA-II水平。在经过长期随访后发现,早期复发患者中PIVKA-II阳性患者比例较AFP阳性患者更高,且二者差异具有统计学意义。多因素分析表明,术前PIVKA-II阳性(而非术前AFP阳性)是HCC术后早期复发的独立高危因素。因此,术前PIVKA-II阳性对预测HCC术后复发具临床实践意义。
在一百年来对维生素K及其PIVKA-II的不断探索中,肝癌的预测领域显示出了其卓越的生命力。基于PIVKA-II的应用及ASAP模型的发展与成熟,对于中国人群HBV、HCV、NAFLD等病因导致的HCC的预测与诊断日臻完善。目前,ASAP模型已在我国全国范围内被广泛应用,成为肝癌高危人群进行体检筛查和血清学诊断的常规检测项目之一,收获了临床医生和检验医生的高度好评。
此外,凭借基于ASAP模型设计的智能信息解决方案(AlinIQ AMS),ASAP进一步走向国际舞台,荣获“Univants卓越医疗奖”。该项基于智能信息系统的ASAP模型不仅可预测早期肝癌的发生风险,而且可优化肝癌的诊疗路径,临床诊治有效性因此得到极大提高,是一种有效且较具前景的癌症预防策略和多学科协作工具。
未来,希望PIVKA-II和ASAP模型勇攀高峰,继续为我国肝癌的早筛、早诊和早治作出贡献,积极推动优化早期肝癌诊断路径,促进多学科紧密协作,助力中国卓越医疗实践再登世界舞台,不断挖掘早筛早诊的深度和广度,惠及全球更多肝癌风险人群!
参考文献:





