新型冠状病毒疫情中临床实验室生物安全评估与风险控制

新型冠状病毒(2019-nCoV),2020年1月12日被世界卫生组织命名。截止到2020年2月11日,全国新型肺炎确诊42715例,死亡1017例。根据目前掌握的新型冠状病毒生物学特点、流行病学特征、致病性、临床表现等信息,该病原体暂按照病原微生物危害程度分类中第二类病原微生物进行管理。在国家卫健委发布的《新型冠状病毒感染的肺炎诊疗方案》【1】中,将新型冠状病毒疑似患者的呼吸道标本或血液标本实时荧光RT-PCR 检测新型冠状病毒核酸阳性作为确诊标准。随着疫情的发展和蔓延,根据临床诊治的需要,越来越多的临床实验室已经或即将开展新型冠状病毒核酸检测。新型冠状病毒患者样本核酸及其它常规检测作为具有潜在致病和可造成生物安全危害的新的实验室活动,实验室在开展实验活动前,针对新型冠状病毒进行必要的生物安全风险评估,基于生物安全风险评估制定预防措施,实施风险控制,进行生物安全管理,开展实验室活动,确保实验室样本、人员及其环境的生物安全。
面对突如其来的新型冠状病毒疫情,临床实验室应如何进行检验活动中的生物风险评估、采取针对性风险控制预防措施?根据《与风险管理过程有关的术语》【2】定义,风险评估就是风险识别、风险分析和风险评价的全过程。因此,实验室生物风险评估就是根据各实验室开展某一个或是多种致病性生物因子的实验活动时,由具有经验的专业人员对实验全过程中的风险因子进行识别,对风险因子发生可能性及导致后果的严重性可能造成的风险和后果逐一进行分析,评价其风险发生率或确定风险因子的风险等级,在此基础上制定针对性风险控制预防措施,将实验室风险降至可接受程度。对于生物安全二级的临床实验室来说,风险因子主要考虑的内容有:生物因子的特性、涉及生物因子的实验室活动中可能的风险(如:样本采集、运输、离心、保存;核酸检测涉及的加样、提取、扩增,等)、人员相关风险(专业及生物安全知识、心理素质、健康状况等)、设施设备(如:生物安全柜)、感染性废物处置中风险(如:废物容器、包装、标识;灭菌可靠性等)、意外事件带来的风险。值得注意的是,各实验室应结合本实验室的实际情况进行风险评估和采取预防措施,但评估和控制的基本原则、方法应遵循国家、行业的相关标准或指南【3、4】。
本文以某实验室新型冠状病毒生物风险评估报告模板和部分内容为例,期望能为临床实验室人员进一步做好实验室生物风险评估提供帮助。
《新型冠状病毒实验室生物风险评估报告》
一、评估目的与依据
本医院作为定点收治2019-nCoV医院,根据临床诊治需求,检验科将在实验室开展新型冠状病毒感染的疑似和确诊患者各类样本的血尿常规、常规生化以及核酸检测工作。为确保人员、实验室以及样本的生物安全,依据《病原微生物实验室生物安全管理条例》【5】、《医疗废物管理条例》【6】、《实验室生物安全通用要求》【3】(GB19489)等相关法律、法规及标准,以及目前国家权威部门发布的:《新型冠状病毒感染的肺炎诊疗方案》(第五版)【1】、《新型冠状病毒实验室生物安全指南》(第四版)【7】以及《新型冠状病毒感染的肺炎实验室检测技术指南》(第四版)【8】等要求,对实验室检测新型冠状病毒疑似或确诊患者样本的相关实验室活动过程进行生物安全风险评估,作为编制作业指导书和日常生物安全管理的依据。
二、感染因子
新型冠状病毒(2019-nCoV)。
病原学特点:2019-nCoV是β属冠状病毒,有包膜,颗粒呈圆形或椭圆形,直径60-140nm,基因组为线性单股正链的RNA病毒,其基因特征与中东呼吸综合征相关冠状病毒(MERS-CoV)和严重急性呼吸综合征相关冠状病毒(SARS-CoV)有明显区别。目前已获得该病毒的全基因序列、电镜照片。对冠状病毒理化特性的认识多来自对SARS-oV和MER-CoV的研究。病毒对紫外线和热敏感,56℃30分钟,乙醚,75%乙醇,含氯消毒剂,过氧乙酸和氯仿等脂溶剂均可有效灭活。氯乙定不能有效灭活。
三、健康危害
1. 传染源:目前所见传染源主要来自新型冠状病毒感染的肺炎患者,无症状感染者也可能成为传染源。在临床实验室其传染源可能来自新型冠状病毒感染的肺炎患者的拭子、痰液、肺泡灌洗液、粪便、血液等各类样本。
2. 传播途径:经呼吸道飞沫和接触传播是主要的传播途径,气溶胶和消化道等传播途径尚待明确。气溶胶有可能是实验室主要传播途径。
3. 易感人群:人群普遍易感。
4. 潜伏期:潜伏期1-14天,多为3-7天。
5. 临床表现:见(《新型冠状病毒感染的肺炎诊疗方案》第五版【1】)。
四、临床实验室检查
发病早期外周血白细胞总数正常或减低,淋巴细胞计数减少,部分患者出现肝酶、乳酸脱氢酶(LDH)肌酶和肌红蛋白增高。部分危重者可见肌钙蛋白增高。多数患者C 反应蛋白(CRP)和血沉升高,降钙素原正常。严重者D-二聚体升高、外周血淋巴细胞进行性减少。
在咽拭子、痰、下呼吸道分泌物、血液、粪便等标本中可检测出新型冠状病毒核酸。
五、新型冠状病毒的诊断
见(《新型冠状病毒感染的肺炎诊疗方案》第五版【1】)。
(一)疑似病例
结合流行病学史和临床表现综合分析。
(二)确诊病例
疑似病例,具备以下病原学证据之一者:
(1)呼吸道标本或血液标本实时荧光RT-PCR检测新型冠状病毒核酸阳性;
(2)呼吸道标本或血液标本病毒基因测序,与已知的新型冠状病毒高度同源。
六、实验室危害
1. 样本:来自发热门诊、病房所有涉及新型冠状病毒感染的肺炎疑似病例、确诊病例患者的鼻咽拭子、血液、痰液、尿液、粪便、肺泡灌洗液。
2. 主要危害:主要是在检验前、中、后操作过程中产生气溶胶而引起实验室相关感染,还可以通过皮肤、开放性伤口以及粘膜接触感染。
七、预防措施
(一)样本
包括:采集、包装、交接、运输、离心、保存、高压、销毁。
防护措施:
1.《可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》【9】中华人民共和国卫生部令第45号A类UN2814包装、具有三层包装系统(主容器、辅助容器、外标签),符合防水、防破损、防外泄、耐高温、耐高压的要求,并应当印有卫生部规定的生物危险标签、标识、运输登记表、警告用语和提示用语。
2. 接取标本时用专用的转运箱,双方交接记录,专人运输。
3. 标本离心时 , 采用密闭的离心机或戴盖离心杯。离心后静置15分钟,戴盖离心杯应在生物安柜内打开、开帽。4. 做好登记工作,并在检测后进行实验室内的高压处理。
(二)人员
包括:样本运输人员;进入实验室检测人员、工勤人员、公司技术人员。 防护措施:
1. 资质与培训:
(1)资质:核酸检测符合规定资质(有PCR上岗证)、有经验的实验室工作人员经生物安全岗前培训,考试合格、方可上岗。实验室工作人员每年参加体检,预留本底血清标本。实验室工作人员必须在身体状况良好的情况下,才能进入实验室的控制区域工作。出现下列情况,不应进入上述区域:身体出现开放性损伤;患发热性疾病;感冒、上呼吸道感染、或其他导致抵抗力下降的情况;怀孕妇女。工作人员的监测期从开始进行实验,直至实验结束后半个月。若操作者或其所在实验室的工作人员在此期间出现与被操作病原微生物导致疾病类似的症状或者体征时应注意诊断和观察。
(2)培训:针对新型冠状病毒开展专项培训,考核。参加培训的人员:实验室所有工作人员、后勤人员、实习学生等。培训内容:国家和地方卫健委关于新型冠状病毒最新相关文件、样本管理规定、核酸检测流程、生物安全防护要求和意外突发情况处理等。考核结果作为上岗必备的条件之一。
2. 个人防护:所有接触新型冠状病毒感染的肺炎疑似病例、确诊病例患者标本和感染性材料的人员均按照生物安全三级实验室要求进行个人防护:佩戴N95口罩,穿连体防护服,带工作帽,带防雾护目镜,鞋套,双层手套。
3. 非常规活动过程中的人员:进入实验室的维修人员需经过生物安全培训,并告知进入实验室可能出现的危害,知情同意后,由实验室人员陪伴并着装进入实验;维修人员的工作由实验室内务人员或生物安全员全程陪同,并在维修人员工作中及时提醒注意生物安全,可降低维修人员在工作中的危害。当维修人员工作完成后应记录其联系方法,潜伏期内密切关注维修人员是否出现相应的临床症状,如出现相应症状立即报告相关部门,及时就医。
(三)实验室检测活动
本实验室开展针对未灭活新型冠状病毒感染患者的血尿便常规检测、血清生化检测和核酸检测。一层门急诊室确定为新型冠状病毒感染患者常规项目检测区域,项目包括血常规;尿常规;凝血指标;甲乙流金标快检;便常规;血清生化;传染病血清免疫学标志物。四层P2+实验室开展样本新型冠状病毒的核酸提取和 PCR扩增。预防措施:
1. 病毒培养检测要求在BSL-3实验室,本实验室不具备相应生物安全防护水平,因此不能开展病毒培养检测。
2. 本实验室开展针对未灭活新型冠状病毒的血尿便常规检测、血清生化检测和核酸检测,都必须在生物安全二级或加强型生物安全二级实验室内进行,所有操作者应经过生物安全培训并取得相应的资质,并在身体健康状态良好的情况下准入。所有操作者均按生物安全三级实验室个人防护要求。
(1)新型冠状病毒患者未灭活血尿便样本常规检测、血清生化检验集中在BSL-2实验室特定区域进行,开放性操作必须在生物安全柜内操作,尽量减少样本在外暴露时间。所有感染性材料的开放性操作应在实验室生物安全柜中进行。
(2)核酸样本提取、核酸扩增过程均在加强型生物安全二级实验室的生物安全柜中进行。
3. 实验室消毒要求:
(1)实验室常备75%酒精、实验室消毒槽(池)、浸泡缸、喷雾器并备有足量500-1000mg/L有效氯含量消毒溶液供随时消毒使用。
(2)每天对实验室使用有效氯500mg/L的消毒溶液擦拭桌面,用20g/L的过氧乙酸进行空气喷雾消毒(8ml/m2),消毒完毕密闭房间作用2小时,再开窗通风或开启紫外线消毒装置进行空气消毒,照射时间不低于30min。
4. 实验废物灭菌要求:每天将所有实验后一次性感染性试验材料经双层黄色密封袋送至本实验室高压灭菌锅进行高压灭菌(121℃ 30min),之后放置固定暂存处待医院统一回收销毁。
八、实验过程风险识别和风险控制(详见附录)
九、关键设施、设备相关风险
1. 生物安全柜:一层实验室检测专区共配有两台AII型生物安全柜,P2+实验室核心区配有一台BII型生物安全柜。所有生物安全柜年检合格。当安全柜风量或柜内负压低于设定参数50%,应停止工作,安全柜和室内消毒后按常规撤出,修复后可使用;柜内出现正压应立即切断电源,停止工作,在严密个人防护条件下进行彻底消毒,实验室封闭24h,全面检修,各项参数正常稳定运转后才可以重新使用。
2. P2+实验室:应确保实验室气流、负压、高效过滤装置维持正常运转并做好记录。当负压持续低于设定压差80%时,应停止工作,人员按常规撤出,检查修复后才可以使用;如果出现正压,应立即停止工作,人员按规定紧急撤出,在严密个人防护条件下进行彻底消毒,实验室封闭24h,全面检修,各项参数正常稳定运转后才可以重新使用。
3. 检测设备:目前实验室把检测新冠病毒确诊及疑似病人的标本收集在相对集中,又具备通风条件的固定检验场所进行检测,实验室设备包括全自动血细胞分析仪、尿干化学分析仪、自动凝血分析仪、全自动生化分析仪、全自动化学发光分析仪、全自动流式细胞分析仪等11台检测设备。每日进行常规的维护保养、质控,定标,确保检测结果的准确性。部分项目采用干浴56度灭活1小时,再进行检测,降低感染风险。血常规尽量采用不开盖的模式进行检测,使用其他无法灭活样本均在生物安全柜内开盖。全自动设备必须使用加盖模式,防止污染,放入仪器待检测完毕后使用有效氯含量2000mg/L的消毒液擦拭消毒。最后工作结束,实验人员撤离后使用过氧乙酸气溶胶喷雾器喷雾消毒。
4. 实验室消毒间配备了压力蒸汽灭菌器,P2+实验室污物间配备了小型高压灭菌锅。
实验室应确保每一个操作人员掌握各类检测设备、实验室生物安全柜、压力蒸汽灭菌器的标准操作规程,以及出现意外事故的应急培训。应特别关注压力表、温度表及灭菌效果。实验室应建立日常维护计划,每年进行年检。
十、意外事故的处理
1. 一般实验室事故:可能造成人身伤害的实验室事故,如污染物溅落在桌面、割伤等情况,应立即紧急处理:
(1)在污染处覆盖含0.55%有效氯浓度消毒液湿毛巾,并用10% 84消毒液消毒,在旁边文字说明消毒中。
(2)未破溃的皮肤表面用消毒液清洗,伤口用碘酒酒精消毒,事故的情况应及时向领导报告。根据感染高致病冠状病毒的可能性,决定预防性使用对高致病冠状病毒有效的抗病毒药物,并对受伤害者进行隔离观察。
2. 实验材料被误用和恶意使用:本实验室执行严格准入制度及门禁系统,实验人员经过严格考核和培训,样本及感染性材料有双人共管流程,用来有效防止实验材料被误用和恶意使用的风险小。
十一、评估综合结论
综上所述,新型冠状病毒是2019年新发现的病毒,比较容易直接或间接在人与人间传播,且能够引起人类严重疾病,目前没有针对该病毒的有效人用疫苗。本实验室相关实验操作评估结论如下:
1. 本实验室不具备三级实验室的条件,因此不开展新型冠状病毒培养、患者血培养与药物敏感性试验、痰培养检查等高风险检测工作。
2. 所有新冠状病毒疑似、确诊病例临床标本的实验操作都应在生物安全二级或二级加强型实验室完成。其中,未灭活样本核酸提取和基因扩增检测在P2+生物安全实验室开展;其余常规检测均在生物安全二级实验室专门区域集中开展。确保实验室感染与泄露风险低风险。
3. 实验活动全过程操作者均按生物安全三级实验室个人防护。按照作业指导书要求熟练完成实验活动,能识别实验活动可能发生的风险,并掌握相应的风险控制措施的处理方法,具备意外事件、事故分析的识别能力,能够按照相应措施处理事件。人员管理有明确的规范和培训考核制度,能识别人员风险并有相应的措施控制风险。可确保降低实验活动中风险发生的几率。
4. 实验室的设施、仪器设备具有严格的管理和使用规范,并有意外事件风险识别和控制措施,可确保实验室的生物安全。
5. 实验室具备严格的消毒与灭菌管理与实施规范流程,并有意外事件风险识别和控制措施,可确保实验室的生物安全。
经综合评估,实验室开展新型冠状病毒核酸以及血常规、尿常规、便常规、凝血指标、甲乙流金标快检、血清生化、传染病血清免疫学标志物、T细胞亚群等项目实验室检测活动,生物风险可控。
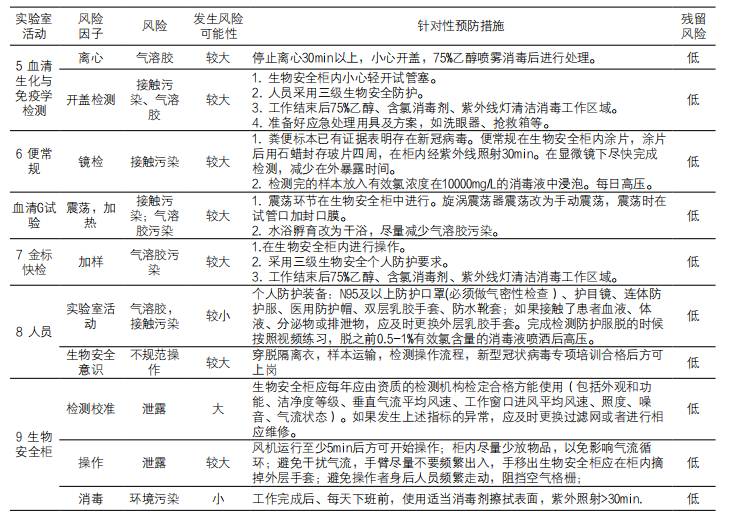
附录 实验过程风险识别和风险控制一览表

衷心感谢军事科学院军事医学研究院教授、CNAS实验室生物安全认可主任评审员陆兵老师对本文的帮助和指导!
参考文献
1《新型冠状病毒感染的肺炎诊疗方案》(第五版),国家卫生健康委.
2《与风险管理过程有关的术语》GB/T 23694-2013.
3 ISO 31000:2018 Risk management-Guidline.
4《实验室生物安全通用要求》(GB19489).
5《病原微生物实验室生物安全管理条例》(中华人民共和国国务院令第424号).
6《医疗废物管理条例》(中华人民共和国国务院令第380号).
7《可感染人类的高致病性病原微生物菌(毒)种或样本运输管理规定》(中华人民共和国卫生部令第45号).
8《新型冠状病毒实验室生物安全指南》(第四版),国家卫生健康委.
9《新型冠状病毒感染的肺炎实验室检测技术指南》(第四版),国家卫生健康委.

收稿日期:2020-02-10




