规范应用心肌肌钙蛋白和利钠肽现场快速检测专家共识(2020年)
【摘要】多项研究和国内外指南建议使用心肌肌钙蛋白(cTn)和B型利钠肽(BNP)/N末端B型利钠肽原(NT-proBNP)用于急性冠状动脉综合征(ACS)和急、慢性心力衰竭的诊断、鉴别诊断和危险分层,以指导相关治疗。鉴于胸痛和胸痛等同症状以及胸闷(呼吸困难)是心血管病患者常见症状,而现场快速检测(point-of-care testing,POCT)具有仪器小型化、操作简单化、结果报告即时化(2~10min内提供结果)、不受时间与地点限制等优势,本共识优先推荐特异度和灵敏度都较好的POCT技术检测cTn和BNP/NT-proBNP分别作为怀疑ACS和心力衰竭患者在适宜临床情况下的初诊检测项目。但POCT在快速获得测试结果、检验周转时间短的情况下,可能会牺牲部分结果的准确性,还存在医生不规范使用POCT和解读检测结果以及质量控制与管理等影响结果准确性的因素,甚至有可能导致错误的临床决策,因此对POCT也需要加强质量管理。为规范POCT技术检测cTn和BNP/NT-proBNP在临床的应用,特编写该共识。
【关键词】现场快速检测;心肌肌钙蛋白;利钠肽;急性冠状动脉综合征;心力衰竭
现场快速检测(point-of-care testing,POCT)也称患者近旁检测[1],具有仪器小型化、操作简单化、结果报告即时化(2~10min内提供结果)、不受时间与地点限制等优势,已经广泛用于第一救治现场,如患者转运途中、急诊、病房及手术室甚至基层诊所等,可用于疾病早期筛查、危险分层、快速诊断和疗效检测等场景,有利于节省医疗成本和推动分级诊疗的实施[2]。2004~2013年期间,丹麦的POCT的总体使用率增加了45.8%[3],2015年苏格兰60%的POCT服务已下沉至基层医疗机构。我国心血管疾病患病率呈持续上升趋势,现患人数预估为3.30亿,死亡率居首位[4-5]。鉴于胸痛和胸痛等同症状以及胸闷(呼吸困难)是心血管病患者常见症状,本共识优先推荐特异度和灵敏度都较好的心肌肌钙蛋白(cTn)和B型利钠肽(BNP)/N末端B型利钠肽原(NT-proBNP)分别作为怀疑急性冠状动脉综合征(ACS)和心力衰竭患者在适宜临床情况下的初诊检测项目。cTn是诊断急性心肌梗死和心肌损伤的“金标准”[6-9],与肌酸激酶同工酶(CK-MB)相比,灵敏度和特异度更高[10]。在近期公布的欧洲心脏学会非ST段抬高的ACS指南中,cTn是唯一推荐的生物标记物;而且心力衰竭患者入院时也建议行cTn检测,用于急性心力衰竭患者的病因诊断(如急性心肌梗死)和预后评估。多项研究和国内外指南建议BNP或NT-proBNP检测推荐用于心力衰竭筛查、诊断和鉴别诊断、病情严重程度及预后评估[11-12]。POCT的主要优点是能快速获得测试结果、检验周转时间短,从而有助于医生快速做出临床决策,但可能会牺牲部分结果的准确性[1]。此外,在院内提供POCT服务时,存在设备维护、人员培训、与实验室系统的连接、质量控制与管理等一系列影响结果准确性的因素,尤其是当操作不规范或质控效果不佳时,POCT结果的准确性会大大降低,从而导致错误的临床决策,因此对POCT也需要加强质量管理。为规范POCT技术检测cTn和BNP/NT-proBNP在临床的应用,由国内长期从事心脏疾病救治和预防、实验室检测的多学科专家组,通过复习医学文献并结合临床实践经验,在借鉴国内外相关指南和专家共识的基础上,结合我国具体情况,编写了《规范应用心肌肌钙蛋白和利钠肽现场快速检测专家共识》,旨在规范并指导POCT的相关临床应用。
一、POCT技术检测cTn和BNP/NT-proBNP的临床应用
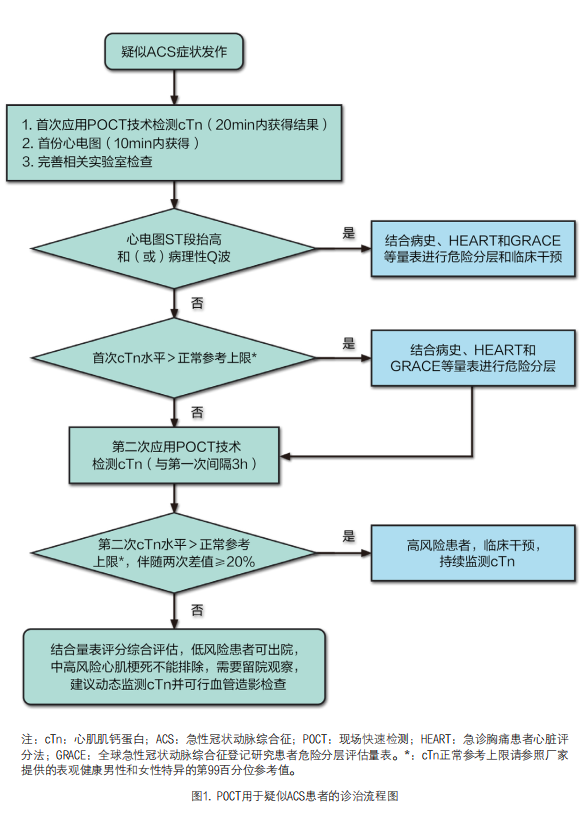
1. POCT技术检测cTn:对于胸痛或胸痛等同症状患者,结合常规的病史询问、体检和心电图检查,POCT技术检测cTn可对疑似ACS患者进行排除、诊断及危险分层[13]。中国胸痛中心的认证标准明确指出,胸痛中心应配备心肌损伤标志物和BNP/NT-proBNP等POCT检查设备,并建议检测cTn的结果应在抽血后20 min获得[14]。对于心力衰竭患者,也推荐检测cTn,用于急性心力衰竭患者的病因诊断(如急性心肌梗死)和预后评估。在紧急情况下,可使用POCT技术检测cTn用于ACS的排除、诊断和危险分层(图1)。在北美开展的急诊医师调查中,75%的医生认为心肌损伤标志物的报告时间应小于45min[14]。
cTn由cTnI、cTnT和cTnC三种不同的亚基组成,其中cTnI和cTnT是实现心肌细胞收缩功能的组分,几乎只在心脏中表达[15]。血液中cTn水平升高超过正常参考值上限99百分位,且存在动态升高或降低时,考虑存在急性心肌损伤[6]。cTnI有心肌特异性,非心脏组织损伤后水平不会升高;而骨骼肌损伤也可能会使cTnT水平升高[15],临床解读需要考虑cTn的检测种类。
尽管cTn水平升高可反映心肌细胞损伤,但心肌蛋白释放可由多种原因造成,如心肌细胞的正常更新、凋亡、cTn降解产物的细胞释放、细胞膜通透性增加、心肌细胞坏死等[16-17]。因此,应该针对具体情况解释cTn测试结果[6]。但无论何种机制,cTn值出现了动态上升和(或)下降都表明发生了急性心肌损伤,临床上应注意非冠状动脉事件的cTn升高和其他干扰cTn检测结果的因素。高敏cTn因其较高的敏感度得到广泛应用,但目前的POCT设备尚未达到实验室标准的高敏cTn检测要求。
2. POCT技术检测BNP/NT-proBNP:BNP和NT-proBNP是利钠肽家族中反映心力衰竭严重程度的血清标志物,与心力衰竭的不良预后有关[18]。血液中利钠肽水平与不同程度的心力衰竭事件具有很强的相关性,诊断准确率可提高至80%[19]。国内外指南均建议,所有急性呼吸困难和疑似急性心力衰竭患者中,均应测量血清BNP或NT-proBNP水平,以区分急性心力衰竭与非心脏原因引起的急性呼吸困难。在紧急情况下,推荐POCT用于疑似心力衰竭患者的排除、诊断、危险分层(图2)。对于有发生心力衰竭风险的患者,以利钠肽生物标记物为基础的筛查,结合优化药物治疗,可以有效地预防左心室功能不全或新发心力衰竭。因此,对于社区中存在心力衰竭的高风险人群,无中心实验室检查利钠肽条件的医院或诊所可考虑应用POCT技术检测利钠肽,进行早期心力衰竭筛查和治疗。一项纳入14项随机对照试验(RCT)的荟萃分析表明,相比常规临床组,BNP指导的治疗组显著降低了心力衰竭相关的住院风险(RR=0.79)[20]。另一项多临床中心研究表明,NT-proBNP指导治疗的高危心力衰竭患者组的心血管死亡率为12%,常规护理组的心血管死亡率为13%[21]。
BNP前体形成后裂解成为BNP和NT-proBNP,BNP由心室肌细胞分泌后入血,通过血清中的BNP受体C和中性内肽酶降解清除,而NT-proBNP在肌肉、肝脏等组织器官中降解,仅通过肾脏排泄清除。虽然二者等摩尔分泌,但半衰期存在差异,BNP为20min,NT-proBNP为120min[22]。
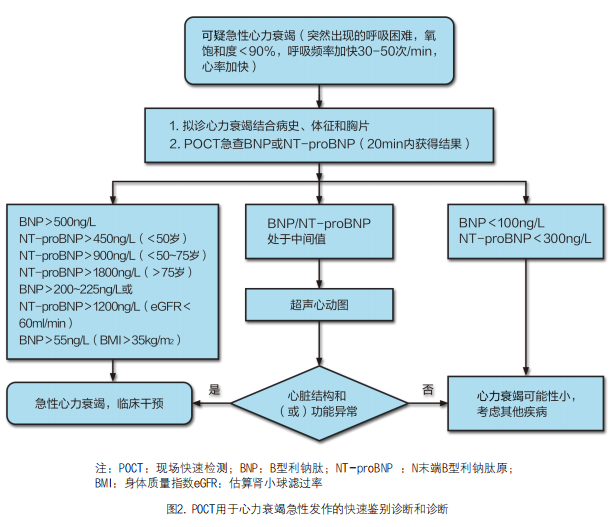
利钠肽具有很高的敏感度,疑似急性心力衰竭患者若血浆水平正常则通常可排除急性心力衰竭。将BNP和NT-proBNP的阈值设置为100ng/L和300ng/L时,其敏感度分别为0.95(95%CI:0.93~0.96)和0.99(95% CI:0.97~1.00),阴性预测值分别为0.94(95% CI:0.90~0.96)和0.98(95% CI:0.89~1.0)[23],较高的阴性预测值是其主要优势,在排除心力衰竭方面具有很高的效能[24]。2016年欧洲心脏病学会急性和慢性心力衰竭诊断和治疗指南[25]和2014年加拿大心血管学会心力衰竭治疗指南[26]建议,在紧急情况下,BNP值小于100ng/L或NT-proBNP值小于300ng/L时可排除急性心力衰竭的诊断。但BNP和NT-proBNP在排除心力衰竭的效能方面有差异[27]。BNP值高于400ng/L与心力衰竭的诊断有关,而NT-proBNP的诊断临界值随患者年龄和性别而变化[25]。虽然利钠肽在诊断心力衰竭具有很高的敏感度和特异度,许多心脏和非心脏因素可影响BNP或NT-proBNP的水平,心脏因素包括ACS、左心室肥厚、瓣膜性心脏病、心包疾病、心房颤动、心肌炎、心脏手术、电转复后和癌症化疗药物的心脏毒性等;非心脏原因包括性别、年龄、贫血、肥胖、肾功能不全、脓毒症、肺感染和慢性阻塞性肺脏疾病等,不能单独依据利钠肽升高来诊断心力衰竭,需要结合临床综合判断[28];诊断急性心力衰竭时,NT-proBNP水平应根据年龄和肾功能不全分层。某些心力衰竭终末期患者的利钠肽水平甚至可能会很低[25]。
临床研究表明,当利钠肽的POCT分析使用与中心实验室相同的抗体和标准材料时,分析结果无较大差异[29-30]。与常规诊疗相比,POCT技术检测BNP可将治疗时间缩短27min,住院时间缩短4d,医疗成本降低26%[31]。但不同的POCT结果存在差异。有研究报道,不同的BNP免疫测定法之间的结果差异高达50%,因此建立标准化的POCT十分必要[32]。
3. POCT技术检测cTn和BNP/NT-proBNP用于新型冠状病毒肺炎(COVID-19)的诊治:COVID-19主要累及呼吸系统,还可损伤其他各个系统,尤其是心血管系统,以心肌损伤最常见。心肌损伤在COVID-19住院患者中的发病率约为7.2%-40.9%,在重症和死亡患者中更为常见。COVID-19相关心肌损伤的临床症状并不特异。胸痛可能提示心肌损伤的发生。约13%的心肌损伤患者出现胸痛症状,而在无心肌损伤的患者中只有不到1%。心肌损伤是COVID-19病情恶化和死亡的独立危险因素,在院出现了心肌损伤的患者死亡风险是无心肌损伤患者的6.6~26.9倍。老年、合并慢性基础病的患者更易发生心肌损伤。且一旦发生心肌损伤,有基础病的患者的死亡率远高于无基础病的患者(69.4% vs. 37.5%)[33]。
对于COVID-19确诊和疑似病例的心肌损伤检测,由于有可能存在病毒血症,血液样本有传染性,应尽可能减少标本的转运、接收、分拣和离心等操作,以降低医护人员感染的风险。建议采用体积小巧、灵活可移动的POCT装备在患者床旁完成快速检测,如果是微流控技术测试可在单张测试卡上完成,避免交叉和人工干预造成的污染。标本采集和常规的生化血气等检查应该遵循最新的COVID-19相关实验室检测的生物安全指南,采用三级生物安全防护。
推 荐:
(1)推荐院前急救、急诊分诊、胸痛中心、重症监护病房(ICU)、冠心病监护病房(CCU)等处理急危重症患者的医疗场所常规配备可检测cTn和BNP/NT-proBNP的POCT设备,并且中心实验室具备cTn和BNP/NT-proBNP等相关检测项目。
(2)推荐内科、老年科、呼吸科等有可能处理心脑血管疾病急症的医疗场所配备可检测cTn和BNP/NT-proBNP的POCT设备,并且中心实验室具备cTn和BNP/NT-proBNP等相关检测项目。
(3)对于基层诊所或社区医院也建议配备可检测cTn和BNP/NT-proBNP的POCT设备,若根据病史、心电图和临床表现明确为ACS或心力衰竭患者应尽快转诊,对于病史、心电图和临床表现不典型但cTn或BNP/NT-proBNP检测异常的患者也应尽快转诊。
(4)POCT技术检测cTn和BNP/NT-proBNP结果报告应在20min内完成,诊断和鉴别诊断应当结合病史、体检结果、心电图、影像学检查等。
(5)POCT技术检测cTn和BNP/NT-proBNP时推荐使用提供定量结果的POCT检测设备。
(6)由于POCT主要优势在于即时性,出现阴性结果需要联合辅助评价措施,并同时采用中心实验室复查,对于疑似ACS的患者需要进行动态检测。
(7)POCT和实验室的检测结果不能直接比较,只有使用相同的检测平台和相同的心脏标志物才可比较。
二、POCT质量管理
在提供POCT服务时,存在设备维护、人员培训、与实验室系统的连接、质量控制与管理等一系列影响结果准确性的因素,尤其是当操作不规范或质控效果不佳时,POCT结果的准确性会大大降低,从而导致错误的临床决策,因此POCT的质量管理发挥着重要作用[27]。有研究表明,在实验室专业人员的支持下,对POCT实施质量管理将会提高测试结果的质量[34]。质量管理应纳入院内整体的POCT质量管理体系,建立院级指导性文件和心血管疾病标志物POCT专属的人、机、物、法、环管理实施细则文件[35-36]。
对POCT的质量保证包括内部质量控制和外部质量保证。内部质量控制旨在检测、减少和纠正POCT过程中的偏差,应针对cTn和BNP/NT-proBNP检测制定各自的POCT内部质控计划。通常每天可采取浓度已知的分析物作为质控液,至少包括高、低两个浓度,将POCT结果与预期值范围进行比较[37]。尤其是在诊断界值附近,应有对应浓度的质控品。外部质量保证旨在保证某院内检查测试结果的整体质量,外部质量保证在解释结果一致性方面非常重要,通常结果的差异来源于操作者、设备和地点等因素。每家医疗机构应根据使用的POCT设备和其他因素确定本单位的参考值范围和临床诊断界值。对于cTn检测方法,应在不少于10%的表观健康男性和女性人群中均能够检测到cTn,并且检测值等于或高于最低检测限。
POCT操作人员应做好日常质量控制、质量控制记录填写和POCT结果的报告。POCT结果必须与时间、患者信息和消耗品批号一起记录,从而有利于结果的追溯。胸痛中心POCT从采集到报告结果应在20min以内完成。
推 荐:
(1)建议采用酶联免疫法、免疫荧光或化学发光技术的定量方法进行分析。样本类型最好能够兼容全血和血浆。建议设备应该具有有线或无线数据传输功能,通过实验室信息管理接口实现数据电子化。
(2)建议定期将POCT结果与中心实验室结果做对比,进行质量控制,POCT方法与中心实验室检测结果间偏倚应≤20%。有条件最好每年评估1次POCT分析灵敏度和功能灵敏度。cTn检测方法应评估最低检测限和10%和20%变异系数时的最低功能检测限。传统cTn可报告范围上限至少达到50ng/ml,BNP达到5,000pg/ml, NT-ProBNP达到30,000pg/ml。
(3)对于不同厂家产品应建立自己的表观健康男性和女性特异度的第99百分位值,并评估其对表观健康人群的检出率。对于cTn检测方法在不少于10%的表观健康男性和女性人群中均能够检测到cTn,并且检测值等于或高于最低检测限。为了更好地针对具体的患者人群和临床实践,每个机构均应确立本单位的参考范围和判断水平。
(4)cTn检测在第99百分位值对应的变异系数≤10%;BNP/NT-proBNP检测在急慢性心力衰竭诊断截断值附近对应的变异系数≤10%;
(5)制定室内质控计划,每天检测样本前应检测各厂家提供配套质控液或第三方质控品,至少包括高、低两个浓度。尤其注意在诊断界值附近,应有对应浓度的质控品。质控超出精密度要求时宜具备警告提示。
(6)每台设备参加国家级或省部级临床检验中心组织的室间质评活动。若同一医疗机构内设备较多,建议选择日均检测标本量较多的临床科室设备参加室间质评计划,同时定期组织全院POCT设备间以及与中心实验室的比对。
(7)结果报告名称应符合标准全称和英文缩写,勿混淆高敏和普通敏感性cTn,检测结果报告单位应采用国际公认单位,高敏cTn单位为ng/L,传统cTn为µg/L 或者ng/ml。
(8)对于一个设备点,最好设置设备专员进行重点、深入培训,使其掌握基本原理、性能以及主要影响因素,熟练进行样本和质控物检测。
三、问题与展望
POCT技术检测cTn和BNP/NT-proBNP有较高的灵敏度和特异度,在初级医疗机构中,部分POCT在临床结果上的效能被证明与中心实验室无异,也获得很高的患者满意度[18]。但POCT的优势依赖于POCT的质量管理,在制度上也存在一系列障碍,只有遵循质量管理的实践指南,才能有效确保结果的准确性,为临床决策快速提供依据。全球POCT市场预计将从2017年的230亿美元增长到2022年的380亿美元,主要驱动力来自重症监护医学和以患者为中心的个性化医疗领域中POCT使用的增加,因此未来POCT在医疗机构的应用将呈不断上升趋势[38]。此外,模型研究表明,重新设计优化POCT流程,充分利用减少的治疗周转时间,可进一步降低成本,从而达到高的成本效益[39-40]。遗憾的是,目前缺乏将POCT与中心实验室进行比较并评估临床结果的RCT研究,长期的POCT真实临床结局仍需进一步的研究[18]。未来应规范cTn和BNP/NT-proBNP的POCT在医疗卫生机构的应用,因为确保POCT结果的质量至关重要;还应了解患者和临床医生的需求,基于需求再研究新的POCT技术,从而改善临床护理。
执笔者: 叶绍东(中国医学科学院阜外医院),黎励文(广东省人民医院),蔺亚晖(中国医学科学院阜外医院),周洲(中国医学科学院阜外医院),唐熠达(中国医学科学院阜外医院)
北京精准医学学会 国家心血管病中心心血管代谢专病医联体共识编委会成员(以姓氏汉语拼音排序):程翔(华中科技大学同济医学院附属协和医院),郭远林(中国医学科学院阜外医院),胡敏(中南大学湘雅二医院),黎励文(广东省人民医院),李广平(天津医科大学第二医院),李琳(中国医学科学院阜外医院),李勇(复旦大学附属华山医院),陆士娟(海南省海口市人民医院),刘刚(河北医科大学附属第一医院),刘君(河北医科大学第一医院),刘铭(天津医科大学总医院),鲁志兵(武汉大学中南医院),裴海峰(中国人民解放军西部战区总医院),沈雳(复旦大学附属中山医院),孙伟(江苏省人民医院),唐熠达(中国医学科学院阜外医院),佟倩(吉林大学附属第一医院),汪芳(北京医院),王丽(石河子大学医学院第一附属医院),王伟(汕头大学附属第二医院),王学峰(上海交通大学医学院附属瑞金医院),徐通达(徐州医科大学附属医院),杨进刚(中国医学科学院阜外医院),杨清(天津医科大学总医院),严晓伟 (中国医学科学院北京协和医院),袁慧(首都医科大学附属北京安贞医院),曾建平(湖南省湘潭市中心医院),张力(浙江大学医学院附属第一医院),张洋(中国医学科学院阜外医院),张真路(武汉亚洲心脏病医院),周洲 (中国医学科学院阜外医院),钟志雄(广东省梅州市中心医院)
利益冲突:所有作者均声明不存在利益冲突
参考文献
Christenson RH, Azzazy HM. Cardiac point of care testing: a focused review of current National Academy of Clinical Biochemistry guidelines and measurement platforms[J]. Clin Biochem, 2009, 42(3): 150-157. DOI: 10.1016/j.clinbiochen.2008.09.105.
Pecoraro V, Germagnoli L, Banfi G. Point-of-care testing: where is the evidence? A systematic survey[J]. Clin Chem Lab Med, 2014, 52(3): 313-24. DOI: 10.1515/cclm-2013-0386.
Haldrup S, Thomsen RW, Bro F, et al. Microbiological point of care testing before antibiotic prescribing in primary care: considerable variations between practices[J]. BMC Fam Pract, 2017, 18(1): 9. DOI : 10. 1186/s12875-016-0576-y.
中国心血管健康与疾病报告编写组. 中国心血管健康与疾病报告2019概要[J]. 中国循环杂志, 2020, 35(9): 833-854. DOI: 10.3969/j.issn.1000-3614.2020.09.001
GBD 2013 Mortality and Causes of Death Collaborators. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013[J]. Lancet (London, England), 2015, 385(9963): 117-171. DOI: 10.1016/S0140-6736(14)61682-2.
Thygesen K, Alpert JS, Jaffe AS, et al. Fourth universal definition of myocardial infarction (2018) [J]. Circulation, 2018, 138(20): e618-e651. DOI: 10.1161/CIR. 0000000000000617.
Roffi M, Patrono C, Collet JP, et al. 2015 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: task force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation of the European Society of Cardiology (ESC) [J]. Eur Heart J, 2016, 37(3): 267-315. DOI: 10. 1093/eurheartj/ehv320.
Chew DP , Scott IA , Cullen L , et al. National heart foundation of australia & cardiac society of australia and new zealand: australian clinical guidelines for the management of acute coronary syndromes 2016[J]. Med J Aust, 2016, 25(9): 895-951. DOI: 10.5694/mja16. 00368.
闵俊. 国家卫生计生委印发《胸痛中心建设与管理指导原则(试行)》[J]. 中华医学信息导报, 2017, 21: 6.
Goodman SG, Steg PG, Eagle KA, et al. The diagnostic and prognostic impact of the redefinition of acute myocardial infarction: lessons from the Global Registry of Acute Coronary Events (GRACE) [J]. Am Heart J, 2006, 151(3): 654-660. DOI: 10.1016/j.ahj.2005.05.014.
中华医学会心血管病学分会心力衰竭学组, 中国医师协会心力衰竭专业委员会, 中华心血管病杂志编辑委员会中国心力衰竭诊断和治疗指南2018[J]. 中华心力衰竭和心肌病杂志, 2018, 2(4): 196-225. DOI: 10.3760/cma.j.issn.2096-3076.2018.12.02.
Yancy W, Jessup M, Bozkurt B, et al. 2017 ACC/AHA/HFSA focused update of the 2013 ACCF/AHA guideline for the management of heart failure: a report of the American College of Cardiology/American Heart Association task force on clinical practice guidelines and the Heart Failure Society of America[J]. Circulation, 2017, 136(6): e137-e161. DOI: 10.1161/CIR. 0000000000000509.
“胸痛中心”建设中国专家共识组. “胸痛中心”建设中国专家共识[J]. 中华危重症医学杂志, 2011, 4(6): 21-29. DOI: 10. 3877/cma.j.issn.1674-6880.2011.06.006.
Novis DA, Jones BA, Dale JC, et al. Biochemical markers of myocardial injury test turnaround time: a College of American Pathologists Q-Probes study of 7020 troponin and 4368 creatine kinase-MB determinations in 159 institutions[J]. Arch Pathol Lad Med, 2004, 128(2): 158-164. DOI: 10.1043/1543-2165(2004)128<158: BMOMIT>2. 0CO;2.
Rittoo D, Jones A, Lecky B, et al. Elevation of cardiac troponin T, but not cardiac troponin I, in patients with neuromuscular diseases: implications for the diagnosis of myocardial infarction[J]. J Am Coll Cardiol, 2014, 63(22): 2411-2420. DOI: 10.1016/j.jacc.2014.03.027.
Mair J, Lindahl B, Hammarsten O, et al. How is cardiac troponin released from injured myocardium?[J]. Eur Heart J Acute Cardiovasc Care, 2018, 7(6): 553-560. DOI: 10.1177/2048872617748553.
White HD. Pathobiology of troponin elevations: do elevations occur with myocardial ischemia as well as necrosis?[J]. J Am Coll Cardiol, 2011, 57(24): 2406-2408. DOI: 10.1016/j.jacc.2011.01.029.
Florkowski C, Don-wauchope A, Gimenez N, et al. Point-of-care testing (POCT) and evidence-based laboratory medicine(EBLM) - does it leverage any advantage in clinical decision making?[J]. Crit Rev CLin Lab Sci, 2017, 54(7-8): 471-494. DOI: 10.1080/10408363.2017.1399336.
Alawieh H, Chemaly TE, Alam S, et al. Towards point-of-care heart failure diagnostic platforms: BNP and NT-proBNP biosensors[J]. Sensors (Basel, Switzerland), 2019, 19(22): 5003. DOI: 10.3390/s19225003.
Tang WH. B-type natriuretic peptide: a critical review[J]. Congest Heart Fail, 2007, 13(1): 48-52. DOI: 10.1111/j.1527-5299.2007.05622. X.
Roberts E, Ludman AJ, Dworzynski K, et al. The diagnostic accuracy of the natriuretic peptides in heart failure: systematic review and diagnostic meta-analysis in the acute care setting[J]. BMJ, 2015, 350: h910. DOI: 10.1136/bmj.h910.
Balion C, Mckelvie R, Don-wauchope AC, et al. B-type natriuretic peptide-guided therapy: a systematic review[J]. Heart Fail Rev, 2014, 19(4): 553-564. DOI: 10.1007/s10741-041-9451-x.
Ponikowski P, Voors AA, Anker SD, et al. 2016 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure: the task force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) developed with the special contribution of the Heart Failure Association (HFA) of the ESC[J]. Eur Heart J, 2016, 37(27): 2129-2200. DOI: 10.1002/ejhf. 592.
Moe GW, Ezekowitz JA, O'meara E, et al. The 2014 Canadian Cardiovascular Society heart failure management guidelines focus update: anemia, biomarkers, and recent therapeutic trial implications[J]. Can J Cardiol, 2015, 31(1): 3-16. DOI: 10.1016/j.cjca.2014.10.022.
Hill SA, Booth RA, Santaguida PL, et al. Use of BNP and NT-proBNP for the diagnosis of heart failure in the emergency department: a systematic review of the evidence[J]. Heart Fail Rev, 2014, 19(4): 421-438. DOI: 10.1007/s10741-014-9447-6.
李迪, 廉姜芳. BNP/NT-proBNP诊断心力衰竭影响因素的研究进展[J]. 现代实用医学, 2010, 22(8): 954-956. DOI: 10.3969/j.issn.1671-0800.2018.08.063.
Xin W, Lin Z, Mi S. Does B-type natriuretic peptide-guided therapy improve outcomes in patients with chronic heart failure? A systematic review and meta-analysis of randomized controlled trials[J]. Heart Fail Rev, 2015, 20(1): 69-80. DOI: 10.1007/s10741-014-9437-8.
Felker GM, Anstrom KJ, Adams KF, et al. Effect of catriuretic peptide-guided therapy on hospitalization or cardiovascular mortality in high-risk patients with heart failure and reduced ejection fraction: a randomized clinical trial [J]. JAMA, 2017, 318(8): 713-720. DOI: 10.1001/jama.2017.10565.
Clerico A, Franzini M, Masotti S, et al. State of the art of immunoassay methods for B-type natriuretic peptides: an update[J]. Crit Rev Clin Lab Sci, 2015, 52(2): 56-69. DOI: 10.3109/10408363.2014.987720.
Franzini M, Masotti S, Prontera C, et al. Systematic differences between BNP immunoassays: comparison of methods using standard protocols and quality control materials[J]. CLin Chim Acta, 2013, 424: 287-291. DOI: 10.1016/j.cca.2013.07.001.
Mueller C, Laule-kilian K, Schindler C, et al. Cost-effectiveness of B-type natriuretic peptide testing in patients with acute dyspnea[J]. Arch Intern Med, 2006, 166(10): 1081-1087. DOI: 10.1001/archinte.166.10.1081.
Clerico A, PAssino C, Franzini M, et al. Cardiac biomarker testing in the clinical laboratory: where do we stand? General overview of the methodology with special emphasis on natriuretic peptides[J]. Clin Chim Acta, 2015, 443: 17-24. DOI: 10.1016/j.cca.2014.06.003.
Wei ZY, Geng YJ, Huang J, et al. Pathogenesis and management of myocardial injury in coronavirus disease 2019. Eur J Heart Fail. 2020 Jul 19. DOI: 10.1002/ejhf.1967.
Price CP, Smith I, Van Den Bruel A. Improving the quality of point-of-care testing [J]. Fam Pract, 2018, 35(4): 358-364. DOI: 10.1093/fampra/cmx120.
中国医学装备协会现场快速检测专业委员会. 手持式现场快速检测(POCT)临床应用与质量管理专家共识[J]. 中华医学杂志, 2018, 98(18): 1394-1396. DOI: 10.3760/cma.j.issn.0376-2491.2018.18.005.
Newman AW, Behling-kelly E. Quality assurance and quality control in point-of-care testing[J]. Top Companion Anim Med, 2016, 31(1): 2-10. DOI: 10.1053/j.tcam.2016.05.003.
Holt H, Freedman DB. Internal quality control in point-of-care testing: where's the evidence?[J]. Ann Clin Biochem, 2016, 53(Pt2): 233-239. DOI: 10.1177/0004563215615148.
Patel K, Suh-lailam BB. Implementation of point-of-care testing in a pediatric healthcare setting[J]. Crit Rev Clin Lab Sci, 2019, 56(4): 239-246. DOI: 10.1080/10408363. 2019. 1590306.
Bingisser R, Cairna C, Christ M, et al. Cardiac troponin: a critical review of the case for point-of-care testing in the ED[J]. Am J Emerg Med, 2012, 30(8): 1639-1649. DOI: 10.1016/j.ajem.2012.03.004.
Bugge C, Sether EM, Pahle A, et al. Diagnosing heart failure with NT-proBNP point-of-care testing: lower costs and better outcomes. A decision analytic study [J]. BJGP open, 2018, 2(3): bjgpopen18X101596. DOI: 10.3399/bjgpopen18X101596.
注:本文转载自:中国循环杂志,2020,(35)269:1045-1051.





