心血管疾病生物标志物临床应用与未来临床诊疗需求
欧洲心脏病学会 Arthur Mark Richards等 编译:王小茜
【摘要】循环生物标志物在心血管疾病(CVD)的风险评估、诊断、预后和疾病管理中起到关键作用。为了达到“最受欢迎”的程度,新的候选标志物必须提供附加的可用、可靠和独立的信息,以便有助于改进临床管理。目前已确定的两种最佳CVD标志物是心脏B型利钠肽和心肌肌钙蛋白。这些标志物反映了心肌细胞的负荷和损伤,并在心力衰竭和急性冠脉综合征的管理中具有确定作用。但是,对于心血管疾病的其他关键病理生理学途径(包括炎症、氧化应激和纤维化),我们缺少类似经过证实的标志物。我们也缺少经过明确验证的、具有优良性能的CVD发病前风险标志物。目前正在评估大量候选标志物是否能满足这些需求,包括细胞因子、肽类、蛋白质、代谢物和循环核酸。随着特定的抗炎、抗氧化和抗纤维化疗法逐渐在CVD的早期阶段确立,我们需要特异性标志物来进行病例选择和疗效评估。
【关键词】心血管;生物标志物;NT-proBNP;心肌肌钙蛋白;炎症;氧化应激;纤维化
生物标志物在心血管疾病(CVD)的风险分层、诊断、预后、疾病监测、治疗剂量滴定和治疗靶标鉴别中发挥重要作用。它们可能表现为心脏或血管成像、血压等体检结果、功能测试或循环物质检测。任何能够提供心血管(CV)风险及其程度或任何现存疾病程度及未来进展信息的可测量生物变量都被视为CV生物标志物。进行此次综述时,我们主要把注意力集中于可测量的血液分析物。血糖、血红蛋白A1c(HbA1c)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL)和总胆固醇使我们自然而然地想到循环生物标志物在CVD检测和管理方面具备的深刻本质特征,以及这些生物标志物如何为糖尿病和血脂异常患者提供诊断信息、风险分层和生活方式干预以及药物治疗指导。除了这些传统的风险标志物和治疗靶标以外,我们还有两种有证据支持和指南指导且被临床广泛应用的主要标志物,即心肌肌钙蛋白和心脏利钠肽。前者对于定义和诊断心肌梗死是必不可少的,也决定着对非ST段抬高冠脉综合征患者立即采取早期有创干预管理策略。后者部分满足了以前未满足的需求,提高了诊断的确定性并提供了急性心衰早期风险分层。那么我们还需要做什么呢?现在和将来的需求是什么?
一、未来标志物需要满足的标准
未来的生物标志物应满足以下一项或多项未被满足的需求:(1)诊断;(2)预后;(3)监测;(4)在CV风险和/或CVD医学管理中提供用于治疗选择和滴定的有效替代终点或治疗靶标。许多标志物由于提供了一部分未知的病理生理学背景信息而具备一定价值,但大多数从来不会被转化到常规管理应用中。新的临床标志物必须以容易实现和可负担起的方式比现行标准实践提供更多信息。新标志物提供的信息必须大大超出已知标志物和预测指标提供的范围,而且在基于证据的管理中,结果必须具有可操作性。如果一个标志物的结果对于临床护理或结局没有合理的影响,那么它在临床实践中就毫无立足之地。我们所关心的测试必须满足高精密度和准确度标准。标志物应与目标疾病具有密切而特异的关系。理想上来说,标志物本质上应为被监测病理过程的一部分。真实反映疾病进展或痊愈及治疗效果的动态标志物比揭示风险却无法改变的标志物特征(如遗传变异)更有价值。随着我们有效应对及管理急性和慢性CVD的能力不断提升,我们需要关注社区人群,并发现和应用能够增强我们执行成本效益高的筛查的能力的标志物,从而更好地发现CVD风险及预防疾病发生。
未满足的需求:明确了希望未来标志物具备的特质之后,我们应考虑目前标志物未满足的需求及新候选标志物的优缺点了。
1. 急性心血管疾病:首先,在急性病中,心肌肌钙蛋白和心脏利钠肽已彻底改变了急性冠脉综合征和心衰的诊断及管理了。然而,它们的缺点很多,而且在临床上很显著。高敏心肌肌钙蛋白I和T检测的出现伴随着急性心肌梗死(AMI)的检测特异性下降。急诊血浆肌钙蛋白升高通常与1型心肌梗死无关,这类患者需要紧急入住冠心病监护室并立即进行心电图监测、抗凝血抗血小板治疗、给予β-受体阻滞药、尽早转入心脏导管实验室进行有创冠脉造影和可能的经皮介入治疗。大约三分之二的急诊患者虽然血浆心肌肌钙蛋白升高且表面上已超过急性梗死阈值,但实际上需要排除AMI而无需接受上述一系列治疗和检测。换句话说,高敏心肌肌钙蛋白检测缺乏特异性,这里的特异性并不是指分析物本身,而是指对需要立即采取措施的AMI诊断缺乏特异性。临床敏锐度结合心电图(ECG)、全面的临床评估和绝对肌钙蛋白升高程度会提高诊断准确度,但很明显我们也需要特异性更高的先进标志物。
类似地,血浆B型利钠肽(BNP)浓度在急性心衰诊断中的作用常常受到其他因素干扰,例如,房颤、肾功能不全和年龄增加使肽类水平升高,而射血分数保留和肥胖则使肽类水平降低。此外,急性心衰以外的许多急性和慢性疾病会扰乱血浆BNP和N末端B型利钠肽前体(NT-proBNP)水平。对于非急性的初期心衰,我们缺乏准确度和特异性足够高的循环生物标志物。欧洲心脏学会在心衰诊断和管理指南中推荐使用 NT-proBNP≤125pg/mL作为排除阈值。这一阈值会产生很多假阳性,尤其是对于有肾功能损伤的老年人来说,更重要的是,会在早期或经过治疗的射血分数保留(HFpEF)心衰患者中产生很多假阴性结果。在所有其他条件相同的情况下,拉普拉斯定律(适用于室壁应力)表明HFpEF心衰患者的血浆循环利钠肽水平要低于射血分数减低(HFrEF)心衰患者。HFpEF心衰患者目前没有经过证实的治疗方法。如果标志物有助于识别适用于HFpEF的新型有效治疗途径和靶标,那将是重大进步。实际上,有数百个候选标志物正在研究中。因此,需要提高BNP和NT-proBNP的特异性,尤其是在非急性 HFpEF情况下。使这一情况更加复杂的是,非AMI和非急性心衰引起的心肌肌钙蛋白和心脏BNP血浆浓度升高仍预示不良预后,但对于此类异常结果的最佳研究和治疗反应仍有待确定。
2. 慢性疾病的风险监测和管理:心衰和冠脉疾病患者与无此类疾病的人群相比,其长期治疗过程伴随着残余过多风险(residual excess risk)。但是,一般而言,当前的最佳做法是对个性化程度相对较低的风险分层进行通用治疗,或在做出诊断(通常在急性情况下)并开始治疗后进行伴随治疗滴定。从观察性数据和随机对照治疗试验的结果很容易得知,“稳定性”慢性心衰概念是一个谬论,5年内的总生存率约为50%,表明心衰的结局具有很大不确定性。我们缺少标志物来改善目前较为粗糙的慢性心衰风险分层,以便医务工作者更有效地分配时间和进行更个性化的药物治疗滴定。B型心脏利钠肽和心肌肌钙蛋白均提供有关慢性心衰的预后信息,但这些标志物在慢性病中的系统应用及其在指导改变药物剂量方面的作用(如有)仍不明确且尚未证实。尽管已对NT-proBNP指导慢性心衰治疗进行了16年的试验,但仍未取得进展。对于所有其他标志物,我们还缺少证据证明重复测量在长期心衰管理中的潜在作用。
3. 主要风险的长期监测和管理:在发病前期(A和B类心衰),标志物未满足的主要需求在于改善风险分层和指导疾病管理。几代以来,心血管风险筛查一直采用粗略的筛选方法。对于中年人,建议使用的CV筛查包括动脉压测量、体重指数、空腹血糖、HbA1c、LDL、HDL和总胆固醇、是否有糖尿病、吸烟状况及早发冠脉疾病家族史。这些Framingham风险因素可以进行大概的风险分层,重点在于“大概”。例如,一位63岁的白人男性,未经治疗前收缩压(BP)160mmHg、总胆固醇6mmol/L、没有糖尿病、不吸烟、也没有CVD病史,在10年内发生重大动脉事件的风险约为15%,如果将BP和脂类水平严格控制在目标水平,则风险可降低为5%。因此,我们将15%的人可能发生的事情降低到5%,却不知道哪15%或5%注定会发生这些事。从资源利用、不准确的患者归类和需要药物治疗、以及不必要的药物分配和支出等方面来看,这种粗略而又不准确的风险评估的后果是显而易见的。为了更准确地鉴别出注定会发生显著CVD的人和有证据表明治疗效果较好的人,我们需要大大改善预测工具。标志物能不能帮助我们实现这一目标呢?社区动脉粥样硬化风险(ARIC)、多种族动脉粥样硬化研究(MESA)、达拉斯心脏研究和世界卫生组织赞助的心血管疾病趋势及决定因素监测(MONICA)等研究提供了社区无CVD人群的长期随访数据。这些队列的生物标志物研究表明,在无症状人群中观察到的表面上正常循环范围内几种不同标志物(hsTnT、NT-proBNP、sFlt 1和GDF15等)的血浆浓度变化,转化为初次采样后十年或更长时间内发生CV事件的概率相差几倍。在无症状社区人群中测量的这些标志物除了与传统风险因素相结合,也可以独立预测CVD事件。
最近的发现表明,Notch信号通路参与了Notch配体的血清浓度变化,反映了扩张型心肌病的舒张功能障碍和疾病严重程度。因此,很明显未来将现有和尚未发现的生物标志物应用到社区人群中有可能改善风险分层,并采用更加合理和个性化的治疗来降低风险。PONTIAC和STOP-HF试验获得了首批令人鼓舞的结果。PONTIAC试验表明,采用抗肾素-血管紧张素和β肾上腺素受体阻滞剂的积极CV保护性药物疗法,可使不复杂的2型糖尿病患者(NT-proBNP水平高于125pg/mL)避免发生不良CV事件。STOP-HF试验表明,对具有一种或以上CV风险因素、血浆BNP浓度高于50pg/mL的患者采取强化监测和定制抗CVD治疗方案,有助于预防心衰和其他不良CV终末器官事件。我们看到了一系列新候选标志物的应用前景。
二、发现新生物标志物的来源
心力衰竭(简称心衰)是心脏结构和功能机械性紊乱的结果,多方面的病理生理学原因都会加剧其发展。心衰的病理生理学恶性循环包括至少六个主要方面:
(1)炎症;
(2)氧化应激;
(3)神经激素激活;
(4)肾功能不全;
(5)心肌细胞损伤和基质重构(图1)。
上述每个信号通路都可能产生和释放生物标志物,本文突出强调了其中某些标志物。心脏机械牵张和神经激素激活的原型标志物是心脏利钠肽。心脏细胞损伤的主要标志物是心肌肌钙蛋白。这些标志物已经用于实践,而且它们(在慢性病和预防策略中)的既定用途和潜在用途确保它们在可预见的将来仍然是最受欢迎的。它们不太可能被替代,但是,如先前所述,我们需要补充标志物。许多种不断演变的CVD的自然病史都涉及持续的炎症和氧化应激以及随之产生的心脏间质纤维化。长期炎症、氧化应激和间质纤维化是许多形式和阶段CVD的关键机制,但是不像心脏损伤或牵张,它们无法通过常规临床应用的标志物进行可靠评估,而且据我们所知,基于标志物对这些病理生理学过程的评估没有经过证实的循证治疗效果。任何能够可靠地反映活动性心脏纤维化和/或累积纤维化率的标志物或组合都将具有巨大的临床价值,并立即受到追捧。
经过充分确认后,这种标志物将被用于:(1)早到晚期慢性病(高血压、心肌病、心脏瓣膜病、中毒性心肌病和所有心衰)的严重程度评估和进展监测;(2)监测新疗法;(3)可能成为实验疗法的治疗性试验的有效替代终点。同样,一旦严格确定了可靠的CV氧化应激和炎症标志物在预后和指导具体治疗反应中的价值,就会有指南指导其用法。新技术可以对任何给定CVD进行广泛的标志物筛查。这包括系统生物学方法或“组学”方法,比如蛋白组学、代谢组学,以及利用大量核酸芯片微阵列筛查microRNA(核糖核酸)和其他非编码RNA等循环核酸,还有选定候选标志物的聚合酶链反应。目前可以检测全血、选定循环细胞类型、血浆、血清或尤其是循环亚组分如细胞外囊泡(包括外泌体)中的标志物。随着我们可以使用的候选标志物范围越来越广,发现强大的新标志物或组合并将其用于改善CVD的监测和管理只是时间问题。
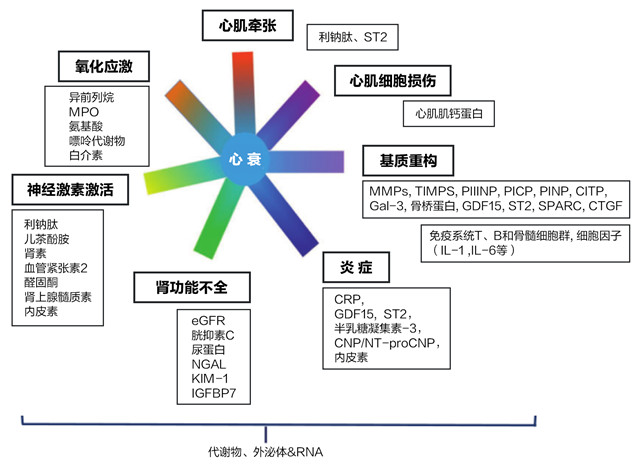
图1. 心衰的病理生理学途径及相关候选循环生物标志物举例
图中心衰的病理生理学途径及相关候选循环生物标志物举例,主要途径在蓝框内用粗体表示。循环生物标志物举例在黑框内用标准字体显示。CNP,C型利钠肽;CTGF,结缔组织生长因子;eGFR,估算肾小球滤过率;GDF15,生长分化因子15;IL,白介素;IGFBP7,胰岛素样生长因子结合蛋白7;KIM-1,肾损伤标志物;MMP,基质金属蛋白酶;MPO,髓过氧化物酶;NGAL,中性粒细胞明胶酶相关脂质运载蛋白;NT-proCNP,氨基末端C型利钠肽前体;PICP,I型前胶原羧基端肽;PINP,I型前胶原氨基端肽;PIIINP,III型前胶原肽;RNA,核糖核酸;SPARC,富含半胱氨酸的酸性分泌蛋白;ST2,白介素1受体样蛋白/致癌抑制因子2;TIMP,金属蛋白酶组织抑制剂。(经过允许,该图改编自Braunwald E. Heart Failure. Figure 7. JACC Heart Failure 2013;1:1-20.)
三、未来最受欢迎的候选心血管生物标志物
1. 肽类和蛋白质:过去5年内多次统计了当下正在研究的不同种类的代表性CV生物标志物,并给读者推荐了一些优秀的综述文章。当前以大量同行评审证据为基础、主要对冠心病和心衰具有预后价值的热点标志物包括ST2、肾上腺髓质中段肽(MR-proADM)、生长分化因子15(GDF15)和半乳糖凝集素-3(Gal-3)。但是与心肌肌钙蛋白或BNP相比,它们在急性冠脉综合征或心衰诊断上均没有优势。有些标志物可提供独立的疾病严重程度和预后信息,但是生物医学界认为还需要进一步评估它们在指导治疗中的作用。考虑到目前的治疗选择,在改善预后方面的临床价值尚不清楚。例如,在急性失代偿性心衰入院后的头30天,MR-proADM只有在能够指导早期改变治疗方案来改善结局的情况下,才能比 NT-proBNP更有生存预后优势。有强有力的证据表明致癌抑制因子2(ST2)不仅在心衰中具有预后价值,而且有助于在仅根据冠状动脉事件发作后24小时内采集样本的结果判断急性冠状动脉综合征之后进行风险分层。我们需要前瞻性的随机试验数据来证明ST2比标准实践更有利于指导增加或增大β肾上腺素受体阻滞剂或其他疗法。我们还需要证据支持在评估呼吸困难患者时,NT-proBNP与降钙素原结果相结合会更好地改善合并肺炎的心衰患者的状况并及早采取有效的抗生素治疗。有很多标志物反映了心室重构和/或心脏纤维化,包括前胶原、胶原降解产物、基质金属蛋白酶(MMP)、金属蛋白酶组织抑制剂(TIMP)、富含半胱氨酸的酸性分泌蛋白(SPARC)、ST2、GDF15、半乳糖凝集素-3和一系列 microRNA。除了两三个标志物,其他标志物与纤维化或累积心脏纤维化率存在密切关系的证据较少(根据组织学或核磁共振评估的心脏细胞外容积)。我们需要更强大的标志物,并提供生物标志物对结局有利影响的证据。氧化应激(异前列烷、嘌呤代谢物和麦角硫因等)或炎症(C反应蛋白=CRP、白介素和其他细胞因子)的表面标志物也存在类似的问题。目前,我们缺乏足够有力的证据表明这些标志物是满足“最受欢迎”条件的成功标志物并把它们用于常规临床实践。
2. 外泌体:循环细胞外囊泡被越来越多地研究其是否可能作为CV生物标志物。这些双层膜囊泡涵盖的颗粒范围很广,包括微粒、微囊泡、外泌体。外泌体由细胞主动产生,含有蛋白质、RNA,可能参与细胞间通讯。它们可能反映来源组织的疾病过程。特定囊泡与LDL颗粒共存(co-fractionate),而其他囊泡则与HDL颗粒分离。因此,可通过连续的LDL和HDL分离来分离不同的血浆细胞外囊泡(EV)亚组分,以鉴定EV蛋白亚群,每个亚群都有自身的蛋白质含量和相关病理生理途径。作为在CVD中起到一定作用的蛋白质工具,血浆EV越来越多地被研究。据报道,循环细胞外囊泡水平与内皮功能障碍之间存在关联,而后者又与后续CV事件有关,Framingham研究显示内皮功能障碍还与心血管代谢风险有关。囊泡计数与心衰(HF)有关。CD144+内皮来源囊泡计数随着纽约心脏协会分级升高而升高。CD31+/膜联蛋白V+囊泡计数与复发性HF相关再入院和死亡有关。近期我们发现,先前认为与系统性血管事件相关的选定细胞外囊泡蛋白(丝氨酸蛋白酶抑制剂F2、丝氨酸蛋白酶抑制剂G1、胱抑素C和CD14)水平也与急性呼吸困难患者存在心衰有关。细胞外囊泡分析提供了一系列全新的潜在标志物,但是这些标志物的临床应用必须有严密的证据支持其所提供的信息能够改善患者管理和临床结局。
3. 代谢物:代谢物与细胞事件存在直接关联,极有可能成为有用的生物标志物。在治疗诱导型心肌梗死中,间隔消融连续采样产生了明确的血浆代谢组学特征。梗死发生后10分钟内,参与嘧啶代谢、三羧酸循环和磷酸戊糖途径的代谢物水平紊乱。这些结果具有特异性和再现性,可以解决高敏心肌肌钙蛋白检测缺乏特异性的问题。需要在疑似AMI患者中进行比较和联合应用肌钙蛋白与代谢物的前瞻性研究。Cheng等人确定了在鉴别心衰患者与对照方面与NT-proBNP性能相当的循环代谢物组合。在HF患者(n=515)和匹配对照队列中进行的发现和确认研究报告了代谢物组合的诊断和预后性能。循环氨基酸(组氨酸、苯丙氨酸和亚精胺)与磷脂酰胆碱C34:4鉴别HF与对照的能力与BNP相当。不对称甲基精氨酸与精氨酸的比值、丁酰肉碱和亚精胺联合必需氨基酸总量提供的HF患者生存预后信息优于BNP(AUC 0.85 vs. 0.74)。随着HF的治疗和控制得到改善,代谢物分析结果趋于正常,这表明连续测量代谢物在抗HF疗法的滴定和慢性HF状态监测中起到一定作用。通过改进的标准化质谱分析,这些简单的基本代谢物在心衰管理方面可展现出高度再现的诊断和预后生物标志物性能。证实的台湾研究结果和代谢物指导治疗滴定策略的成功随机试验无疑使它成为最受欢迎的生物标志物。
4. 循环核酸:循环核酸包括microRNA和循环RNA。对血源microRNA作为生物标志物的研究已进行了十多年,但循环RNA及其他非编码RNA的作用还在初始探索阶段。
Tijsen等人发现HF患者的血浆microRNA(miR-423-5p,-18b,-129-5p,-1254,-675,-202,-622)水平升高,并且强调miR-423-5p作为HF诊断标志物可与BNP相媲美。这组microRNA不同于急性心肌梗死(MI)中升高的microRNA(miR-1,-133,-499,-208)。Wong等人分析了健康对照、135例已接受治疗 HFrEF(EF<40%)和133例已接受治疗HFpEF(EF>50%)患者的血浆microRNA。受试者操作特征曲线分析(AUC>0.65,P<0.001)发现,可以区分HF与对照的82个microRNA具有差异性调节异常。24个microRNA能够区分HFrEF与HFpE,AUC>0.60,P<0.001。选定的microRNA组合加上NT-proBNP提高了对HF与非HF对照的鉴别能力,AUC>0.98。最值得注意的是,在潜在临床应用方面,对于指南所给NT-proBNP临界值产生假阳性和假阴性(主要是HFpEF)心衰诊断结果的案例,microRNA评分能够对其正确地重新归类,准确度在90%以上。这表明microRNA可在综合征的初期、早期或部分治疗阶段识别心衰,尤其是在射血分数保留的情况下,床旁临床评估、影像学和NT-proBNP(作为唯一生物标志物)常常不具备诊断准确度。
在目前已发现的成千上万的人microRNA中,已确定一些microRNA可以作为治疗靶标。例如,我们已证明对抗性miR-31具有心脏保护作用。在实验性心肌梗死和临床心衰中,这种microRNA在心肌和血浆中显著升高。对抗性miR-31在大鼠心肌梗死中显著限制了梗死面积和MI后不良重构,并有益于保留MI后心脏结构和功能。
四、小结
生物标志物对于心脏疾病的合理评估和管理是不可或缺的。已经确定了两个强大的标志物即心脏利钠肽和心肌肌钙蛋白在急性病中的作用,并且它们的适用范围已经扩展到非急性病的长期监测和风险分层了。在很多情况下它们的特异性是不够的,而我们正等待有证据支持的补充标志物出现,以纠正这一缺点。此外,虽然这些值得信赖的标志物提供了可具操作性的心肌细胞牵张、神经激素激活和心肌细胞损伤信息,但是它们并未评估炎症、氧化应激和纤维化等重要的CV病理生理过程。随着有效治疗尤其是针对这些途径的疗法不断改进,我们需要标志物来明确每个过程的程度和活动,以及反映个性化治疗效果,而特定生物标志物在一定程度上也能指导个性化治疗的选择。在对经典循环肽类候选标志物(如ST2、GDF15、MR-proADM和半乳糖凝集素-3)的探索富有成效的同时,我们还在蛋白组学、代谢组学及循环外泌体和核酸筛查方面发现了令人振奋的新标志物。但是,任何受欢迎的标志物都必须经过严密的评估,证明其有助于改善临床结局之后才能进入常规临床实践。





