肠道菌群: 新的心血管疾病生物标志物
作者:Pablo Perez-Martinez等 编译:王小茜
【摘要】心血管疾病(CVD)仍是发达国家的主要死因。导致CVD发生的心血管风险因素(主要是2型糖尿病和肥胖)呈上升趋势。目前以控制传统风险因素为主的预防和治疗管理明显不足以阻止这种疾病的发生。因此,寻找新的CVD生物标志物是大多数临床研究项目的第一要务。由于肠道菌群与心血管及非心血管疾病的关联,其已成为当下的研究热点。本综述重点关注肠道菌群影响CVD的现状,尤其是对血脂、糖尿病、高血压和肥胖等主要CVD传统风险因素的影响。
【关键词】微生物群,肥胖,糖尿病,高血压,血脂代谢,心血管疾病
一、肠道菌群在心血管风险评估中的作用
心血管疾病(CVD)仍是现代社会的主要死因。此外,导致CVD发生的心血管风险因素并没有减少,反而在增加。这不仅具有特别重要的临床意义,而且对全球健康负担造成的社会经济成本也有巨大影响。因此,想要防止这种疾病发生,仅靠控制传统风险因素是不够的。虽然许多二级预防患者的传统风险因素控制较好,但仍会出现新的心血管事件。我们需要预防而不是治疗此类问题,同时还需要寻找能够帮助我们控制CVD的新的中间标志物。另外,由于缺乏有效治疗方法,人们对于有助于明确动脉粥样硬化病理生理学的新通路越来越感兴趣。实际上,近期有证据表明肠道菌群与心血管和心脏代谢疾病如肥胖、代谢综合征(MetS)、高血压和2型糖尿病有关(图1)。
传统上,人类胃肠道被视为接受膳食成分(只是被吸收或代谢)的被动器官。然而,近期研究发现人类胃肠道还是上万亿细菌的家,而且肠道菌群作为内分泌器官发挥着重要作用。事实上,有一种理论认为微生物群落与人类宿主之间的相互作用取决于健康或疾病状态。现在我们很确定人类肠道拥有核心细菌微生物组,主要由拟杆菌和厚壁菌门等类群组成,而较不常见的类群也存在,如变形菌门、放线菌和疣微菌门,但数量较少。肠道菌群与膳食成分相互作用产生功能信号,影响正常的生理学过程,也影响人类宿主的慢性病发展。有趣的是,近期证据表明肠道菌群与膳食相互作用的某些产物可改变炎症和免疫应答,从而影响动脉粥样硬化过程。因而,膳食成分引起的肠道微生物代谢导致促粥样硬化循环因子(影响心血管风险)的产生。实际上,Wang等人证明肠道菌群的卵磷脂代谢对CVD有促进作用。一项包含4000名参与者的临床研究证实了TMAO的产生对人类肠道菌群有依赖性,而且血清TMAO水平可以剂量依赖的方式预测3年内的心血管风险发生率。近期小鼠实验表明这一机制涉及血小板激活,还证明了胃肠道菌群会影响血浆TMAO水平。
另一个证明微生物内分泌学影响心血管风险的例子是短链脂肪酸(SCFAs),包括乙酸、丁酸、丙酸和戊酸,它们是具有类激素特性的肠道菌群代谢物,优于在盲肠和近端结肠中发现的厌氧菌亚组。已证明SCFAs可调节胰岛素敏感度、免疫应答和能量代谢,因此直接影响CVD风险。另外,肠道菌群的脂类代谢决定着动脉粥样硬化的形成。在这方面,已证实肠道菌群导致胆汁酸功能性改变,决定了其与法尼酯X受体或G蛋白偶联胆汁酸受体(TGR5)等潜在受体的结合。总的来说,胆汁酸代谢中的微生物-宿主交叉反应在心脏代谢途径中起关键作用,改变了脂类代谢,因此与CVD风险有关。
最后,不仅细菌代谢物能够充当调节心血管风险的激素,而且细菌细胞壁的成分(主要是卵磷脂和肽聚糖)也可被宿主Toll样受体(TLRs)和含核苷酸寡聚化结构域的受体识别,在炎症增强时会影响CVD的发病机理,还会改变胆固醇逆向转运和增加胰岛素抵抗。因此,我们知道肠道菌群这个内分泌器官能够产生自己的激素和代谢物,与参与不同代谢途径的特异性受体相互作用。此外,已证明肠道菌群代谢产物间接与宿主内分泌系统相互作用,改变重要激素如瘦素、胃饥饿素和皮质醇的功能代谢。因此,肠道微生物组在内分泌系统中发挥核心作用,主要体现在产生自身体液因子以及间接改变经典激素功能的信号。
在过去十年内,无数报告将微生物群与心血管和非心血管疾病相联系。本综述重点关注肠道菌群影响心脏代谢疾病(导致CVD发生)的现状,尤其是对血脂、糖尿病、高血压和肥胖等主要传统风险因素的影响。
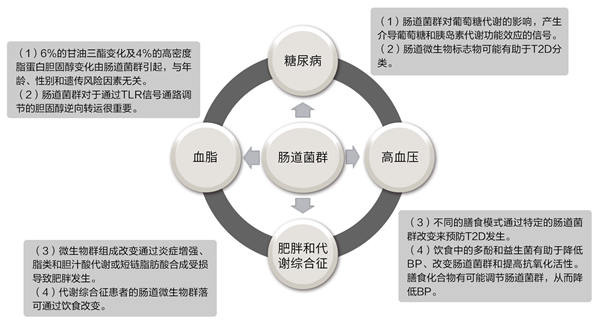
图1. 肠道菌群在心血管风险中的作用。
BP,血压;TRL:Toll样受体;T2D,2型糖尿病
二、肠道菌群对糖尿病的影响
在过去几年内,2型糖尿病(T2D)在全球大爆发,目前已成为最重要的慢性病之一,对公共卫生产生至关重要的影响。由于T2D影响多个机体系统,因此T2D患者更易于发生多种继发性并发症。鉴于T2D具有重要的临床意义及可能导致严重的残疾,现代社会应高度重视T2D预防。
人类肠道菌群与T2D发展之间的关联越来越明确。近期在欧洲和中国两个独立队列中进行的宏基因组关联研究证明了肠道菌群与T2D病理生理学之间的潜在关联。在欧洲人群中,使用鸟枪法测序检测145名欧洲女性的粪便宏基因组,这些女性的血糖正常、葡萄糖耐量减低或被诊断为T2D。观察到T2D患者的宏基因组存在组成性或功能性改变,并且基于能够相当准确鉴别T2D的宏基因组特征设计了一个数学模型。有意思的是,将该模型用于葡萄糖耐量减低的女性时,结果发现它能够鉴别具有类糖尿病代谢的女性。根据这些发现,制定了一项宏基因组关联研究(MGWAS)方案,并执行了两阶段MGWAS,对345名中国人进行肠道菌群DNA深度鸟枪测序。MGWAS分析表明T2D患者具有中度肠道菌群失调,某些普遍的产丁酸盐细菌丰度降低和各种机会性致病菌丰度增加,以及具备硫酸盐还原和抗氧化应激能力的其他微生物功能丰富。对另外23人的分析证明这些肠道微生物标志物可能有助于T2D分类。两组都发现了T2D患者与健康对照之间的宏基因组差异。这两项研究第一次证明了糖尿病患者与正常人之间的宏基因组差异,并且可根据宏基因组序列预测疾病发展。
关于人类肠道菌群与T2D发生之间的关联,有各种机制被证实。比如,血浆TMAO水平(源于膳食营养成分)与动脉粥样硬化血栓疾病如T2D有关。糖尿病小鼠模型证明含黄素单氧化酶3敲除及后续TMAO水平可预防高血糖、高血脂和动脉粥样硬化发生。近期研究发现一种可降解肠道内粘蛋白的细菌(Akkermansia muciniphila)在系统性葡萄糖代谢中发挥关键作用,且在小鼠和人类生理学中作用相似。除了宏基因组关联研究,16SrRNA基因测序在微生物生态学检测中的应用提供了一个完整的技术平台,通过此平台可评估人类微生物群,并探索微生物组与T2D关联所涉及的不同机制。研究证明T2D患者菌群失调,双歧杆菌属(Bifidobacterium spp)和柔嫩梭菌群(Faecalibacterium prausnitzii)数量较低,以与丁酸盐产生相关的抗炎症活性低而闻名。此外,动物模型已证明脂多糖(LPS)(主要源于富含饱和脂肪的饮食)会导致代谢性内毒素血症,这种病症在T2D患者的炎症状态中发挥关键作用。微生物群与饮食相互作用也会产生LPS,结果就是产生大量与胰岛素抵抗有关的炎症细胞因子,如TLR4、TNF-α和IL-6。之前肠道菌群影响葡萄糖代谢的其他潜在机制也被证实了。
总而言之,基因组、生物学、临床和实验方法均证明了T2D患者的肠道菌群有所改变,至少不同于葡萄糖代谢未改变的正常人。另外,肠道菌群对葡萄糖代谢的影响是明确的,主要是产生介导葡萄糖和胰岛素代谢功能效应的信号。
三、肠道菌群对高血压的影响
没有人会否认血压(BP)是最重要的心血管风险因素之一。目前在发达国家,约3亿3千万人患有高血压。在发展中国家,这个数字约为6亿4千万。世界卫生组织认为高血压是全球过早死亡的最重要原因之一,而且这个问题越来越严重。预计到2025年,将有15亿6千万成人受高BP的影响。
BP调节是最复杂的生理机能之一,取决于诸多系统如心血管、肾脏、神经和内分泌系统的联合作用。然而,饮食对于控制血压具有重要的作用。肠道及其微生物群则是这些系统与饮食相互作用的重要场所。实际上,已证明膳食化合物可能会调节肠道菌群,从而升高或降低BP。有趣的是,研究证明通过膳食补充的多酚有助于通过改变肠道菌群和提高抗氧化活性来降低BP。
此外,近期研究表明高血压与肠道病理生理学改变有关。因而,Santisteban等人检验了以下假设:肠道交感神经激动增加与炎症状态增强和菌群失调有关,而且肠道的这些病理学改变与高血压有关。大鼠模型证明血压升高与可控制BP的微生物菌群改变有关。他们得出结论,交感神经-肠道通讯障碍与肠道菌群失调和炎症有关,并且在高血压中起关键作用。
总之,众所周知肠道菌群失调与严重的慢性病有关。近期证据表明高血压与肠道功能改变、肠道菌群改变和肠道-神经系统连接性改变有关。然而,需要进一步研究来更好地了解高血压与微生物群之间的关联。
四、肠道菌群对肥胖的影响
全球约17亿人超重,其中最显著的是发达国家。T2D的急剧增加与发达国家超重和肥胖的增加密不可分,这可能是由于生活方式的重大改变。饮食是与定居肠道菌群相互作用并影响肥胖发展的最重要环境因素。因此,大家对肠道菌群与肥胖之间的关系越来越感兴趣,以便更好地了解肥胖的病理生理学和确定新的预防及治疗方法。微生物群组成的改变可通过多种机制促进肥胖发展,例如炎症增强、脂类和胆汁酸代谢,从而增加从饮食中获得的能量或损害短链脂肪酸的合成。肠道菌群作为一个整体在宿主新陈代谢中充当完整的器官,可通过在特定饮食后进行长期饮食干预来塑造。我们最近研究了肥胖人群在采用地中海饮食(Med饮食)或低脂、高复杂碳水化合物饮食(LFHCC饮食)1年后微生物群的变化。结果表明长期采用Med和LFHCC饮食可通过对肠道菌群进行不同的特定改变,分别增加罗氏菌属(Roseburia)和普拉梭菌(F. prausnitzii)的丰度,从而避免胰岛素抵抗。我们先前证明了饮食可改变代谢综合征患者的肠道微生物群。
最后,研究表明饮食、年龄、激素以及性别(很大程度上未被探索)对人类肠道菌群的影响存在很大的个体间异质性。我们旨在根据性别和体重指数(BMI)鉴别与肥胖有关的差异性肠道菌群特征。使用16S测序分析了39例男性和36例绝经期女性的菌群结构差异,这些人具有相似的饮食背景并且年龄和BMI分层相匹配。我们观察到BMI>33时,男性的拟杆菌属丰度低于女性。另外,我们观察到男性粪便样本中的韦永氏球菌属(Veillonella)和甲烷短杆菌属(Methanobrevibacter)高于女性。我们还观察到男性的嗜胆菌属(Bilophila)丰度低于女性,无论BMI如何。经过年龄和性别纠正后,发现66种细菌类群(属水平)与BMI和血脂有关。31%的BMI变化、29%的甘油三酯变化、33%的高密度脂蛋白变化、46%的低密度脂蛋白变化和28%的总胆固醇变化由微生物群引起。我们的结果表明男性与女性的肠道菌群不同,而且这些差异可能受肥胖程度的影响。
五、肠道菌群对脂类代谢的影响
如同上述讨论的所有其他心血管风险因素,肠道微生物组也是引起血脂变化的主要原因。在此背景下,Fu等人鉴别出了其比例与血脂水平有关的肠道细菌类群,并调查了是否可以用与年龄、性别和宿主遗传学有关的微生物群来解释血脂变化。对LifeLines-DEEP队列的893位受试者进行研究:经过年龄和性别纠正后,发现了与BMI和血脂相关的34种细菌类群,其中大多数关联是新发现的。结果表明6%的甘油三酯变化和4%的高密度脂蛋白变化由微生物群引起,与年龄、性别和遗传风险因素无关。包含肠道微生物组的新风险模型解释了高达25.9%的HDL变异,显著优于未包含微生物组的风险模型。
这些结果可能涉及的机制与TLR信号通路调节胆固醇代谢及肠道菌群可能是胆固醇逆向转运(RCT)的重要因素有关。胆固醇从血管壁流向巨噬细胞是RCT预防动脉粥样硬化的第一步。肝X受体(LXRs)是控制胆固醇代谢并在结合内源性羟固醇(oxysterols)时被活化的核受体。已知LXR激动剂可上调ATP结合盒转运体A1和G1的表达,从而导致RCT增加。另外,TLR4可能通过髓性分化初级反应蛋白88(MyD88)非依赖途经抑制LXRs活化。近期证明TLR2和TLR4作为载脂蛋白A-I对于RCT是必不可少的,但对于高密度脂蛋白则不是必需的,并且利用了MyD88依赖信号通路。肠道菌群影响血脂代谢的另一个可能机制是通过乙酸、丁酸、丙酸和戊酸等SCFAs实现的。这些代谢物可发挥局部作用并充当能量源,但也可以被吸收和刺激糖原异生或影响胰岛素敏感度。最后,高水平TMAO通过改变RCT、固醇代谢和胆汁酸质量及数量作用于血脂代谢。
总体来说,在人类胃肠道观察到的这些结果和肠道菌群活动研究发现了决定胆固醇稳态的可识别生理学信号。
六、未来研究方向
在目前的临床实践中,有两个概念是明确的。第一,心血管疾病仍然是发达国家发病率和死亡率的主要原因;第二,导致CVD发生的心血管风险因素并没有减少,反而在增加。目前以控制传统风险因素为主的预防和治疗管理明显不足以预防这种疾病发生,因此了解发病过程可能涉及的控制机制非常重要。
更好地了解遗传因素和进行复杂的基因型-表型相互作用研究后,我们对个体间心脏代谢风险因素差异有了更多的认识。然而,了解其他关键因素对代谢的影响机制有助于当下的心血管疾病预防和治疗。在这方面,有足够的证据表明微生物群是影响心血管风险的新因素。不同的膳食成分与微生物群的首次接触决定了最终的表型,也会使我们的机体产生许多不同的后果。但是,为了避免目前不断增长的证据库产生更大的偏差,未来我们应该达成一个共识。因此,尽管已经清楚确立了这一复杂知识的基础,但如果要实现为肠道菌群和代谢紊乱设计真正有效的营养和药理疗法的最终目标,则必须有强有力且明确的基础。
如同环境与基因相互作用的新领域,未来必须考虑以下事项:
1. 重复研究(replication study):证明研究结论之间的一致性,主要是在膳食干预研究中研究营养与微生物群之间的相互作用。
2. 大样本量和种族多样化:这是肠道菌群的另一个重大局限。样本量和种族不同,结论大相径庭。另外,大量证据来自于实验动物研究。
3. 鉴别调节肠壁与微生物组之间关系的机制。
4. 不仅鉴别微生物学模式,还要鉴别微生物学功能。
5. 将分子和实验知识转化到临床实践中。
6. 研究如何调节和有效控制微生物组。
7. 使可影响最终结果的潜在混杂因素均一化,如性别、年龄、体重指数、吸烟和饮食。
8. 不仅调查饮食与微生物组的相互作用,还有其他潜在治疗如抗生素、益生菌或益生元以及粪便移植的作用。
9. 最后,寻找可用于临床实践的简单风险模式鉴别方法。
七、结论
已有充分的证据表明,肠道菌群是新的CVD标志物。已证明肠道菌群是代谢紊乱发生率不断升高的重要决定因素,因此了解微生物群稳态是未来预防和治疗管理需要关注的问题。
在过去几年内,我们发现了肠道微生物组反应可通过饮食来改变,但是这种反应高度复杂,并且个体间差异性较大。现在是时候巩固所有现有证据了。另外,此类研究可能有助于鉴别膳食成分影响肠道微生物组反应的机制,还有利于发现存在代谢紊乱风险的对象并为其提供预防措施或适当的个性化饮食干预。





