胶乳增强免疫比浊法快速检测血液中糖化血红蛋白方法的建立
【摘要】目的:建立一种使用胶乳增强免疫比浊法快速定量检测全血中糖化血红蛋白(HbA1c)含量的方法。方法:样本中总Hb与Hb抗体修饰的胶乳微球结合形成Hb抗体修饰微球-Hb(含HbA1c)复合物,体系吸光度变化值与总Hb呈正相关;往体系中加入HbA1c的单克隆抗体后,形成胶乳-HbA1c-鼠抗人HbA1c单克隆抗体的复合物,此复合物与试剂中的羊抗鼠IgG抗体反应形成凝集,凝集程度与样本中HbA1c的含量呈正相关。结果:该方法获得检测结果的时间不超过10min,操作简单,建立了HbA1c检测的标准曲线,最低检出限为1.5%,检测范围为2.0%~17.0%。结论:该方法与商业化试剂盒相关性良好,降低了检测成本,可以满足临床检测的要求,具有良好的应用前景。
【关键词】胶乳增强免疫比浊;HbA1c;免疫复合物
成人的血红蛋白(Hb)通常由HbA(97%)、HbA2(2.5%)和HbF(0.5%)组成。HbA又可分为非糖化血红蛋白,即天然血红蛋白HbA0(94%)和HbA1(6%)。根据糖化位点以及反应参与物的不同,HbA1可进一步分为HbA1a、HbA1b、HbA1c等亚分组。其中A1c(Hemoglobin A1c,HbA1c)占HbA1的80%,化学结构为具有特定六肽结构的血红蛋白分子[1]。HbA1c 是血红蛋白在高血糖的作用下发生缓慢连续的非酶促糖化反应的产物。葡萄糖在血红蛋白β链N-末端缬氨基酸残基特异性地修饰血红蛋白形成糖化血红蛋白。正常生理条件下非酶促糖化反应产物的生成量与反应物的浓度呈正比。由于蛋白质浓度保持相对稳定,糖化水平主要取决于葡萄糖浓度,也与蛋白质和葡萄糖接触时间长短有关。因此糖化血红蛋白是反映病人2-3个月的血糖平均水平的一个很好的指标。
胶乳增强免疫比浊法(Latex particle-enhanced turbidimetric immunoassay,LETIA),即是将待测物的抗体包被于胶乳颗粒上,增大了抗原抗体反应复合物的体积,光通过之后,透射光和散射光的强度变化更为显著,从而提高检测的灵敏度。相对传统的免疫比浊方法,LETIA具有检测范围更广泛、临床检测的灵敏度更高等优势,大大促进了免疫比浊法在临床上的广泛应用[2-3]。
临床中对于糖化血红蛋白检测的方法主要是酶法、离子层析法、金标免疫渗滤法等。酶法在过氧化物酶的作用下氧化色原底物而呈色,进行比色法测定,灵敏度与专一性比免疫比浊法低;离子层析法精密度高、重复性好,被临床广泛采用,但该方法检测成本相对较高;金标免疫渗滤法,操作较简便,但是精密度、灵敏度相对较差[4-5]。因此建立一种操作简便、价格低廉的糖化血红蛋白检测方法具有十分重要的意义。
本研究建立了胶乳增强免疫比浊法直接测定总Hb中HbA1c的百分含量的方法。样本中总Hb和HbA1c与抗体修饰的胶乳微球有相同的反应性而固相化,当加入HbA1c的特异性单克隆抗体后形成胶乳-HbA1c-鼠抗人HbA1c单克隆抗体的复合物,此复合物与试剂中羊抗鼠IgG抗体反应而形成凝集,凝集量与样本中HbA1c的量呈正相关。
一、研究材料与研究方法
1. 仪器与试剂:日立7180全自动生化分析仪购自日立集团有限公司;羧基乳胶微球(200nm,固含:10%)购自苏州为度生物技术有限公司;兔抗人Hb抗体、羊抗鼠IgG抗体、鼠抗人HbA1c单克隆抗体购自上海罗氏制药有限公司;糖化血红蛋白标准品购自中国计量科学研究院;甘氨酸、N-羟基琥珀酰亚胺(NHS)、EDC(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)购自国药集团化学试剂有限公司;糖化血红蛋白校准品、质控品购自上海捷门生物技术有限公司;实验用水均为超纯水,其他未提及试剂均为分析纯。试剂的配制:
(1)甘氨酸缓冲液60mmol/L:称取4.5g甘氨酸,使用900mL超纯水溶解,调节pH至7.6,定容至1L;
(2)总Hb检测试剂:取固含10%抗体修饰的胶乳微球颗粒1mL于10mL甘氨酸缓冲液中,4℃冷藏保存;
(3)羊抗鼠IgG抗体溶液:使用甘氨酸缓冲液(60mmol/L)稀释至0.3%;
(4)鼠抗人HbA1c单克隆抗体溶液:使用甘氨酸缓冲液(60mmol/L)稀释至0.32%;
(5)NHS溶液的配制:称取NHS 3mg使用超纯水稀释至100μL(现配现用);
(6)EDC溶液的配制:称取EDC 2mg使用超纯水稀释至100μL(现配现用);
(7)微球稀释液的配制:PBS+甘油5%+聚乙二醇6000加0.1%+BSA3%加入超纯水中搅拌均匀;
(8)R1\R2稀释液的配制:Tris+HCl调PH+叠氮钠0.5%+吐温1%加入超纯水中搅拌均匀。
2. 样本前处理:用抗凝管采集的新鲜全血,取样20μL,加1mL溶血素或水溶血,备用。溶血后的样本低温避光在4℃可保存10天。
3. 乳胶微球的修饰:取胶乳微球1mL于5mL离心管中,加入1mL PBS缓冲液,置于37℃恒温箱中震荡10min;加入30mg/mL NHS溶液50μL,加入20mg/mL EDC溶液50μL,搅拌30分钟后,加入100μg Hb抗体,于37℃恒温箱中震荡反应2h,加入10μL乙二胺(1%的溶液现用现配),终止反应1.5h,于10000rpm离心15min,弃上清液,加入2mL微球稀释液振荡重悬,于功率45%超声15-30min,使微球分散开。使用R1\R2稀释液稀释至5mL,备用。
4. 免疫检测流程:免疫反应流程如图1所示,取6μL前处理完毕的样本或者HbA1c校准品于1cm比色杯中,在37℃下加入 R1试剂225μL,孵育5min,于660nm测定吸光值A1;加入试剂R2 75μL,孵育3min,于660nm测定吸光值A2;计算△A=A2-A1,△A的值于血液中HbA1c的百分含量呈相关性。将检测值代入建立的标准曲线即可测得样本中HbA1c的百分含量[6-7]。
二、研究结果与讨论
标准曲线的建立:分别测定2.0、5.6、7.4、11.6、14.0%浓度HbA1c的校准品,建立标准曲线,如图2所示。试剂线性在[2.0%,14.0%]标准曲线的相关系数大于0.99,说明线性关系良好,可以用于临床样本的定量检测。测定值的3倍标准偏差确定方法的最低检出限,该方法的最低检出限为1.5%。
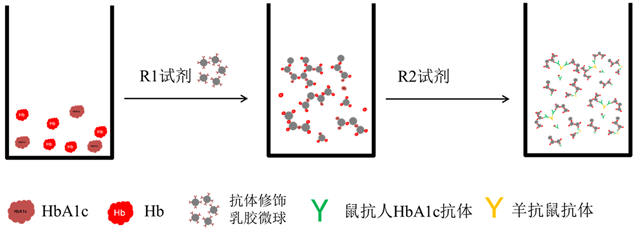
图1. 免疫反应流程
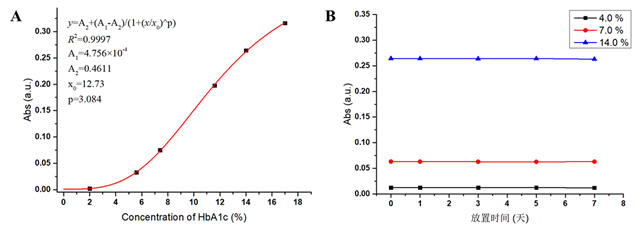
图2. HbA1c检测标准曲线(A)和试剂稳定性(B)
2. 稳定性:将检测试剂置于37℃恒温箱中放置一段时间,考察试剂在检测4.0、7.0、14% HbA1c浓度时的检测性能,如图2所示,在37℃放置7天后,试剂的检测性能仍能保持良好的状态,说明检测试剂的稳定性良好。
3. 特异性:在HbA1c含量11.6%样本中分别加入胆红素40mg/dL、氨基甲酰化Hb7.5mmol/L、乙酰化Hb 5.0mmol/L、乳糜微粒200NTU、抗坏血酸50mg/dL,测试干扰物质对检测试剂的影响,如图3A所示,干扰物质的加入未对检测带来明显影响。
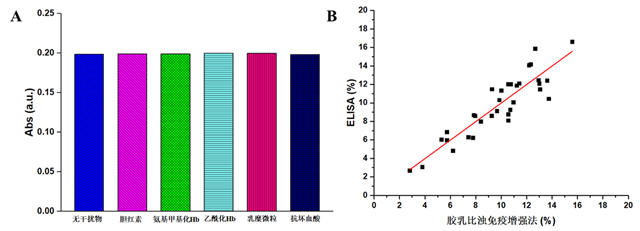
图3. 试剂的特异性(A)和方法学对比(B)
4. 实际人血样检测方法学对比:利用开发的胶乳增强免疫比浊试剂,检测了33份的临床血液样本,将这些样本的检测结果与酶标试剂盒的测试结果进行比对,如图3B所示。两者的相关系数R2=0.90,说明两者测试结果一致,系统之间相关性良好。
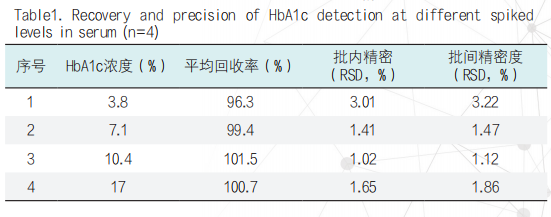
5. 回收率和精密度:考察了该检测方法在HbA1c水平为3.8、7.1、10.4、17%时的回收率和批内及批间精密度,如表1所示,平均回收率为96.3%~101.5%,批内变异系数及批间变异系数均小于4%,说明此方法检测HbA1c具有良好的精密度和重现性。
表1. HbA1c检测的回收率、批内和批间精密度(n=4)
三、结论
本研究开发的胶乳增强免疫比浊法测定血液中的糖化血红蛋白检测试剂盒各项性能良好,且用标准物质检测偏差小于1%。与ELISA等检测方法相比较,该检测方法用时更短,操作更简便。在临床上,胶乳增强免疫比浊法的试剂准确度更高,结果更可靠,因此,该方法具有良好的临床应用前景。
参考文献
尚红, 王毓三, 申子瑜. 全国临床检验操作规程, 2015, 1(3): 234-237.
《生物化学检验》, 2010年7月第3版, 人民卫生出版社
《临床生物化学和生物化学检验》, 2006年6月第3版, 人民卫生出版社
《临床生物化学和生物化学检验实验指导》, 2003年3月第2版, 钱士匀主编, 人民卫生出版社
《临床化学方法学评价》, 1996年6月第1版, 兰州大学出版社
GB/T 26124—2011临床化学体外诊断试剂(盒)
YY/T 1605-2018 糖化血红蛋白测定试剂盒(胶乳免疫比浊法)





