多重荧光PCR毛细电泳片段分析技术研究与临床应用

吴勇,博士、教授级高工,宁波海尔施基因科技有限公司首席技术官。中国医药生物技术协会生物诊断技术分会常务委员,浙江省特聘专家。北京大学生物学系理学学士;中科院上海植生所理学硕士;美国佛罗里达大学细胞及分子生物学博士。曾在美国贝克曼库尔特有限公司就职8年,主持开发出了多款分子检测产品。2011年回国加盟海尔施集团主持开发分子诊断产品,至今已有5款多重基因产品获得NMPA三类注册证。共发表SCI论文30余篇,已获得中国专利局及美国专利局授权的发明专利29项。
21世纪,全球仍然面临着重大公共卫生威胁,尤其在新型冠状病毒流行背景下,病原体的混合感染会导致高发病率和高死亡率,危害程度严重,控制难度极大。因此对一系列致病微生物进行鉴别诊断,是对传染性疾病疫情防御和精准治疗工作的前提。本文介绍一种新的多重荧光PCR毛细电泳技术及其应用情况。
一、多重荧光PCR毛细电泳片段分析的技术原理
多重PCR(multiplex PCR)是在普通PCR基础上加以改进,在同一个PCR反应体系中加入多对引物,同时检测多个目的基因的表达情况[1]。该技术已被广泛地应用于基因检测的多个领域,如基因突变和多态性检测、基因缺失分析、定量分析、RT-PCR检测等[2]。
对PCR产物的分析,传统的分析方法建立在凝胶电泳基础上,利用片段大小及电荷不同对核酸进行分离和分析,虽然成本较低,但操作繁琐、精确度差。新一代基因片段分析通过将多重荧光PCR(图1A)和毛细管电泳分离技术(图1B)巧妙的结合,可在一个反应中同时对多种PCR产物进行定量分析[3]。具体来讲,同一个PCR反应体系中包含多对引物(每一个靶点的其中一个引物上,5’端含荧光标记),各引物特异性地结合相应的目的基因,扩增产生不同长度的片段;通过毛细电泳系统对不同片段长度的PCR产物进行分离和识别,从而对病原体进行鉴别检测(图2)。
注:针对各病原体和内参的基因序列设计不同的特异性引物,并对整个引物扩增体系进行优化,确保每一组引物只能特异性扩增一种病原体或内参(每一个靶点的其中一个引物上,5’端含荧光标记)。在反转录阶段中,由特异性反向引物与相应模板RNA结合进行反转录,得到反转录产物(cDNA)。在PCR扩增反应阶段中,特异性的正向引物和反向引物以DNA或cDNA为模板进行多模板扩增进而产生大量的PCR产物,不同靶点的PCR产物长度不同。

图1A. 多重荧光PCR扩增过程原理图
多重荧光PCR毛细电泳片段分析的特点主要包括:(1)高效性,可以在一个反应中同时检测5-40个靶点,可检测到低至20个拷贝的单碱基差异的核酸序列;(2)系统性,多重荧光PCR非常适用于成组的病原体检测,如病原体的多种型别或混合感染。(3)经济性,在同一反应管内同时检测多种病原体,节省人力物力,为患者节约开支,并为临床提供更全面更准确的诊断信息。由于多重荧光PCR毛细电泳片段分析技术可以实现多种病原体的快速鉴别,既能提高检测通量,又能降低检测成本,因此适合推广使用[4]。
注:PCR扩增产物经过毛细电泳分离,将不同片段大小的PCR产物进行分离,通过对不同长度靶向DNA片段的识别从而判断病原体类型。
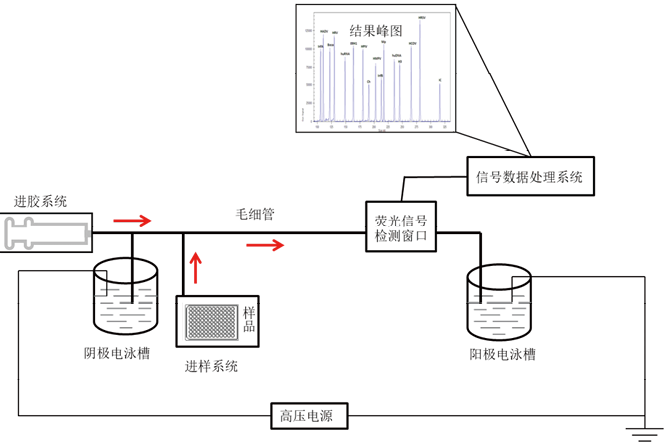
图1B. 毛细电泳过程原理图
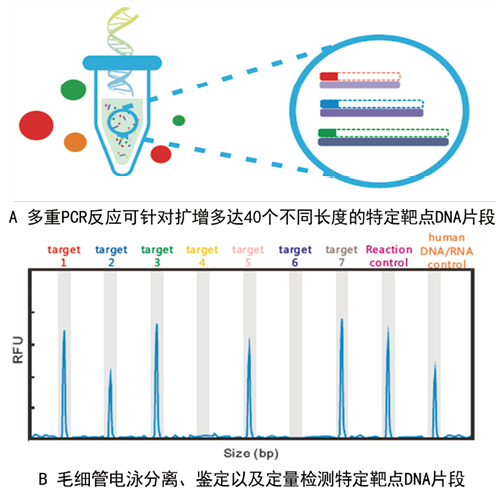
图2. 多重荧光PCR毛细电泳片段分析结果示意图
二、多重荧光PCR毛细电泳片段分析技术临床应用及评价
王乐等人报道了一种多重荧光PCR毛细电泳片段分析方法,可在一个反应中同时检测20种呼吸道常见病毒,且无交叉反应,特异性较好。各位点平均500拷贝/μL时可同时特异地检测出所有病毒,部分病毒的检出限<10拷贝/μL,灵敏度较高[5]。文章也比较了毛细电泳片段分析法和qPCR法的临床阳性样本检出率,结果发现与毛细电泳片段分析法相比,qPCR法对于混合感染样本更容易出现漏检情况,而毛细电泳法的病原体检出率更高。
张海邻等的研究发现多重荧光PCR毛细电泳片段方法具有比直接免疫荧光法更高的灵敏度(58.37% vs 41.53%)[6]。Wei等人比较了毛细电泳片段分析法(SureX HPV test)和qPCR方法(Cobas 4800 test和Venus HPV test)对临床样本的检测效果,结果表明与qPCR方法相比,毛细电泳片段分析法对临床样本检测的假阳性和假阴性率更低[7]。这可能是因为,qPCR反应的前15-20个循环的荧光信号作为荧光本底信号,意味着此循环数内的信号都被掩盖,且反应管中探针水解释放的荧光背景,也对灵敏度造成影响。而基于毛细电泳的多重荧光PCR方法,多余的荧光可在毛细电泳过程中被分离,因此不存在荧光信号干扰的问题,更容易检测到qPCR基线下方的区域。在进行相同样本检测时,多重荧光PCR毛细电泳片段分析法需要的扩增循环数更低(图3)。
Li等[8]对比该方法与液态芯片技术对于临床样本检测的效果,结果表明,无论在单一病原感染还是多病原感染的病原学诊断方面,多重荧光PCR毛细电泳片段分析法的灵敏度和特异度均较高。研究人员也对可能的原因进行了探讨,一方面,两种技术前期都要经过多重PCR扩增,引物二聚体在PCR产物中的比例较高,这会影响芯片杂交的效率。但在多重荧光PCR毛细电泳片段分析中,引物二聚体片段较短,出峰时间较早,不会对后续特征峰造成干扰。另一方面,基于毛细电泳的多重PCR方法分辨力极高,甚至相差1bp的DNA片段都能分开,且发生等位基因突变时,出峰位置也会有时间差别,检测的特异性较高。同时,多重PCR片段分析法通过不同长度引物的设计组合能明显看出杂峰的出峰位置,方便对体系进行优化。
注:图中3条曲线分别代表三个样本的qPCR反应曲线,以灵敏度较高的Ct值为29的样本为例,qPCR方法在29个扩增循环数时可检测到该样本,而多重荧光PCR毛细电泳片段分析法只需要25个循环数即可检测到该样本。Ct值(threshold):qPCR反应中,每个反应管内的荧光信号到达设定阈值时所经历的循环数。基线(baseline):在PCR扩增的最初几个循环数里,荧光信号变化不大,接近一条直线。
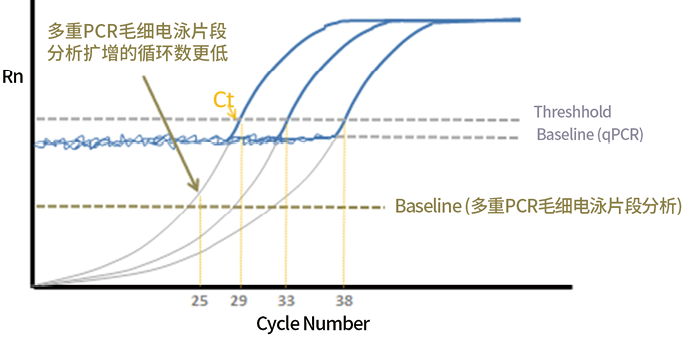
图3. 多重荧光PCR毛细电泳片段分析法的信噪比分析
多重荧光PCR毛细电泳片段分析技术以其具有灵敏度和特异性高、通量高、重复性好等优势,已被应用于多个研究领域,包括肿瘤的风险评估、遗传病筛查、多种心脑血管和血液病的诊断等[9],其中,该技术在病原学检测中,由于能放大检测同一个样本里的多种病原,因而在临床应用中受到广泛关注。
孟俊等通过多重荧光PCR毛细电泳片段方法对9457例妇女的宫颈脱落细胞进行HPV基因分型检测,结果发现,总感染率为14.36%(1358/9457),其中多型别感染占19.81%,部分患者甚至是三重感染甚至五重感染,为宫颈癌的预防、筛查、诊治及随访提供重要的依据[10]。刘宇奇等[11]通过多重荧光PCR毛细电泳片段分析方法对长春地区儿童呼吸道感染病进行流行病学分析,结果表明,13种呼吸道病原检测的灵敏度、特异度、阳性预测值、阴性预测值分别达到97.31%、100%、100%和99.85%,且整个试验过程耗时短、时效性好(4h之内最多可完成192例样本检测)、检测项目全面,涵盖儿童呼吸道感染常见的病毒,满足大规模样本的多病原检测,为呼吸道感染病原学诊治提供科学依据。
三、展望
自新冠疫情以来,对呼吸道病原体的鉴别诊断愈来愈受到重视。一项对武汉地区8274例受检者的新型冠状病毒检测及其合并感染的结果分析中,新冠阳性组中其他呼吸道感染阳性率为5.77%,新冠阴性组中其他呼吸道感染阳性率为18.39%[12]。国家卫健委印发的《新型冠状病毒肺炎诊疗方案(试行第八版)(国卫办医函〔2020〕680号)》指出:“新冠肺炎主要与其他已知病毒性肺炎及肺炎支原体感染鉴别,尤其是对疑似病例要尽可能采取包括快速抗原检测和多重荧光PCR核酸检测等方法,对常见呼吸道疾病进行检测”。因此,加强病原体鉴别诊断技术的研究,提高对病原微生物检测的能力,发展能同时检测数十种病原体的检测技术,是防控工作的重要一环。针对病原微生物设计多重荧光PCR毛细电泳片段分析体系,对病原体检测具有较高的灵敏度和特异性[4, 13],而且该技术易于普及,不断地推广应用,将会对新发传染病的防治带来好处[14]。
参考文献
J S Chamberlain, R A Gibbs, et al. Deletion screening of the Duchenne muscular dystrophy locus via multiplex DNA amplification [J]. Nucleic Acids Res. 1988 Dec 9; 16(23): 11141-56.
P Markoulatos, N Siafakas, et al. Multiplex Polymerase Chain Reaction: A Practical Approach [J]. J Clin Lab Anal. 2002; 16(1): 47-51.
Alex J Rai, Rashmi M Kamath, et al. Analytical validation of the GeXP analyzer and design of a workflow for cancer-biomarker discovery using multiplexed gene-expression profiling. Anal Bioanal Chem. 2009 Mar; 393(5): 1505-11.
M Hindiyeh, D R Hillyard, K C Carroll. evaluation of the Prodesse Hexaplex multiplex PCR assay for direct detection of seven respiratory viruses in clinical specimens[J]. Am J Clin Pathol. 2001 Aug; 116(2): 218-224.
王乐, 赵梦川, 石仲仁,等. GeXP多重RT-PCR技术在儿童呼吸系统病毒感染病原体检测中的应用[J]. 中华检验医学杂志, 2015, 38(12) : 852-856.
张海邻, 陈小芳, 吕芳芳, 等. 多重 PCR 技术检测儿童下呼吸道感染病毒和不典型病原体的价值[J]. 温州医科大学学报, 2017, 47(11): 791-795.
Baojun Wei, Ping Mei, Shengkai Huang, et al. evaluation of the SureX HPV Genotyping Test for the Detection of High-Risk HPV in Cervical Cancer Screening[J]. Virol J. 2020 Nov 9;17(1):171.
Xue Li, Bo Chen, Shaoya Zhang, et al. Rapid Detection of Respiratory Pathogens for Community-Acquired Pneumonia by Capillary Electrophoresis-based Multiplex PCR[J]. SLAS Technol. 2019 Feb; 24(1): 105-116.
医疗机构临床检验项目目录, 2013年版
孟俊, 金丽兰, 林琳. 9457例妇女人乳头瘤病毒感染情况分析[J]. 国际检验医学杂志, 2018, 39(A02): 5.
刘宇奇, 黄艳智, 孙利伟,等. 基于毛细管电泳多重PCR方法对小儿呼吸道感染病原分析[J]. 中国小儿急救医学, 2019, 26(10): 764-770.
汪明, 吴青, 徐万洲,等. 武汉地区 8 274 例受检者新型冠状病毒核酸检测及合并感染结果分析[J]. 中华检验医学杂志, 2020, 43(4): 341-345.
薛梦星, 仇惠英, 冯宇峰,等. 多重PCR结合毛细管电泳检测FLT3及NPM1基因突变的实验方法的研究[J]. 中国血液流变学杂志, 2011, 21(4): 569-572.
蒋露晰, 任红宇, 周海健, 等. 社区获得性肺炎病原体检测方法研究进展[J]. 中华流行病学杂志, 2016, 37(7):1051-1054.




