呼吸道传染病病原体快速检测新技术与研究开发重点

王升启,军事科学院军事医学研究院研究员、军事科学院首席专家。主要从事传染病分子诊断与治疗研究。曾获国家杰出青年基金和“求是”杰出青年奖、吴阶平医药创新奖,是首批国家新世纪百千万人才、原总后勤部“科技金星”、全国优秀科技工作者,荣立二等功3次。兼任全军传染病分子诊断新技术重点实验室主任、核酸药物国家地方联合工程研究中心主任、生物芯片北京国家工程研究中心副主任。以第一完成人获国家技术发明二等奖1项、国家科技进步二等奖1项、省部级一等奖4项;获授权发明专利23项;获我国第一个自主研发的反义核酸1类新药临床研究批件;获医疗器械注册证65项(国家25项,军队40项),多项为首次获批;在Nat Microbiol、Nucleic Acid Res和Gut等国际期刊发表SCI论文160余篇。
呼吸道传染病严重危害人类健康,是全球面临的重大公共卫生问题,且新突发传染病多为呼吸道传播,如2003年暴发的严重急性呼吸综合征冠状病毒(SARS-CoV)、2009年暴发的甲型H1N1流感病毒、2013年暴发的人感染高致病性H7N9禽流感病毒、55型腺病毒及2019年暴发的新型冠状病毒(2019-nCoV)感染等,对全球公共卫生和经济发展构成了巨大威胁。
病原体检测和确证是呼吸道传染病疫情防控的首要环节,可阻断传播、避免恐慌,发挥“雷达”和“准星”的作用。新型冠状病毒肺炎(简称“新冠”)疫情中,早发现、早报告、早隔离、早治疗的“四早”策略是防控的重要手段,其中,快速、准确的病原体检测是“早发现”的前提,是采取有效隔离措施、防止疫情蔓延的关键。目前常用的检测方法有基于检测病原体特异性基因的核酸检测技术、基于检测病原体抗原或抗体的免疫检测技术等,不同的技术各有优势。本文主要对近年来呼吸道传染病病原体检测新技术及其应用、相关检测产品研发等进展情况和关键问题进行讨论。
一、病原体核酸检测新技术
基于核酸扩增的技术具有灵敏、特异、快速等突出优点,被广泛用于病原体检测和临床疾病诊断。目前最常用的核酸检测技术为聚合酶链式反应(PCR)、等温扩增技术、基因芯片技术等。本部分针对近年来呼吸道病原体核酸检测技术领域的新进展进行回顾和综述。
1. 双链基因探针实时荧光PCR:实时荧光PCR是目前国际公认的病原体检测应用最广泛和稳定的分子检测技术,在呼吸道传染病病原体实验室确证中具有不可替代的地位和作用。如获批国家注册证的新冠病毒核酸检测产品中,90%以上采用的是实时荧光PCR技术。探针是实时荧光PCR技术的核心,根据荧光探针结构的不同,可分为以下几种:水解探针(hydrolysis probes)[1]、分子信标探针(molecular beacon,MB)[2]、杂交探针(hybridization probe)[3]、蝎型探针(scorpion)[4]及复合基因探针(complex probe)[5-6]等,其中,复合基因探针具有荧光具有背景低、灵敏度高的突出优势。
复合基因探针[6]结合了分子信标和杂交探针的优点,由荧光探针和淬灭探针2条探针组成,荧光探针长25个碱基左右,5'端标记荧光基团,3'端磷酸化防止被延伸;淬灭探针长15个碱基左右,3'端标记淬灭基团。2链杂交时形成荧光共振能量传递(fluorescence resonance energy transfer,FRET),无荧光信号;当有特异模板被扩增时,由于荧光探针与模板完全互补,形成的杂交比与淬灭链杂交更稳定,FRET作用消失,发出较强荧光(图1)。复合基因探针特异性、灵敏度较高,可以用来鉴别单碱基突变。
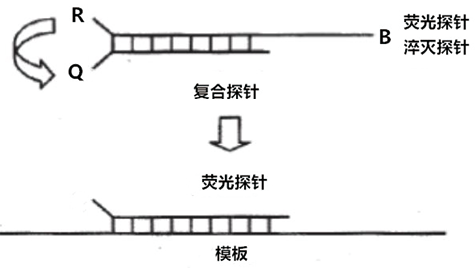
图1. 复合基因探针的原理图
在复合基因探针基础上改进的双链基因探针[7],遵循双链探针Tm值低于探针与模板结合Tm值的原则,由不完全互补的正、负2条链组成。一条链5'端标记荧光基团(R),3'端标记相应淬灭基团(Q),其互补链5'端标记荧光基团,3'端标记相应淬灭基团(图2)。该探针结构的主要优点,一是探针一条链5'端标记的荧光基团和另一条链3'端标记的淬灭基团距离更近,淬灭更彻底,降低背景荧光信号,可提高灵敏度;二是标记荧光和相应淬灭基团的2条探针均与模板结合,也可进行基因分型检测。
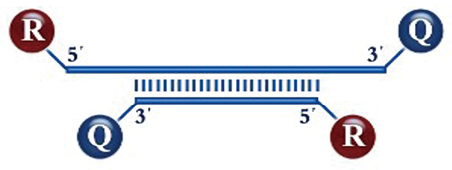
图2. 双链基因探针原理图
2. 基于CRISPR的核酸检测技术:近年来,CRISPR/Cas技术飞速发展,基于该技术发展的分子检测方法具有快速、灵敏、特异、廉价等特性,已广泛应用于生命科学领域,尤其在病原体检测领域发展迅速。目前用于呼吸道病原体检测的主要有CRISPR/Cas12和CRISPR/Cas13等系统。CRISPR/Cas13检测系统,张锋等[8]开发了一种基于CRISPR/Cas13的SHERLOCK技术,为SARS-CoV-2提供了快速准确的诊断方法。通过使用合成的SARS-CoV-2的RNA片段,设计并检测了2个可识别SARS-CoV-2特征的sgRNA,激活Cas13酶活性,切割报告分子,产生信号(图3)。该技术最后需要将试纸条浸入反应体系中,通过辨识条带位置的不同来确认是否感染SARS-CoV-2。
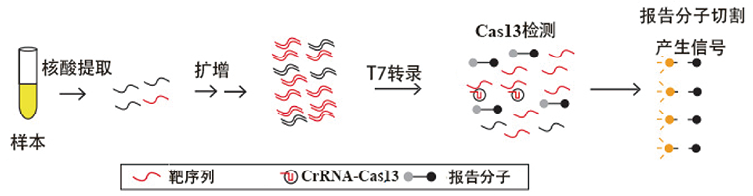
图3. CRISPR/Cas13检测系统
诺贝尔奖获得者Doudna等[9]报道了一种CRISPR/Cas13a和手机直接检测新冠病毒的RNA的方法,这是一种简便且便携的检测方法,实现从采样到检测的一体化。该装置通用小型精简的手机摄像头进行荧光测试。此外,因为手机摄像头具有高灵敏度、强连接性以及GPS和数据处理功能,所以这是一种可以应用到资源匮乏地区的实用工具,有助于即时检测(图4)。
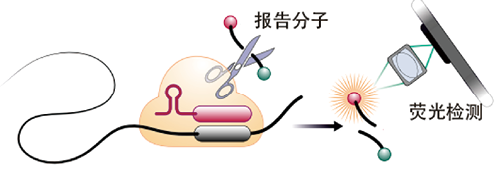
图4. 基于手机的CRISPR/Cas13核酸检测系统
在CRISPR/Cas12检测系统,美国加州大学研究人员开发了一种基于CRISPR/Cas12的快速检测SARS-CoV-2的方法,称为DETECTR(DNA endonuclease targeted CRISPR trans reporter)的病毒传感器。该方法具有与qRT-PCR相当的准确性,具有无需加热循环、快速、单核苷酸靶标特异性、无需复杂的实验室设备等优势[10]。此外,复旦大学牵头的研究团队报道了一种基于CRISPR/Cas12的“多相复式非连续生产法”用于检测SARS-CoV-2,俗称“一锅法”(opv CRISPR),是将逆转录环介导等温扩增技术(RT-LAMP)及Cas12a剪切整合到一个反应体系中完成检测(图5)。在SARS-CoV-2潜在感染的临床样本的检测中,用opv CRISPR方法得到的结果和中国疾病预防控制中心批准的RT-PCR的检测结果达到100%的一致。这种“一锅法”的形式,可以完全避免扩增子的污染,实验操作步骤也被大大简化,具有很好的临床应用前景[11]。
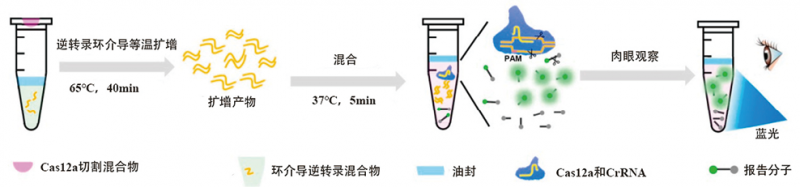
图5. CRISPR/Cas12检测系统
虽然基于CRISPR/Cas的检测技术发展迅速,但是仍然存在一些障碍和局限性需要研究解决,首先受到PAM序列特点的影响,sgRNA设计的灵活性有限,设计相对复杂;其次CRISPR/Cas系统识别目标位点以外的其他位点,产生“脱靶”效应,导致检测结果出现假阳性;因此,除了对现有CRISPR/Cas的诊断技术继续优化外,仍需发现、发展新型的CRISPR/Cas诊断系统,或与其他方法进行整合以提高应用的普适性,从而确保其具有良好的临床适用性。
3. 基因芯片新技术:基因芯片(genechip)又称为DNA芯片(DNA chip)、DNA微阵列(DNA microarray),是生物芯片(biochip)的一种,也是生物芯片技术中发展最成熟、最先进入应用和实现商品化的技术[12]。基因芯片技术是直接将DNA探针或者在固相支持物(如玻片、硅片、尼龙膜等)上原位合成寡核苷酸固定于支持物表面,然后与待分析的标记样品杂交,标记的样品通过于基因芯片上已知碱基序列的DNA片段互补杂交,从而得到样品的遗传信息,确定样品的核酸序列,或对基因表达量及其特性进行分析[13]。
当前,大多数基因芯片的显像和分析方法都是基于有机荧光染料的激发荧光,该方法成熟、简便,能够达到一般的检测要求,但有机荧光染料有自身难以克服的缺点:光淬灭、信号强度低、光谱重叠等,从而影响到检测信号的灵敏性、均一性和重复性,信号检测也依赖激光共聚焦扫描仪,体积笨重,价格昂贵。我国在临床诊断用生物芯片产品研发领域处于国际领先地位,但生物芯片技术仍然没有发挥其应有的应用价值。
为解决生物芯片技术检测灵敏度低、操作步骤多、易污染等突出问题,我国研究者发明了高灵敏可视化生物芯片技术[14],研制出一种新的纳米金复合底物Nanogold-DAB,HRP能够直接催化此复合底物反应导致大量纳米金颗粒特异沉积,从而建立了一种生物芯片的纳米金复合底物高灵敏可视化检测方法,图6表示了新型底物Nanogold-DAB的反应原理:纳米金的NHS基团与DAB的一个氨基缩合反应形成酰胺键而得到Nanogold-DAB产物。该技术通过酶催化和银离子还原显色2次信号放大,灵敏度比传统方法提高10倍以上。同时,创新设计全封闭防污染芯片结构,成功研制了全新的自动化生物芯片检测仪,实现了扩增、杂交、检测和分析一体化。基于可视化生物芯片技术研制的流感病毒分型基因芯片获得了首个可视化生物芯片产品的注册证书。
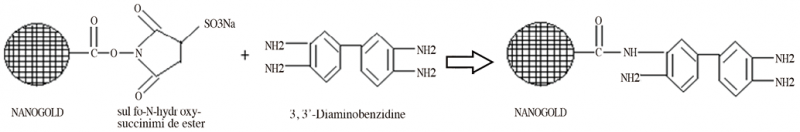
图6. Nanogold-DAB复合底物反应原理示意图
二、免疫检测新技术
免疫层析检测技术以其操作便捷、成本低廉、检测快速的特点,已广泛应用于各类样本中的小分子、生物大分子、病毒、细菌的快速检测,成为目前应用范围最广的即时检测技术之一。纳米标记材料是影响免疫层析检测性能的关键,常用材料包括胶体金、荧光纳米材料等。胶体金是免疫层析检测技术最常用的检测标签,其检测结果肉眼可见,无需使用读数设备,适用于现场定性检测。荧光纳米材料包括有机荧光染料、量子点、上转化发光纳米粒子等,具有多通道定量检测能力,其中量子点免疫层析、表面增强拉曼光谱免疫层析等新技术发展迅速。
1. 量子点免疫层析新技术:量子点(Quantum dots,QDs)是一种2~20nm尺寸的半导体纳米材料,由于量子尺寸效应而具有带隙能和荧光能尺寸可调的性质。典型的量子点材料为CdSe/ZnS核-壳结构,ZnS外壳可钝化CdSe内核表面,防止内核氧化或分解。与传统的有机荧光探针相比,量子点具有无光致漂白作用,性质稳定,高量子效率;吸收光谱宽,发射光谱窄,可由单一光源激发多种波长量子点,具有多通道检测能力的优点(图7)。采用量子点标记检测代替传统的胶体金标记技术,可实现具有高灵敏、多通道、定量检测能力的荧光免疫层析技术[15-18]。
在620nm发射波长的量子点表面分别修饰甲型流感病毒H5、H9两种亚型的检测抗体,在层析条2条检测线分别包被其捕获抗体,采用夹心法量子点荧光免疫层析实现了对这两种亚型甲型流感的同时检测,H5亚型检测限为0.016HAU,H9亚型检测限为0.25HAU,检测耗时仅15分钟[16]。针对复杂生物样本背景干扰下的高灵敏检测重大需求,新近报道了一种基于兼具磁性和量子点荧光的复合功能纳米材料,可从复杂样本中磁免疫富集待测靶标,并与免疫层析技术联用,从鼻咽拭子中富集检测甲型流感病毒,检测限为22pfu/ml[19];检测SARS-CoV-2 spike(S)和核衣壳蛋白(NP)抗原检测灵敏度分别为1pg/ml和0.5pg/ml,有助于提高现场检测SARS-CoV-2感染的检测精度和效率[20]。
2. 表面增强拉曼光谱(SERS)免疫层析技术:拉曼光谱是一种表征分子结构振动的指纹光谱,在表面科学、材料表征、痕量检测、生命科学方面有着广泛应用前景。20世纪70年代,Fleischmann、Van Duyne和Creighton等发现吸附在粗糙银电极表面或附近的分子的拉曼信号得到极大提高,即表面增强拉曼散射(surface-enhanced Raman scattering,SERS)[21-23]。多种贵金属增强基底可使吸附于其表面的分子SERS信号比普通拉曼信号增强104~107倍,并且贵金属纳米缝隙及纳米尖端附近电磁场发生共振耦合,形成热点(hot spot)效应,能够产生强烈的SERS增强效应。相较于传统的胶体金标记手段,SERS标记具有灵敏度高、抗光漂白、光谱带宽窄、多通道检测能力等优势,已广泛应用于生化分析领域[24-27]。将拉曼标记物应用于免疫层析检测,有望提高免疫层析检测灵敏度和检测通量。
最近报道了磁免疫富集SERS免疫层析检测呼吸道病毒的应用[28]。单分散的Fe3O4磁核表面以带正电的聚乙烯亚胺静电吸附大量纳米金颗粒作为种子还原一层银壳,吸附拉曼报告分子,并共价偶联修饰甲型流感病毒和腺病毒的抗体(图7a)。功能化的磁性SERS标签可实现从复杂样本中免疫结合、磁富集病毒颗粒,并结合免疫层析试纸条,实现快速高灵敏的SERS检测(图7b)。通过磁富集和SERS增强双重机制,使检测限比胶体金法降低了2000倍。
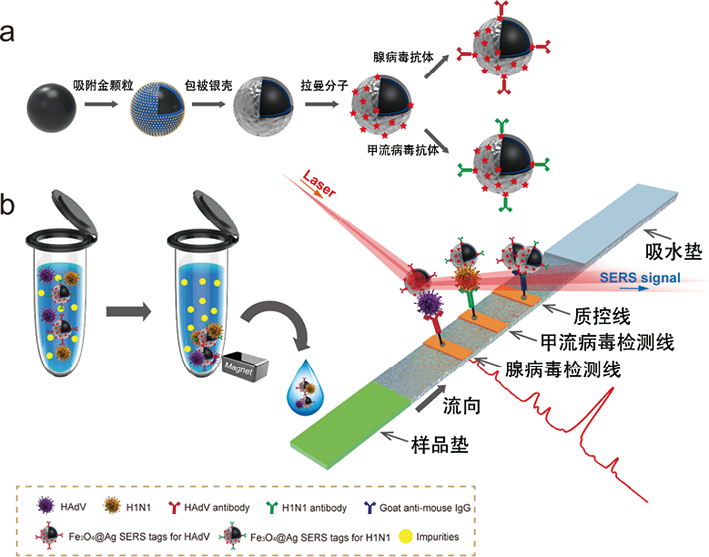
图7. 表面增强拉曼光谱免疫层析技术检测呼吸道病毒
三、病原体快速检测技术研发重点
近年来,尤其是新冠肺炎疫情以来,呼吸道传染病快速检测技术和产品研发取得了突破性进展,研究开发了大批适用于不同应用场景的创新检测技术和产品。在后续的基础研究和技术产品开发中,应着力研发或解决以下几个重点问题。
1. 发现新的诊断标志物并充分验证其特异性:生物标志物是生命科学基础研究向临床诊治转化的桥梁。包括疾病诊断标志物和药物治疗特征标志物等在内的特异性生物标志物发现,以及在此基础上研制的特异性诊疗技术,是实现检测技术源头创新重要体现。新的标志物不仅包括诊断相关标志物,还应包括预测病情严重程度等标志物,同时应充分考虑从个体差异角度发现宿主特异性标志物的可能性。
2. 加强检测试剂参考品的研发和储备:参考品是检测试剂标准化的重要物质基础,是控制试剂质量必不可少的工具,但目前呼吸道检测试剂相关国家参考品的品种和数量暂不能完全满足试剂研发、注册检验的需要,可通过组织相关研发企业、具有病原体培养能力的单位以及疾病控制、医疗机构等单位,共同进行参考品的研发、合作标定和验证,应急条件下可考虑由国家组织对检测试剂进行统一的考核和性能评价。
3. 重视体系化呼吸道传染病病原体检测产品的研制:应着力突破现有检测技术和产品的局限,完成呼吸道传染病病原体检测产品的补缺配套和升级换代,实现检测技术和产品的一体化、集成化、自动化和箱组化,形成从已知到未知病原体、从现场到实验室的病原体快速检测和确证能力,全面提升我国对呼吸道病原体的检测能力和技术水平。
参考文献
Sun P, Ye Y, Li Y, et al. Establishment of hydrolysis probe system real-time PCR assay for rapid detection of canine circovirus. 3. Biotech, 2021, 11: 472.
Drake TJ, Tan W. Molecular beacon DNA probes and their bioanalytical applications. Appl Spectrosc, 2004, 58: 269A-280A.
Emig M, Saussele S, Wittor H, et al. Accurate and rapid analysis of residual disease in patients with CML using specific fluorescent hybridization probes for real time quantitative RT-PCR. Leukemia, 1999, 13: 1825-1832.
Stroup SE, Roy S, McHele J, et al. Real-time PCR detection and speciation of cryptosporidium infection using scorpion probes. J Med Microbiol, 2006, 55: 1217-1222.
Li Q, Luan G, Guo Q, et al. A new class of homogeneous nucleic acid probes based on specific displacement hybridization. Nucleic Acids Res,2002, 30: E5.
Wang SX, Wang S,Chen WG. A new fluorescent quantitative polymerase chain reaction technique. Analytical Biochemistry, 2002, 309: 206-211.
刘丽艳, 刘琪琦, 张影, 等. 双链探针实时荧光PCR核酸检测新技术研究, 中国生物工程杂志, 2020, 40(11): 28-34.
Joung J. Detection of SARS-CoV-2 with SHERLOCK One-Pot Testing. N Engl J Med, 2020. 383(15): 1492-1494.
Fozouni P. Amplification-free detection of SARS-CoV-2 with CRISPR-Cas13a and mobile phone microscopy. Cell, 2020???.
Broughton JP. CRISPR-Cas12-based detection of SARS-CoV-2. Nat Biotechnol, 2020,38(7): 870-874.
Wang R. opvCRISPR: One-pot visual RT-LAMP-CRISPR platform for SARS-cov-2 detection. Biosens Bioelectron, 2021, 172: 112766.
Bowtelld DL. Options available from start to finish-for obtaining expression data by microarray. Nat Genet, 1999, 21(2): 25-32.
Schena M. Genome analysis with gene expression microarrays. BioEssays, 1996, 18(5): 427-431.
Qi SH, Chen RH. Shi HM,Zhang SW.Introduction of nanogold-DAB as a HRP substrate for simplifying detection in visual DNA microarrays. Analytical Methods, 2012,4 1178–1181.
Petryayeva E, Algar WR. Multiplexed homogeneous assays of proteolytic activity using a smartphone and quantum dots. Anal Chem, 2014, 86 (6): 3195-3202.
Wu F, Yuan H, Zhou C, et al. Multiplexed detection of influenza A virus subtype H5 and H9 via quantum dot-based immunoassay. Biosens Bioelectron. 2016, 77:464-470.
Di Nardo F, Anfossi L, Giovannoli C, et al. A fluorescent immunochromatographic strip test using quantum dots for fumonisins detection. Talanta, 2016, 150:463-468.
Zhou J, Yang Y, Zhang CY. Toward biocompatible semiconductor quantum dots: from biosynthesis and bioconjugation to biomedical application. Chemical Reviews, 2015, 115 (21): 11669-11717.
Bai ZH, Yang WX, Zhu YY, et al.Rapid enrichment and ultrasensitive detection of influenza a virus in human specimen using magnetic quantum dot nanobeads based test strips, sensors and actuators B, Chemical, 2020, 325: 128780.
Wang CX, Liu CL, Zhang X, et al. Ultrasensitive and simultaneous detection of two specific SARS-CoV-2 antigens in human specimens using direct/enrichment dual-Mode fluorescence lateral flow immunoassay. ACS Applied Materials & Interfaces, 2021, 13: 40342-40353.
Wang C, Wang C, Wang X, et al. Magnetic SERS strip for sensitive and simultaneous detection of respiratory viruses. ACS Appl Mater Interfaces, 2019, 11 (21): 19495-19505.
Fleischmann M, Hendra PJ, McQuillan AJ. Raman spectra of pyridine adsorbed at a silver electrode, Chemical Physics Letters, 1974, 26 (2): 163-166.
Jeanmaire DL, Van Duyne RP. Surface raman spectroelectrochemistry: Part I. Heterocyclic, aromatic, and aliphatic amines adsorbed on the anodized silver electrode. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry, 1977, 84 (1): 1-20.
Albrecht MG, Creighton JA. Anomalously intense raman spectra of pyridine at a silver electrode. J Am Chem Soc, 1977, 99 (15): 5215-5217.
Li M, Cushing SK, Liang H, et al. Plasmonic nanorice antenna on triangle nanoarray for surface-enhanced raman scattering detection of hepatitis B virus DNA. Anal Chem, 2013, 85 (4): 2072-2078.
Li M, Kang JW, Sukumar S, et al. Multiplexed detection of serological cancer markers with plasmon-enhanced raman spectro-immunoassay. Chem Sci, 2015, 6 (7): 3906-3914.
Wang J, Wu X, Wang C, et al. Magnetically assisted surface-enhanced raman spectroscopy for the detection of staphylococcus aureus based on aptamer recognition, ACS Appl Mater Interfaces, 2015, 7 (37): 20919-20929.
Qian X, Peng XH, Ansari DO, et al. In vivo tumor targeting and spectroscopic detection with surface-enhanced Raman nanoparticle tags. Nat Biotechnol, 2007, 26 (1): 83-90.
Wang C, Wang C, Wang X,et al. Magnetic SERS strip for sensitive and simultaneous detection of respiratory viruses. ACS Appl Mater Interfaces, 2019, 11 (21): 19495-19505.




