当代基因检测对于健康个体临床诊疗的重要价值

马懿,现任北京安智因生物技术有限公司医学部经理。西安交通大学生物工程系学士,医学院法医系直攻博研究生,澳大利亚昆士兰大学生物医学科学系博士,墨尔本贝克心脏病和糖尿病研究所分子心肌病部研究员,中国医学科学院北京阜外医院实验诊断中心周洲教授课题组博士后,获2012年国家优秀自费留学生奖学金,2020年大兴区优秀青年人才。曾受聘在中国遗传学会遗传咨询分会举办的“第十一届遗传咨询培训班”担任授课讲师,任《高通量测序技术临床规范化应用北京专家共识》起草组执行专家。在包括European Heart Journal在内的业内高水平杂志发表SCI论文及核心期刊十余篇。

殷昆仑,博士,助理研究员,现任中国医学科学院北京阜外医院实验诊断中心项目负责人;并担任中心高通量测序平台负责人。研究方向为心肌病分子诊断和遗传学研究,以第一和参与作者身份发表SCI论文11篇,主持中国医学科学院阜外医院青年基金项目一项,参与多项国家自然科学基金和中国医学科学院重大专项。
近年来,高通量测序技术(next generation sequencing,NGS)在单基因遗传病,尤其是整体发病率相对较高的遗传性心血管病临床应用中的重要意义已经得到了普遍认可,且在国内外得到了广泛应用,包括疾病相关所有致病基因的基因组合检测(panel)以及覆盖人类目前已知的20000多个基因的全外显子组测序(whole exome sequencing,WES)和全基因组测序(whole genome sequencing,WGS)[1]。由于WES和WGS自身覆盖基因的全面性,在实际应用中,也会检出与受检者现有临床表现或检测意图无关,但大概率会引起相关疾病的(可能)致病变异,即次要发现(secondary finding)或偶然发现(incidental finding)。因此美国医学遗传学与基因组学学会(The American College of Medical Genetics and Genomics,ACMG)在综合考虑这些变异相关疾病的外显率、疾病严重程度、是否有医学干预方法之后,推荐在受检者签署相关知情同意后,告知与受检者现有临床表现不符、但具有严重影响且有临床干预措施的偶发基因(v3版,共73个基因,其中与遗传性心血管病相关的有35个基因[2])。国内暂时无相关研究支持在无症状的健康人中进行NGS检测的重要意义。本文报道了在日常检测过程中遇到的几例健康个体进行检测的案例,借此说明基因检测对于“健康”个体的重要作用。
一、典型病例1
受检者X先生是一名44岁男性(图1,III5),自述最近加班后常出现胸闷气短,且站久后出现下肢浮肿的症状,与自己确诊为肥厚型心肌病(hypertrophic cardiomyopathy,HCM)的父亲(II5)心衰时候的表现类似,因此自行服用了父亲常用药倍他乐克,但症状似乎无好转。考虑到自己家族内除父亲外还有多名确诊的HCM患者(II2,II3,II4,III2,III3),且此前已在中国医学科学院阜外医院通过基因检测找到明确的MYH7 c.1988G>A(p.Arg663His)致病变异,受检者X先生感觉自己可能也患有HCM,随即在阜外医院进行了相关临床检查。但心电图及超声心动图的检查结果基本正常,仅提示窦性心律不齐及左房略增大(39mm),心肺运动试验结果完全正常。临床医生觉得目前无HCM相关提示,建议受检者X先生无需服药,调整更为健康的生活方式,减少熬夜,再观察看看。但受检者X先生仍然无法放心,觉得自己可能只是像8岁的侄儿(IV1)一样暂时未发病,最后医生建议可进行亲属中已鉴定出的MYH7致病变异的Sanger测序,进一步评估是否真的存在家族性HCM风险。测序结果提示受检者X先生并未携带家族遗传的MYH7致病变异,将来发生HCM的概率较低,与普通人无异。根据中外HCM相关临床指南[3, 4]推荐,基因检测结果阴性的X先生无需进行临床随访,不像自己携带MYH7致病变异的无症状侄儿(IV1),需要长期临床随访,以便及早发现病情进展,及时干预改善预后。至此,借助于基因检测,受检者X先生终于消除了“心病”,按照医嘱,停止了自行服药,不再熬夜,胸闷的症状也逐渐消失。
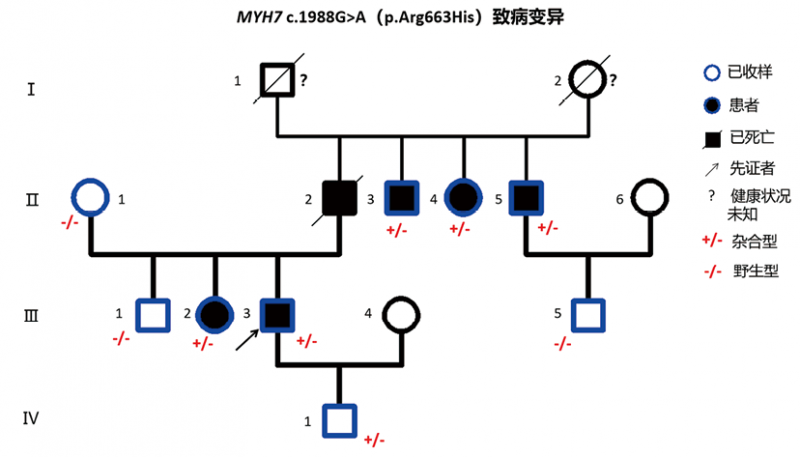
图1. 案例1中受检者(III5)的明确肥厚型心肌病家族史及家系中的MYH7c.1988G>A致病变异携带情况(+/-,杂合;-/-,野生型)。Sanger测序发现受检者并未携带该MYH7致病变异,因此今后罹患肥厚型心肌病的概率较低,与普通人无异。
受检者Y先生是一名20岁的男性,平素体健,且心脏彩超未见异常,但其父亲2年前因主动脉夹层进行了主动脉置换手术,临床怀疑父亲有马凡综合征的可能。受检者Y先生自行学习后发现马凡综合征为一种遗传病,且主动脉夹层也有遗传因素的影响,因此想了解自己今后发生主动脉夹层的风险,联系了相关医院,希望进行相关疾病的基因检测。
目前中外相关指南[3-6]均建议对临床确诊或高度疑似的遗传性心血管病患者进行检测,并在找到明确的(可能)致病变异后,再对其家系进行该变异位点的遗传筛查,有助于发现新的患者和致病变异携带者,但对于仅有家族史的无症状亲属目前尚无相关推荐。因此,临床建议受检者Y先生先送疑似马凡综合征父亲的样本进行遗传性主动脉病基因组合检测(panel),但受检者Y先生表示作为家中独子,并不想让父亲知道,增加父亲的心理负担,只要确定自己是否有患病风险,并保证自己将来的后代也无患病风险即可。最终,受检者Y先生在被临床医生明确告知基因检测后即使未能发现明确的(可能)致病变异也不代表无患病风险后,仍强烈要求进行检测。不过,最终的检测结果却证实了受检者Y先生的担忧,受检者Y先生的确携带一个与马凡综合征(Marfan syndrome,MFS)相关的明确致病变异FBN1 c.7409G>A(p.Cys2470Tyr),提示其父亲的主动脉夹层很可能也源于马凡综合征,而非孤立性的。
最终,临床医生根据相关指南和专家共识[5, 6],建议受检者Y先生作为一名基因型阳性的无症状携带者,应进行疾病早期预测和干预,如定期(发生主动脉扩张前每年1次,扩张后半年1次)影像学检查以发现和监控早期疾病。同时,由于受检者Y先生也有50%的概率再生出一名患者,因此若今后有生育健康后代的需求,可以通过选择性生育(如产前筛查或胚胎植入前遗传学筛查)获得不携带该致病变异的后代[5, 6]。
三、典型病例3
受检者H先生,43岁,受邀参加了公司内部针对健康人设计的免费遗传性心血管病风险与个体化用药相关基因检测,签署相关知情同意时并未告知存在任何健康状况异常。该基因检测主要覆盖了ACMG推荐报告的与11种严重心脑血管病相关的高风险遗传综合征相对应且有医学干预方法的35个偶发基因[2]的整个编码区及相邻的5bp内含子区,同时也检测了与34种心血管病药物反应性相关的27个多态性位点。
检测结果显示,受检者H先生携带1个与家族性高胆固醇血症(Familial hypercholesterolemia,FH)相关的致病变异APOB c.10579C>T(p.Arg3527Trp)。FH是一种常染色体(共)显性遗传病,其主要临床表现为血清低密度脂蛋白胆固醇(low density lipoprotein-cholesterol,LDL-C)水平明显升高,部分患者可能出现皮肤/肌腱的黄色瘤[7]。联系受检者H先生询问其最近一次的体检结果,发现其胆固醇及LDL-C水平均已显著升高,分别为6.64mmol/L(正常2.8-5.7mmol/L)及4.72mmol/L(正常<4.0mmol/L),且已经持续了一段时间,但并未出现明显的黄色瘤。此前,受检者H先生一直觉得自己的血脂异常只是吃得太好导致的,只要控制饮食多加锻炼就可以恢复,因此从未就医。但根据FH中国专家共识[7],检测到LDLR、APOB、PCSK9和LDLRAP1基因上的致病/可能致病性突变是诊断FH的金标准,因此受检者H先生可直接确诊为FH,其胆固醇及LDL-C升高也是源于检出的APOB致病变异,而非单纯的生活习惯不佳,应立即启动降胆固醇药物治疗,这样才能降低早发动脉硬化性心血管疾病的风险,从而改善存活率。
这与同为常染色体显性遗传的HCM一样,专家共识和指南同样建议对已找到明确致病变异的FH患者家系进行该变异位点的筛查[5, 7]。通过询问受检者H先生的家族史发现,其母亲一直在服用他汀来控制LDL-C水平,有较大可能也携带该APOB致病变异,并遗传给了受检者H先生。在确定自己的高血脂主要是由遗传导致后,受检者H先生终于就医,并开始服用他汀,不久便将LDL-C水平控制在了正常范畴。
四、分析与讨论
在临床诊断的背景下,基因变异的致病性判断通常需要基于患者的临床表型和家族史提供支持性信息。目前,国内外所有的专家共识和指南均推荐对疑似或确诊的遗传性心血管病患者(包括成人和儿童)进行相关的基因检测,若能找到明确的(可能)致病变异,不但可以帮助患者明确诊断和鉴别诊断,也可进行高危亲属筛查,并从一定程度上指导临床诊疗及优生优育[3-8]。但对于健康人,或仅有家族史的健康人,目前暂无足够证据支持基因检测的必要性,也没有关于在确定潜在致病性偶然发现后应如何进行后续管理的相关指南。
此前,针对4525名美国无症状成人的WES结果显示,有0.9%的无症状个体携带遗传性心血管病相关(可能)致病变异,其今后14.3年内发生心血管病相关死亡的风险比其他个体高3.24倍[9]。而针对21915名eMERGE网络(如生物银行、专科门诊等)的个体基因检测数据重新分析发现,遗传性心血管病相关偶发基因上的(可能)致病变异比例为0.87%,仅次于遗传性肿瘤的1.38%[10]。阜外医院此前针对421名表型正常、肥胖或先天性心脏病儿童进行WES检测发现,约2.85%(12名)的个体携带与其表型无关的偶发基因(可能)致病变异,其中9名携带遗传性心血管病相关变异(3名FH,4名心肌病,1名马凡综合征,1名嗜铬细胞瘤/神经节瘤)[11]。以上研究均提示,成人及儿童中发现的与其临床表现无关的遗传性心血管病相关偶然发现可能并不罕见,应该得到重视。
本文中的3个案例实际上代表了从基因型推测临床表型,并在一定范围内指导临床的可行性,它与此前更为常见的基于临床表型研究基因型的过程截然相反。当然,这也对受检者后续的临床随访、健康管理及可能产生的社会心理学负担提出了挑战。为了更好地指导临床实践,可能需要更为系统地收集和整理偶然发现相关数据,并结合基因及变异特异性证据来估计外显率,以便更为深入地确定变异表型谱。
综上所述,虽然目前国内尚缺乏针对健康成人及儿童的大规模测序研究,但目前的研究结果及包括本文中介绍的3个案例在内的临床实践经验均支持对“健康”个体,尤其是有家族史的“健康”个体进行基因检测,其不可忽视的临床意义和社会影响应该得到重视。
参考文献
惠汝太,张抒扬.单基因遗传性心血管疾病基因诊断与精准治疗可靠、可行、可用. 中华心血管病杂志, 2019. 47(3): p. 4.
Miller DT, Lee K, Chung WK, et al.ACMG SF v3.0 list for reporting of secondary findings in clinical exome and genome sequencing: a policy statement of the American College of Medical Genetics and Genomics (ACMG). Genet Med, 2021. 23(8): p. 1381-1390.
3.Ommen SR, Mital S, Burke MA, et al.2020 AHA/ACC guideline for the diagnosis and treatment of patients with hypertrophic cardiomyopathy: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation, 2020. 142(25): p. e558-e631.
中华医学会心血管病学分会, 中国成人肥厚型心肌病诊断与治疗指南编写组, 中华心血管病杂志编辑委员会, 中国成人肥厚型心肌病诊断与治疗指南. 中华心血管病杂志, 2017. 45(12): p. 18.
中华医学会心血管病学分会精准心血管病学学组, 中国医疗保健国际交流促进会, 精准心血管病分会, et al., 单基因遗传性心血管疾病基因诊断指南. 中华心血管病杂志, 2019. 47(3): p. 22.
国家心血管病专家委员会血管外科专业委员会, 杨航, 罗明尧, et al., 遗传性胸主动脉瘤/夹层基因检测及临床诊疗专家共识. 中国循环杂志, 2019. 34(4): p. 7.
中华医学会心血管病学分会动脉粥样硬化及冠心病学组and 中华心血管病杂志编辑委员会, 家族性高胆固醇血症筛查与诊治中国专家共识. 临床医学研究与实践, 2018. v.3(09): p. 207.
Landstrom AP, Kim JJ, Gelb BD, et al. Genetic Testing for Heritable Cardiovascular Diseases in Pediatric Patients: A Scientific Statement From the American Heart Association. Circ Genom Precis Med, 2021. 14(5): p. e000086.
Khera AV, Mason-Suares H, Brockman D, et al., Rare Genetic Variants Associated With Sudden Cardiac Death in Adults. J Am Coll Cardiol, 2019. 74(21): p. 2623-2634.
Mcaw G.Frequency of genomic secondary findings among 21,915 eMERGE network participants. Genet Med, 2020. 22(9): p. 1470-1477.
Chen W, Li W, Ma Y, et al.Secondary findings in 421 whole exome-sequenced Chinese children. Hum Genomics, 2018. 12(1): p. 42.




