阵发性睡眠性血红蛋白尿综合征的诊断与治疗

邓坤仪,主任技师。现任职于广东省中山市博爱医院检验科主任技师;从事细胞形态检验工作多年,共主持市级科研课题3项,参与科研课题多项,曾获中山市科技进步一等奖1项,中山市科技进步二等奖1项。参与《医学检验形态学手册》的编写,发表论文十多篇。
阵发性睡眠性血红蛋白尿症(PNH):是一种获得性红细胞膜缺陷性疾病,造血干细胞PIG-A基因突变,使部分或完全血细胞膜糖化磷脂酰肌醇(GPI)锚合成障碍,造成血细胞表面GPI锚连蛋白缺失,细胞灭活补体等能力减弱,从而引起细胞容易被破坏,发生溶血等[1]。发病时临床表现为清晨酱油色尿,慢性血管内溶血,可伴有全血细胞减少和反复血栓形成。
一、临床病例介绍
1. 临床资料:患者男,45岁。主诉“全血细胞减少11年,乏力1个月”于2021年9月3日入院。既往史:2010年因乏力不适在广东省XX医院检查发现全血细胞减少,予骨髓穿刺检查,考虑再生障碍性贫血。2012年1月因“全血细胞减少、左髋疼痛、发热”于中山市XX医院住院。骨髓细胞学形态学改变符合再生障碍性贫血;骨髓FISH:CDF1R(5q33)缺失的比例为17%大于阳性参考值3.007%;诊断:骨髓增生异常综合症(5q-综合症)。2012年3月因“血细胞减少、左髋疼痛”至广东省XX医院住院,FISH:5q-(阴性),7q-(阴性);染色体:46XY,13个,45XY,37个;诊断为阵发性睡眠性血红蛋白尿伴再生障碍性贫血(PNH-AA)。2016年12月行骨髓穿刺+活检术送广州金域医学检验中心骨髓细胞结果示:增生减低骨髓象;骨髓活检:(右髂前骨髓穿刺活检)少量碎骨片及脂肪组织,未见明显造血。CD55阴性红细胞/总红细胞50.26%,CD59阴性红细胞/总红细胞:50.98%。2017年1月至中国医学科学院血液病医院住院,诊断:再生障碍性贫血-阵发性睡眠性血红蛋白尿综合征(AA-PNH)。近两年患者自觉效果欠佳,自行停服环孢素、安特尔等药物,期间多次因头晕、乏力在外院予以输血治疗,2021-04-07患者头晕、乏力明显,查血常规:WBC 3.0x109/L,Hb 42g/L,PLT 96X109/L,MCV 114.2fl,MCHC 315g/L;在我院予以输血、十一酸睾酮软胶囊促进骨髓造血,予环孢素软胶囊免疫抑制好转出院,出院后口服十一酸睾酮软胶囊、环孢素软胶囊治疗至今,近1月患者自觉乏力明显,活动后明显,血尿明显,外院查血常规示血红蛋白47g/L,今为进一步治疗,门诊拟“AA-PNH”收入我院治疗。
2. 实验室检查:(1)血常规:WBC 3.0×109/L,RBC 1.01×1012/L,HGB 43g/L,PLT 89×109/L,RET24.47%,MCV140.7fl。患者三系减低,有重度贫血,网织红百分比明显增高。(2)尿液分析:尿液外观呈浓茶色,PH7.0,隐血2+;蛋白质2+;尿胆原+。尿沉渣中完整的红细胞仅为2个/μL,可见吞噬含铁血黄素上皮细胞如图1,尿含铁血黄素4+,如图2和图3。可判定为血管内溶血,血红蛋白尿。(3)生化检查:AST 90U/L,LDH 4274U/L,总胆红素51.6μmol/L,直接胆红素17.1μmol/L,间接胆红素34.5μmol/L。可溶性转铁蛋白受体238.11nmol/L。这证明患者体内存在溶血现象并缺铁。(4)基因检查:检测到PIGA基因突变,PIGA编码糖基化相关蛋白,基因突变可导致获得性造血干细胞克隆性疾病,为PNH发病机制之一。

图1. 尿沉渣10×40倍含铁血黄素阳性细胞(未染色)
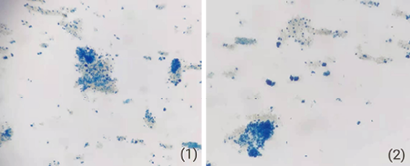
图2. 尿沉渣10×40倍含铁血黄素阳性细胞(普鲁士蓝染色)
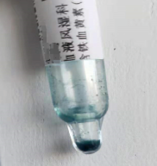
图3. 患者尿普鲁士蓝染色(外观)
3. 鉴别诊断:患者2017年1月于中国医学科学院血液病医院诊断再生障碍性贫血—阵发性睡眠性血红蛋白尿(AA-PNH)。确诊后不规则口服环孢素、安特尔。近两年停服环孢素、安特尔以至病情加重,外周血三系减低,晨起血尿,呈浓茶色。骨髓增生活跃,溶血性骨髓象。简易血清酸化溶血试验(Hams试验)、蔗糖水溶血试验和尿含铁血黄素试验(尿Rous试验)统称简易“PNH三项”。结合病史和临床症状,该病例选择本实验室开展的尿含铁血黄素试验(尿Rous试验),得出强阳性结果,酸化溶血试验(Hams试验)阴性。流式细胞结果、染色体核型分析、MDS FISH六项结果未见异常,AA相关基因PIGA突变,该基因是PNH发病机制之一。如果不了解这是一位有AA-PNH病史的患者,他的一些检查结果会让人迷惑,比如他的血红蛋白降低了,MCV增高,可溶性转铁蛋白受体(sTfR)升高了,骨髓铁染色外铁阴性,外铁阳性率达83%。是缺铁性贫血合并巨幼细胞性贫血吗?结合病情、sTfR和铁染色结果可见患者是存在缺铁性贫血。网织红细胞达24.47%,总胆红素、直接胆红素和间接胆红素增高,叶酸和维生素B12正常,骨髓细胞未见巨幼变,可认为是溶血进行中,新生的红细胞增多,造成MCV明显增高。
4. 临床诊断:再生障碍性贫血-阵发性睡眠性血红蛋白尿综合征(AA-PNH)。
5. 治疗:输血、补铁、碱化尿液、免疫抑制促进造血等对症处理,一周后复查血常规血红蛋白从刚入院的49g/L上升至89g/L,出院一个月后复查血常规血红蛋白88g/L,患者病情得到控制。
二、讨论与分析
1. PNH诊断标准[2]:(1)临床表现符合PNH;(2)实验室检查:Hams(酸溶血)试验,糖水试验,蛇毒因子溶血试验,尿潜血(或尿含铁血黄素)等项试验中符合下述任何一种情况:①两项以上阳性;②一项阳性,但须具备下列条件:A:两次以上阳性,或一次阳性,但操作正规,有阴性对照,结果可靠,即时重复仍阳性者。B:有溶血的其他直接或间接证据,或有肯定的血红蛋白尿出现。C:能除外其他溶血,特别是遗传性球形红细胞增多症,自身免疫性溶血性贫血,葡萄糖6-磷酸脱氢酶(G6PD)缺乏症所致的溶血和阵发性冷性血红蛋白尿症等。③流式细胞术检测发现外周血中CD55或CD59阴性中性粒细胞或红细胞>10%(5%~10%为可疑)。若临床表现符合,实验室检查具备1)项或2)项者皆可诊断本病,而该两项也可以相互佐证。本病例于2017年1月于中国医学科学院血液病医院诊断再生障碍性贫血—阵发性睡眠性血红蛋白尿(AA-PNH)。
2. 尿含铁血黄素试验:尿含铁血黄素试验也称Rous试验。当血管内红细胞被大量破坏时,血红蛋白可直接通过肾脏滤过。久之铁离子可以含铁血黄素的形式沉积于上皮细胞,并随尿液排出。尿中含铁血黄素是不稳定的铁蛋白聚合体,其高铁离子与亚铁氰化钾作用,在酸性环境下可产生蓝色的亚铁氰化铁沉淀[3]。
本实验室在尿沉渣0.2ml中先后滴加20%亚铁氰化钾和浓盐酸试剂充分混匀,再向沉渣中滴加染色液应用液1ml,在室温下放置30min后离心沉淀,取出上清液后对沉渣进行显微镜检查。
如在高倍镜下见有分散或成堆的蓝色、直径约1~3μm粗大颗粒即为阳性,如在上皮细胞内出现则更为可靠,有时管型中亦可见到同样的蓝色颗粒。正常人应为“阴性”,该病例结果则呈“阳性”。阳性结果主要见于慢性血管内溶血,如阵发性睡眠性血红蛋白尿症。也见于溶血性输血反应、机械性红细胞损伤、烧伤、药物性溶血和重型血红蛋白病等。血管内溶血初期,上皮细胞内尚未形成可检出的含铁血黄素,可呈阴性反应[3]。
3. 临床经验总结:本病例是临床已确诊的AA-PNH患者,本文的主要目的是向读者展示传统项目Rous试验的操作方法和阳性结果。通过本病例可见,Rous试验在重度贫血,血红蛋白尿频发的PNH病人呈强阳性。PNH检测项目与FCM(流式细胞)技术相比,前者具有设备便宜,容易开展,收费低,患者易接受,但敏感性和特异性不足;后者则敏感性高且特异性强,但设备昂贵,收费高,难成为基层医院贫血疾病诊断的筛查项目。在查找文献的过程中,我也发现不少将PNH误诊为单纯缺铁性贫血的病例报道,误诊患者的临床症状和表现与缺铁性贫血非常相似,但常规补铁治疗可能诱发或加重溶血。因此临床上遇到反复发作,病因不明,经输血或补铁治疗效果不良的缺铁性贫血;贫血伴溶血、黄疸、尿液颜色改变,要考虑PNH可能,必要时行PNH三项检测及流式细胞术进一步排查。
参考文献
[1] 肖作淼, 张丽琴, 叶萍, 唐金凤, 邹民, 肖九长. 简易“PNH三项”与流式细胞术在PNH诊断
与鉴别诊断的综合价值比较[J]. 赣南医学院学报, 2018, 38(03): 225-228.
[2] 沈悌, 赵永强. 血液病诊断及疗效标准[M]. 4版. 北京: 科学出版社,2018.
[3] 尚红, 王毓三, 申子瑜. 全国临床检验操作规程[Ml. 4版, 北京: 人民卫生出版社, 2015.




