Lp(a)检测标准化
脂蛋白(a)[Lp(a)] 是心血管疾病风险的重要预示因子。许多研究说明,血浆Lp(a)水平的升高与心血管疾病危险增加有关。但是,无论国内或国外,各个实验室间的Lp(a)检测结果缺少可比性,一个患者标本的Lp(a)结果,使用不同的试剂或检测系统,可以出现相差数倍的差异,限制了它在临床中的广泛应用。
为此,1995年国际临床化学与检验医学学会(IFCC)成立Lp(a)工作组,与国际研究机构、多个诊断公司一起,探索Lp(a)国际参考物质。历经8年努力,终于在2004年,IFCC的生物标准化专家委员会接受了“IFCC SRM 2B”为国际上第一个Lp(a)免疫测定的WHO/IFCC国际参考试剂。该参考物质的每个安瓿内的Lp(a)为0.1071nmol±0.0086nmol,可溯源至Lp(a)的协同参考方法;将使诊断公司的校准品在计量上溯源性符合欧洲共同体的体外诊断医学产品通则。
在整个Lp(a)标准化的工作中,Dr. Marcovina和Dr. Dati F是两位为该项工作作出杰出贡献的大家。
可是,尽管在2004年就已经建立了Lp(a)的参考方法和参考物质,但直至最近才在检验市场上出现了真正以nmol/L表达检测结果的产品,患者样品可溯源至IFCC SRM 2B。这原因何在?
一、Lp(a)结构的特殊性是使检测结果
不一的重要原因
脂蛋白(a)[Lp(a)]由LDL脂蛋白样部分与载脂蛋白(a)[apo(a)]部分共价连接组成。LDL样部分由磷脂(PL)、游离胆固醇(FC)、apoB围绕由甘油三酯(TG)和胆固醇酯(CE)构成的核心。Apo(a)结构见图1和图2。
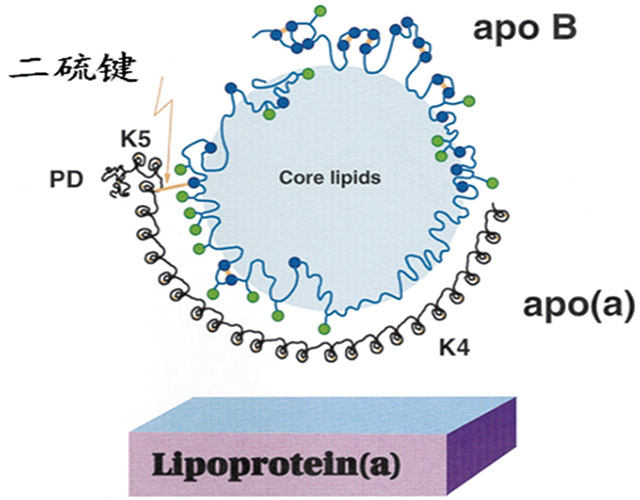
图1 脂蛋白(a)[Lp(a)]的结构图
如图1所示,在Lp(a)中,与其他脂蛋白一样,有一个脂肪核心,内含胆固醇、胆固醇酯、甘油三酯、磷脂等。在脂肪核外由两条蛋白链包裹,一条是载脂蛋白B(apoB),另一条则是代表Lp(a)特征的载脂蛋白(a)[apo(a)]。这两条蛋白链间有二硫键将它们链接。从结构上,检测Lp(a)只能检测apo(a)。
经研究了解,发现Lp(a)的特殊性质。它的大小和密度呈非均相性,完全因为是apo(a)的独特性。apo(a)是富含碳水化合物的蛋白,在个体内或个体间的颗粒大小变异很大。请仔细观察图1中apo(a)的图示,它是呈许多小圈圈互相链接的一个蛋白。每个这样的“圈圈”其实就是apo(a)的基本环饼结构(Kringle)。请参见图2。
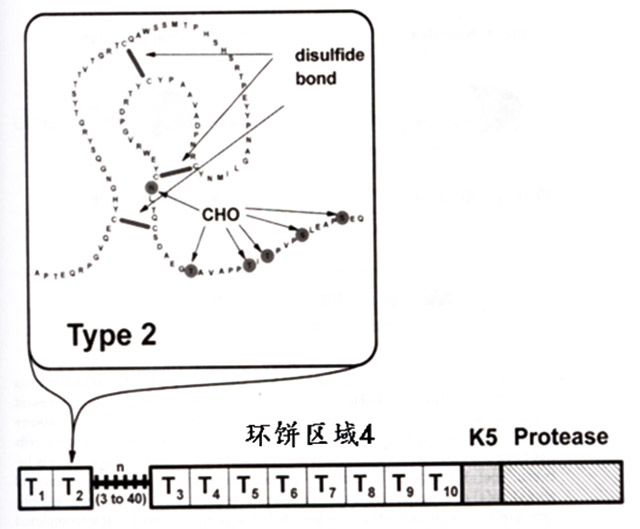
图2 apo(a)的环饼结构示意图
由于每个“圈圈”是图2所示的一个三环结构,在形态上相似于丹麦的馅饼-环饼(kringle),由此命名为环饼。从内在结构上,发现apo(a)和丝氨酸蛋白水解酶原的纤溶酶原有着高度的均相性。在蛋白化学结构上,将apo(a)放在纤溶酶原家族内。因为apo(a)纤溶酶原非常相似,它们都是以环饼结构为基础组成的蛋白。请参见图3。
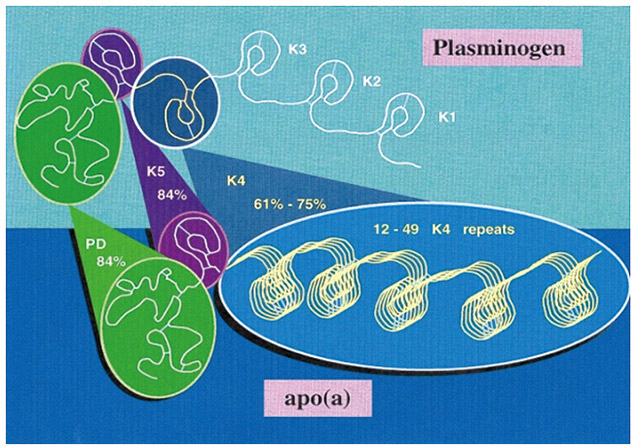
图3 纤溶酶原和apo(a)蛋白结构的比较
由图3,纤溶酶原由5种不同环饼结构域(分别被命名为罗马数字Ⅰ~Ⅴ),以及相连的氨基酸末端尾部区域(T)和胰蛋白酶样蛋白酶结构域(P)组成。注意,图示的各个环饼结构以K1、K2、K3、K4和K5表示,正确的应是KⅠ、KⅡ、KⅢ、KⅣ、和KⅤ,每一段都只是一个环饼结构。当然,在每一段的环饼内在氨基酸组成和排列是不同的。但是,apo(a)的蛋白结构中,与纤溶酶原相比,它缺失了K1、K2、和K3段;但是,原来纤溶酶原的第四段K4只是一个环饼结构,在apo(a)中却出现了由12~49个在蛋白一级序列上完全一样的重复环饼结构。这个重复结果的数量变异,使形成的apo(a)的蛋白在大小上差异很大。apo(a)是富含碳水化合物的蛋白,在个体内或个体间使最后的Lp(a)颗粒大小变异很大。最后一个尾部PD段,在纤溶酶原中,是展现纤溶酶活性的地方,但是在apo(a)中,这段尾部已经变性,不再具有酶的活性了。
为了对apo(a)有更多的理解,可以看图4。图4的上部为纤溶酶原的结构,图下部为apo(a)的结果。在图中可以看到,纤溶酶原可以分为七个结构。但是,在apo(a)中,apo(a)无尾部区域和环饼Ⅰ~Ⅲ,但在KⅣ中由多拷贝与纤溶酶原相似序列组成,内中从结构上可分为KⅣ2到KⅣ10型结构,其中除了KⅣ2外,其余KⅣ1、KⅣ3、KⅣ4、KⅣ5、KⅣ6、KⅣ7、KⅣ8、KⅣ9和KⅣ10每一型,都只是一个环饼结构序列;就是KⅣ2型内,在各个apo(a)中重复的环饼个数各异其拷贝数在各个Lp(a)中各异; KⅣ2型的重复构成了脂蛋白(a)颗粒大小异质性的分子基础,颗粒大小异质性是脂蛋白(a)的一个特征。
最后还有与纤溶酶原环饼KⅤ、最后的P段无酶活性的蛋白酶结构域相似的结构域链接组成。由于apo(a)的蛋白样结构中隐藏的纤溶酶原激活剂裂解位点发生了置换,因此纤溶酶原激活剂对裂解脂蛋白(a)的蛋白酶样结构域失活,不能将其裂解。 所以,apo(a)没有了“纤溶酶原家属”溶解纤维素的作用。
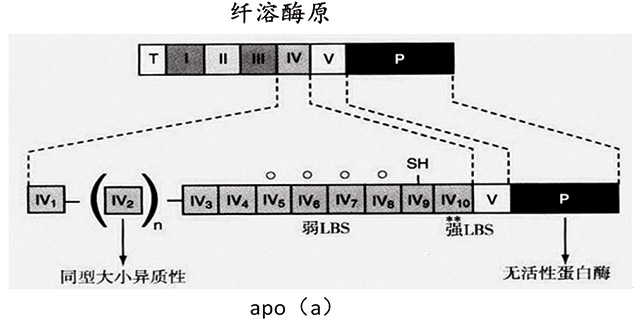
图4
综上所述,Lp(a)的多态性的根本问题是内含的apo(a)的多态性,特别是环饼区域K4的第2型中的相似环饼从3~40个不等。不论种族、性别、年龄、是否具有血脂代谢问题等,各个个体内的Lp(a)内、或各个个体间的Lp(a)间,apo(a)的多变是检测结果变异的主要原因。apo(a)的大小从187 kDa到662 kDa。大小的不均一影响了血浆中Lp(a)免疫化学检测水平。
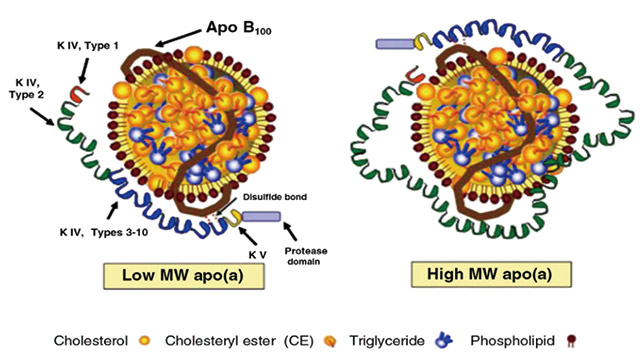
图5 不同大小的脂蛋白(a)的图示
图5形象地表示,不同大小的脂蛋白(a)颗粒内,它们中间的脂肪核心基本相似、apoB也一样长短,就是apo(a)的长短有显著差异。图中K IV,Type 1为KIV内的1型环饼;无论Lp(a)大小,都一样大小;图示的K IV,Type3-10表示在apo(a)中KIV内的3型到10型的环饼,无论Lp(a)大小也都一样。唯有K IV,Type2,即apo(a)KIV中的2型环饼,在不同大小的Lp(a)中,有着非常大的差异;高分子量Lp(a)内的2型环饼蛋白链要长得多;低分子量Lp(a)内的2型环饼蛋白链则要短得多。
在免疫检测中,检测抗体若是抗重复的K4第2型抗原,apo(a)颗粒小于存在于检测校准品内apo(a)的,Lp(a)结果偏低;反之,结果偏高。只有使用可识别每个apo(a)上仅一个类型环饼结构蛋白片断的、或抗apoB-100(apoB)的、或Lp(a)其它蛋白组分的抗体,才能准确地检测Lp(a)。这是长期以来,在形成Lp(a)检测试剂盒中长期困惑的问题。为此,只能以检测apo(a)的蛋白质量mg数来报告结果。使用mg/L的质量单位表示Lp(a)是不准确的,因为在各个Lp(a)颗粒中,apo(a)与apoB的质量比率各异。所以,应以nmol/L表示Lp(a)蛋白含量。
二、选择参与Lp(a)标准化工作的检测系统
1、确认一致同意的Lp(a)参考方法
为了准确检测所有血浆样品中的Lp(a),与apo(a)颗粒多态性无关,在美国西雅图的华盛顿大学西北脂类研究实验室,使用抗apo(a)的K4第9型的表面决定簇的单克隆抗体,形成了直接结合的双单克隆抗体酶联免疫测定方法(a-40 ELISA),检测血浆中的Lp(a)。许多研究作者对该检测方法作了详细的评价,说明apo(a)的不均一不影响测定准确度。
使用抗apo(a)K4第8型决定簇的不同检测抗体,又形成了另一个免疫测定(a1-1 ELISA),也显示了它对apo(a)异构体大小不均一的不敏感。因为以上任何单克隆抗体都不会与apo(a)分子的多变部分的决定簇反应,可以摩尔(mol)单位表示设定靶值。
2、选择合适的Lp(a)参考物质
经比较,SRM 2B使18个INA与ITA检测系统的变异小于8%(表1),显示分析性能可接受;以及在稳定性上表现良好。所以选择SRM 2B为Lp(a)的通用校准品,用于进行一致性检测调查前,为各个系统的厂商校准品定值。这是经过一个很长的艰苦努力才得到的这个目前较认可的物质。
表1 SRM 2B使18个常规检测系统经校准后,检测患者样品得到的结果
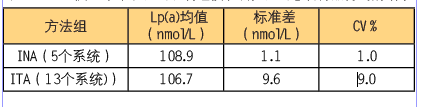
3、对SRM 2B的Lp(a)定值
使用两个实验室制备的Lp(a)一级参考物质,为SRM 2B设定靶值。使用每个新鲜制备的分离Lp(a)。使用一致统一的两个ELISA参考方法(使用的单克隆抗体分别为a-40或a1-1)进行定值。在4个连续天内,共得到SRM 2B的144个结果。无论使用哪一个Lp(a)一级参考制品、或无论使用哪一个ELISA参考方法,对SRM 2B的定值非常相似,最后的定值为:107.1nmol/L±8.6nmol/L。
三、Lp(a)标准化工作的第三阶段:
使用推荐的SRM 2B参考物质后对实现患者
血清检测结果一致性的评估
1、在第三阶段由16个厂商与6个研究实验室对SRM 2B材料评估,确定它是否具有将基础的准确值传递给厂商的校准品的能力;并经该物质标准化后,在各个方法间结果的一致性的能力。
2、选择了30份健康供体的新鲜冰冻血清,内含Lp(a)值与apo(a)异构体范围大而广;具有的K4 apo(a)区域为13~31个、Lp(a)含量范围为10~414 nmol/L,使用a-40 ELISA Lp(a)参考方法为之定值。
3、各个参与定值的Lp(a)检测系统包括:10个免疫透射比浊测定(ITA)、8个免疫散射比浊测定(INA)、2个荧光免疫测定(FIA)、1个免疫电泳测定、和1个ELISA。几乎所有的检测系统均使用多克隆抗体检测Lp(a)的apo(a)部分。有2个ITA方法使用标记于胶乳颗粒的单克隆抗体,1个FIA方法(DELFIA a/B)使用了抗apoB作为检测抗体的多克隆抗体。
4、Lp(a)的胶乳增强ITA方法是最准确的检测系统,平均绝对偏倚仅4.4nmol/L;其它方法的偏倚为12.4~23.8nmol/L。仅两个Lp(a)检测系统对ap(a)o(a)异构体的非均一具有最小的偏倚。通过使用SRM 2B,在Lp(a)的胶乳增强ITA方法与Lp(a)的协同参考a1-40ELISA测定间,具有了极其重叠的Lp(a)结果。
5、但是很明显,无论是一级或二级的参考物质,因为apo(a)大小的非均一的影响,都不能消除不同分析方法间得到的Lp(a)值的实质性差异。
四、WHO生物标准专家委员会批准IFCC SRM 2B
为“第一个Lp(a)免疫测定国际参考试剂”
WHO在2003年11月,正式接受IFCC SRM 2B为“第一个Lp(a)免疫测定国际参考试剂”,完整的称呼为:WHO/IFCC SRM 2B。该参考物质储存于玻璃安瓿,内含0.1071±0.0086 nmol的Lp(a)(依据分装时的不精密度,变异为2.9%)。它的定值可追溯至Lp(a)的美国西北参考实验室的参考检测系统。
五、罗氏系统系列的Lp(a)
2012年,罗氏公司与Dr.Marcovina的紧密合作,终于解决了常规系统检测Lp(a)结果的可比性。非常值得介绍。将准确的Lp(a)检测传递给常规化学检测系统。
1、标准化过程概述
(1)邀请Dr.Macovina为公司的顾问。由她协调和考虑实验方案。这个非常重要。
(2)所有100份进行比对的患者血清内含有的Lp(a)(a)含量(nmol/L),均由Marcovina实验室采用确认的ELISA参考方法定值。这是以SRM 2B参考物质校准后进行检测的结果。
(3)另选5份样品具有的Lp(a)值范围从低到高、异构体范围从大到小,作为罗氏建立校准品定值的溯源依据。
2、公司一级校准品定值过程
公司首先对一组Lp(a)一级校准品内各个校准品内含有的Lp(a)进行了初始检测。在一台cobas c 501仪器上,使用一个批号的试剂,按照操作程序,以公司的一级校准品初始值校准仪器。得到Lp(a)含量与免疫透射比浊的信号(△A/s)关系。在仪器上检测Dr.Marcovina提供的5份具有参考值的血清。得到在cobas上的检测结果。
Dr.Marcovina的5份血清本来就具有Lp(a)的参考值。与cobas c 501现有条件下检测得到的Lp(a)值,形成五对比较值。使用直线回归统计。观察统计结果。要求:截距很小,斜率与1的差异说明罗氏系统与参考系统的系统差距。比对的目的是希望cobas的检测结果与Dr.Marcovina参考值一致。将每个一级校准品的初始值除以斜率,使cobas c 501对5份血清检测值接近Marcovina参考值。
以各个校准品调整后的“校准值”校准cobas c 501,再检测五份Marcovina血清,再次进行比较(cobas 检测值~Marcovina参考值)。
以上校准品定值的调整和对Marcovina血清的检测、进行方法学比较,不断地调整罗氏一级校准品的校准值、反复检测5份血清,直至达到这5份血清,在罗氏的cobas c 501上,可以检测得到的结果与参考值的回收率最佳。这样,可确定罗氏的Lp(a),在cobas c 501 上的一级校准品校准值。对100份血清样品的比对,以证实一级校准品定值成功。见图6。说明一级校准品定值成功。罗氏公司的cobas c 501上以常规免疫比浊方法,可以与Dr. Marcovina的参考方法检测患者样品,得到一致的结果。
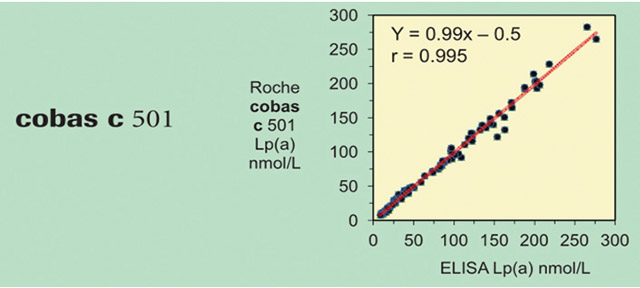
图6 一级校准品定值调整后对患者样品检测结果与Marcovina实验室检测结果的比较
3、检测可靠性在罗氏系统间的转换
为了使罗氏所有检测仪器均可以实现Lp(a)检测结果的可靠性,在cobas c 501上得到罗氏一级曲线,以专用软件转换给其他5台罗氏仪器cobas c 311、Cobas c 701、COBAS INTEGRA 400、COBAS INTEGRA 800和MODULAR ANALYTICS。然后6个仪器平台分析一组95例样品,结果被送到西北脂类代谢和糖尿病研究实验室Dr. Marcovina处,统计分析数据。
经分析,3台cobas c系统得到的结果符合确定的准确度认证指标,而其他三台罗氏分析仪显示了与apo(a)大小有关的偏移,大于确定的限值。反映Lp(a)的KIV2型中重复环饼对检测结果有影响。在Dr. Marcovina指导下,对这三个仪器平台使用专用软件工具确定了特定的校准品值。再次重复分析95例样品提供的结果,符合了认证的指标,确认了这个做法的有效性。
4、解决Lp(a)内apo(a)在K IV 2型的重复环饼影响的大致做法
(1)了解不同NWRL的Lp(a)值下对罗氏检测偏移的影响。见图8。
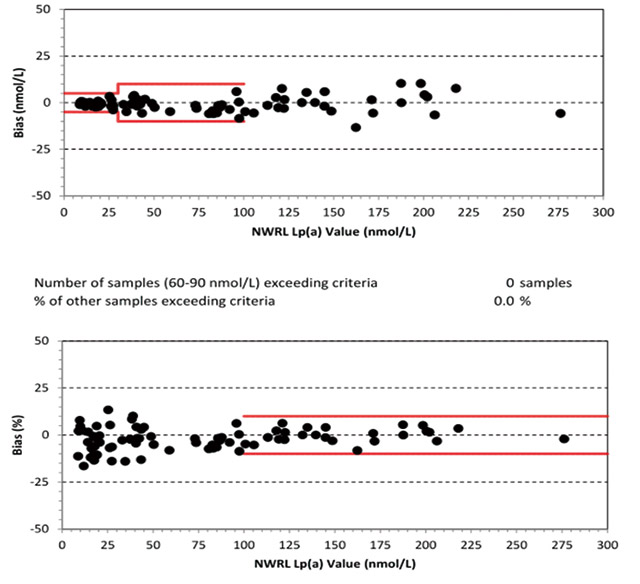
图8 样品中Lp(a)的NWRL定值与罗氏检测得到的结果偏移间的关系由图8说明,检测结果的偏移与NWRL的Lp(a)定值有关。
图9说明,出现罗氏检测结果与NWRL检测偏移,主要因检测样品中具有的apo(a)异构体分布有关。因此,Dr. Marcovina采取了初略的回归统计,估计出主要的apo(a)大小与偏移的关系。将该关系形成软件,有罗氏公司自动“纠正”因样品apo(a)异构体导致的偏移。
如上图的关系,仅回归统计为:n=80,Y=-0.15X+1.1,r=-0.110。
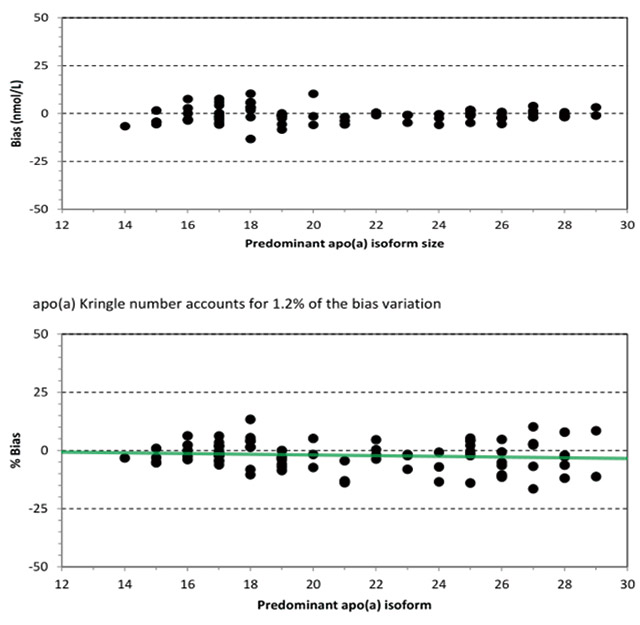
图9 罗氏检测出现的偏移与样品内主要的apo(a)异构体的关联
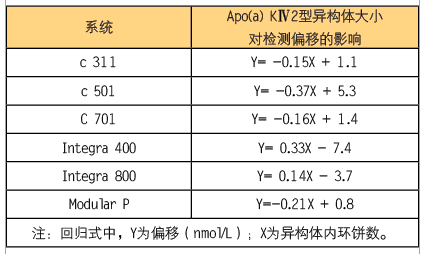
经过实验,确定各个罗氏仪器平台上,检测偏移与样品内apo(a)异构体大小的关系见表2。
表2 Apo(a)KⅣ2型异构体大小对检测偏移的影响
对所有罗氏仪器平台进行因样品内apo(a)异构体对检测偏移的影响的纠正。再次进行罗氏系统与Dr. Marcovina实验室检测比较,完全符合要求,因此,Dr. Marcovina出具了证实罗氏系统具有可溯源至Lp(a)参考系统的证书(见图10)。
以上资料充分说明,样品(校准品)内含有的 KⅣ内2型环饼的多寡(或重叠个数)对Lp(a)的检测有影响。在不同的罗氏的各个系统上,其实影响也是不同的。这就是为什么罗氏设计的特定软件系统对检测数据一致性的重要!

图10 罗氏检测系统检测Lp(a)溯源性证书
六、总结
1、严格而言,应该对不同系统有一个配合的校准品是最佳做法。可是这违背了罗氏长期来,每个分析物的校准品,在任何系统上只有一个值的做法。目前罗氏总部依然采用了所有系统校准值的总均值,作为Lp(a)产品的校准值,实验说明没有引入明显的误差。
2、一个专用软件用于为校准品组设定系统特异的Lp(a)值。该校准品组由5个独立混合血清组成,内含的Lp(a)水平范围从低到高,apo(a)大小范围从大到小。使用这个方式,六个不同系统得到Lp(a)水平,产生了一致和准确的值,并与以WHO/IFCC参考物质校准的ELISA参考方法得到的结果,具有可比性。在这些系统上的Lp(a)值,消除了apo(a)大小多态性的影响。
3、从现有资料上,其实罗氏公司从来没有直接使用过SRM 2B参考物质。这个物质制备时才只有2000支。完全依靠了Dr.Marcovina实验室。在她实验室中,SRM 2B校准它们的系统,由他们为公司提供了5份可溯源至SRM 2B和Marcovina的参考方法的新鲜人血清,作为罗氏建立自己的一级校准品和市售校准品的依据。我想罗氏公司也可以从这个产品的溯源性过程,对溯源性概念有了再次认识。
4、我对Lp(a)标准化关注了许多年。Dr.Dati是我的老朋友。在2003年,WHO/IFCC批准了Lp (a)后,我很快就知道了。为此也在我的书中做了较详细的介绍。但是,如果不是这次罗氏公司与我交流,我一直对Lp(a)在临床实验室的问题很灰心!一直使用mg/L,从不考虑使用nmol/L!实验室间的可比性很差!因此,10多年前的Lp(a)标准化似乎成了空白。这次罗氏提供的资料,其中有全世界著名的脂类标准化专家Dr.Marcovina的亲自参与,将罗氏6个不同系统的Lp(a)检测结果,真正实现了可比性。心中万分喜悦!
5、推出的好产品可以准确检测Lp(a)。但是,以往临床应用的文献,以mg/L表达的结果无法说明结果的可靠性。因此,我很期望国内在心血管疾病的研究和观察中,更多的使用罗氏LPA2系统产品。注意不是LPALX产品,因为该产品依然不是可溯源至SRM 2B的!
6、还有,在无法了解各个厂商的Lp(a)产品的可靠性前(指尚未可溯源至SRM 2B),千万不要去将各个其他公司的Lp(a)的mg/L结果,与罗氏的nmol/L比较!也不要随意将罗氏的nmol/L结果换算为mg/L,与其他公司产品的结果进行比较!因为,没有从根本上了解产品的可靠性前,这样的比对不仅没有意义,而且还会带来预想不到的反作用。必须谨慎。
7、在目前条件下,以罗氏的Lp(a)检测的免疫方法,可以报告nmol/L的结果,大致上与国际上正在追求脂蛋白颗粒的技术上。还可以比比。今后,我很相信,对于脂蛋白检测的结果,将一定会直接检测各类脂蛋白的颗粒!几年前的LDL-P已经被认可了。所以,Lp(a)的颗粒浓度一定会被大家认可。
声明:由于这项标准化的工作,是在罗氏公司内部发展的。公司没有任何公布的文献资料。因此请各位同道谅解。




