临床实验室检验结果自动审核的流程设计与临床应用

夏良裕,中国医学科学院北京协和医院检验科生化免疫专业组组长,副主任技师。研究方向:临床生物化学检验,临床实验室质量管理,实验室自动化、信息化、智能化。学会任职:第二届中国中西医结合学会检验医学专业委员会实验室信息智能化专家委员会副主任委员,中国医学装备协会检验医学分会临床检验装备自动化信息化学组委员,全实验室检测系统智能化学组委员,北京医学检验学会医学实验室与诊断产品质量管理分会委员,中国医学装备人工智能联盟检验医学委员会第一届委员。中国合格评定国家认可委员会(CNAS)医学实验室评审员。
检验报告是临床实验室工作的产品[1],为临床诊疗工作提供重要诊疗决策依据。ISO 15189:2012实验室认可第5.8、5.9条款要求实验室制定发布检验报告相关的程序性文件以对此过程进行控制,在发布报告前对结果进行审核,应综合考虑质量控制、比较历史结果并结合临床信息进行分析,以保证检验结果的准确性并在适当时对检验结果作出解释[2]。
保证检验结果的准确性是检验结果审核的首要任务。虽然结果审核属于分析后环节,但需要考虑检验的全过程,包括样本质量评估、质控情况、结果的合理性、仪器运行状态、干扰影响因素分析、与历史结果比较、不同项目关联性检查、与患者情况符合性分析等,以确保检测的准确性以及与患者情况的一致性。另外,随着新项目的日益增多,循证医学向个体化医学和精准医学的发展,临床对检验结果解释的要求也越来越迫切。检验指标不仅反映人体的生理病理状态,还与疾病的致病原因、发病机制、病程演变、用药敏感性、耐药、疗效和预后判断相关。当前临床检验专业分工细化,检验项目众多,每个指标均可能有不同的影响因素以及反映不同的生理病理状态,这种海量的知识,无论是检验人员还是临床医生,均不可能完全掌握。因此,需要由不同专业的检验技师、医师结合实际情况对检验结果作出必要的解释,以保证结果得到合理的应用,这已成为检验结果审核中一项重要和迫切的任务[3]。
检验结果的审核可分为人工审核与计算机审核二种方式。计算机审核又称自动审核或智能审核,目前对这两种说法没有明确的界定。自动审核指在遵循操作规程的前提下,计算机系统按照临床实验室设置的已通过验证的规则、标准和逻辑,自动对检测结果进行审核并发布检验报告成为医疗记录的行为。在此过程中,还与实验室预设的可接受标准相符的结果自动输入到规定格式的患者报告中,无需任何外加干预[4]。自动审核的应用是自动化检测技术与信息技术的快速发展的必然结果。随着检验新项目的不断增加,全自动分析仪、全自动检验流水线的广泛应用,临床实验室检测工作量不断增长,检测能力也快速提升,导致报告审核人员不足、TAT延长等。应用自动审核可有效缓解人力不足问题,提升工作效率,缩短TAT,提升检验报告质量[5-8]。
自动审核的特点在于计算机按照人为设定的规则执行结果审核,侧重于应用规则识别各种与结果准确性相关的信息,保证结果的准确性。自动审核程序主要签发无明显异常的结果,可提高工作效率,缩短TAT,同时起到质量保证作用。文献或工作中也有将自动审核称为智能审核,可以理解为自动审核程序及其中的流程设计和规则制定是人类智能的体现。严格来说,智能的程序应该具有学习的能力,而现在的自动审核程序多无学习能力。真正的智能审核要求计算机程序在人工设定规则的基础上具有一定的学习能力,在应用过程中可通过学习不断完善规则,具有较复杂的逻辑判断能力、综合分析能力,其审核的重点在于检验结果的解释并能给出适当的结论或建议。
一、检验结果自动审核应用现状
国际上,自20世纪80年代开始计算机自动审核逐渐应用于临床实验室生化、血细胞计数的结果审核[9-10],之后陆续有相关应用报道[11-15]。美国临床实验室标准化研究所(CLSI)于2006年发布了自动审核的应用指南AUTO10-A[16],框架性描述了自动审核的实施流程及对分析前、分析中、分析后自动审核关注要点。2013年西班牙临床生化和分子病理学会向646家实验室发放关于自动审核的调查问卷得到85家实验室回复,其中54家应用了自动审核,由此得出自动审核使用比率达到64%的说法并不准确,仅为13%的应答率似乎提示了自动审核的关注度并不高,在北美的临床实验室似乎有同样的情况[17],作者分析可能有3个原因:没有或有限的技术支持、信息系统无法执行复杂规则、并且缺乏自动审核实施流程与经验。CLSI关注到了相关问题,于2019年发布了新版自动审核指南AUTO15-ED1,新版指南从不同专业角度进行全面详细阐述,目的是使其更具有可操作性[18],以推广自动审核在实验室的应用。
国内自动审核的应用起始于2010年前后。虽然起步较晚,但近几年快速发展,应用涉及生化、免疫、血液、尿液、凝血等多个专业领域。国内专家组织编写的自动审核行业标准于2018年发布[4],以规范自动审核的应用。近几年国内实验室发表的自动审核相关研究文献数量显著增加,且有多位学者组织多中心研究[7-8, 19],推动了自动审核的应用。国内应用自动审核实验室的增长可能与实验室样本量快速增长、TAT要求时间短及自动化水平快速提升有关。另外,实验室信息系统(LIS)以及基于流水线的中间体自动审核软件的应用也起到了重要作用。笔者所在的北京协和医院检验科于2012年建立自动化流水线后引入中间体软件并开始测试自动审核,于2013年开始实施生化检验报告的自动审核,后续又在LIS系统开发了自动审核程序并将其应用扩展到多个专业。至2022年,实验室已在生化、免疫、临检多个专业应用自动审核签发检验报告,不同专业/项目自动审核通过率为30%~99%(表1),三个专业组自动审核样本数达到总样本量的一半。与国际上相似,目前国内自动审核应用多集中在大型医院。笔者与同行交流发现,虽然很多临床实验室希望实施自动审核的意愿强烈,但由于多种因素无法应用,其中的原因值得探讨。
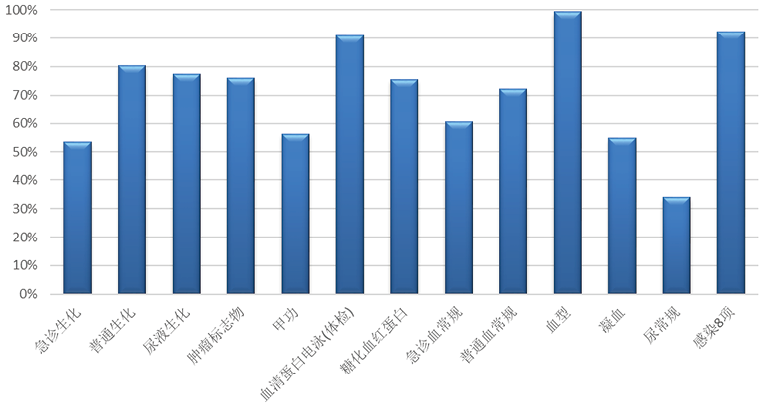
图1. 北京协和医院检验科不同专业/项目自动审核的通过率
二、检验结果自动审核设计与实践
1. 软件选择:当前临床实验室主要应用中间件或LIS实施自动审核。中间件多为全自动流水线设备的配置软件,是早期实施自动审核的主要软件。在实施过程中一般由厂商技术人员协助实验室进行参数设置。仪器将结果传输到中间件,计算机按设定的规则判断是否符合自动审核标准,接着由中间件将结果及自动审核标志传输给LIS,标记为通过的结果由LIS直接签发,未通过的结果由人工审核签发。通过中间件实施自动审核应用广泛,技术成熟,现阶段仍是临床实验室主要的自动审核方式,但其往往受仪器或流水线检测项目的限制,不能应用于实验室所有项目,而LIS实施自动审核者不受此限制。另外,LIS可实现跨专业检验项目关联判断,如检索血小板数量判断血清钾离子结果是否受其影响,检索红细胞压积用于判断确定凝血样本是否合格。近些年,国内多个LIS厂家已开发了自动审核系统,笔者实验室所用的LIS自动审核程序即由本实验室与厂家技术人员联合开发,可支持不同仪器、不同专业的检验结果自动审核。实验室可结合自身情况选择不同的软件实施自动审核,也可二者并用。
2. 流程设计:自动审核流程是支撑自动审核软件的骨架,表明程序在执行自动审核时关注方向与内容,由此可体现程序是否覆盖了对分析前、中、后各环节可能存在问题的全面判断,包括样本质量、质控结果、仪器运行状态、干扰影响因素分析、结果合理性判断,以及危急结果识别、历史结果比较、不同项目关联性比较、与患者情况符合性分析、项目完整性判断(少项或多项)等。程序根据流程中设置的所有节点对每个报告执行相同的判断,相比人工审核,自动审核的应用对检验报告审核具有标准化的效果。图2为笔者实验室生化免疫定量检验结果自动审核流程设计。本流程中判断样本性状通过仪器报警符号实现,如当检测乳酸脱氢酶(LDH)的样本出现溶血时,仪器通过血清指数判断样本溶血,并给LDH的结果后添加警告符号“h”(不同的仪器有类似的机制,报警符号可能不同),LIS的自动审核程序通过识别“h”判断样本溶血对LDH造成影响,该项目不通过。判断检验结果是否数字型可识别一些不合理的结果,如仪器传输错误输入的字符等;极限范围的设置可识别一些不可能的结果,如ALT的极限范围设置为0~1000,则可防止负值结果被自动审核。不同软件或不同专业可以设计不同的审核流程[5-8],但其中的审核节点应包含检验报告审核关键要点。在实施自动审核之前,实验室应了解软件的自动审核流程,确认其符合实验室有关检验报告审核的要求。
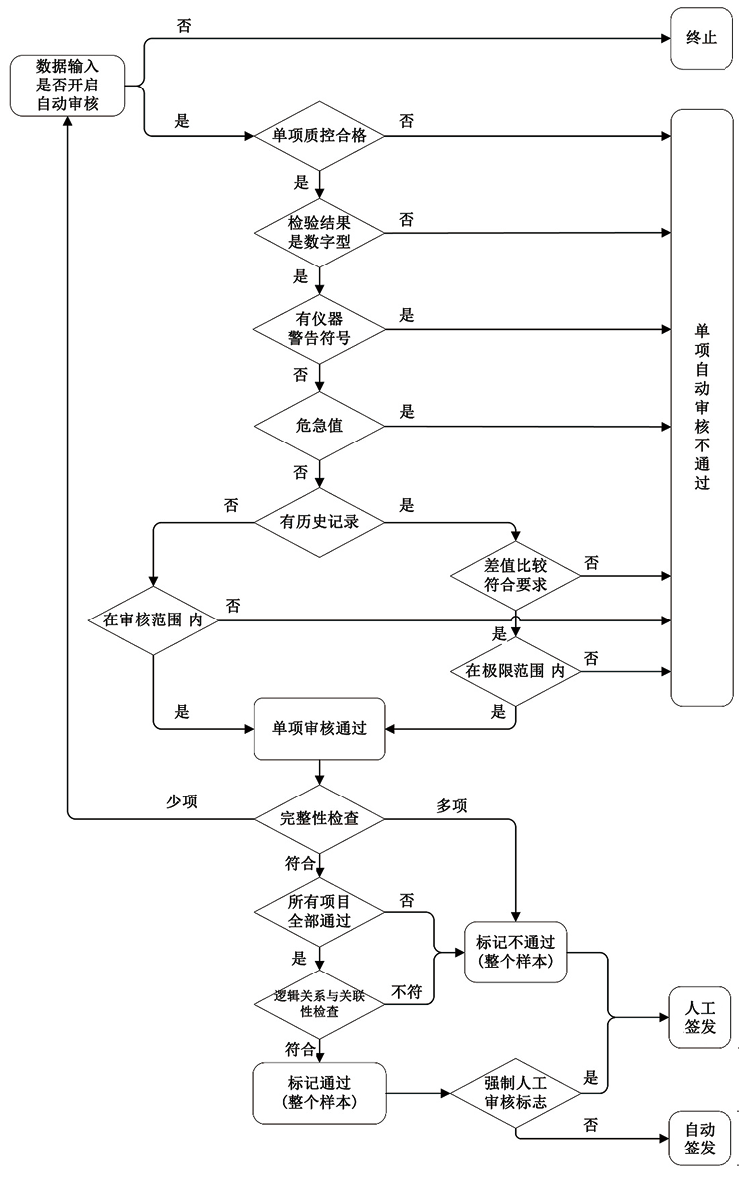
图2. 生化免疫定量检测项目自动审核流程示意图
3. 参数设置:定量检验项目自动审核的参数一般包括结果审核范围(verify limit)或审核区间(verification intervals)、差值检查范围(delta check)、逻辑关系、仪器报警信息、关联性检查等。参数设定是影响自动审核准确性和通过率的关键,也是实施自动审核的难点。
(1)审核范围:定量项目审核范围可以根据参考区间、医学决定水平、分析测量范围(线性范围)、危急值或其上下限的组合确定,也可以由实验室自行定义[4, 18],如根据所在实验室每个项目患者结果分布的百分位数确定,如果直接使用参考区间,自动审核通过率比较低,而使用分析测量范围则范围较宽,风险增大。笔者实验室应用百分位数法设定生化项目的审核范围[5],此方法统计简单,预期通过率可控,如预设ALT的单项目标通过率为90%,可设置5%和95%分位数为审核范围的上下限,后期可根据评估情况进一步调整,如调整为2.5%和97.5%分位数或1%和99%分位数,可提高单项通过率。定性检测项目,如感染类项可使用模型枚举法进行设定,乙肝病毒5项全阴性为一个可通过的模型,乙肝病毒表面抗体阳性的同时其他4项阴性为另一个可通过的模型。也可以使用排除法,如乙肝病毒表面抗原阳性不通过。
(2)差值检查范围:差值检查即同一患者历史结果的比较,用于判断患者结果变化是否合理。差值检查有助于识别在分析过程中任何阶段出现的错误。分析前错误常见原因包括样本量不足、样本标识错误(容器中的样本非标签所示患者)、静脉输液或静脉穿刺针或留置管中残留液体的污染以及使用不合适的采集管。分析中错误包括探针故障、凝块和纤维蛋白、仪器重要部件故障等,分析后错误包括转录错误、稀释因子计算不正确等[20]。病理生理变异相对较小的项目适宜设置差值检查,对于变异较大的项目,应用差值检查需要慎重,如血糖。差值检查范围可以设置百分差异或绝对差异,绝对差异的设置多适用于低值范围的结果。AUTO15提出必须设置历史结果比较的时间范围,示例最长时限为90天,超过设定时间范围的结果不进行判断[18]。笔者认为差值检查时间范围可默认与最近的一次结果比较,部分项目时间范围可放宽到1年以上,如血型结果的比较可不受时间限制。即使生化项目,时间限制也不宜太短,如对于体检者,大多数结果比较稳定,与一年前的数据进行比较仍有价值。差值检查允许范围可根据参考变化值(reference change value,RCV)、允许总误差设定,也可以参考文献或者根据实验室数据自行统计结果确定。差值检查的设定对自动审核通过率可产生较大影响,需要持续调整[21]。
(3)项目关联性:不同项目之间可能存在的某种关系称为关联性,应用关联性检查有助于识别分析全程因素对结果的影响。不同项目可以是由相同仪器或不同仪器检测或是不同专业的项目。有些关联分析可以直接设定,如总蛋白应大于白蛋白、总胆红素应大于直接胆红素、总胆固醇结果应大于高密度脂蛋白胆固醇与低密度脂蛋白胆固醇之和等;有些需要根据实验室数据统计可接受范围,如肌酐与尿素比值。跨专业的关联检查需要信息系统支持,如审核血清钾结果时宜判断血小板数量是否明显增高导致血钾假性增高[22],审核凝血结果时判断红细胞压积是否在合适范围内等。实验室也可通过文献检索或自行研究的方式设置不同的关联性检查。
(4)仪器报警信息:仪器报警信息直接反映了分析过程中的状态,是自动审核程序必须设定的参数。对于影响检验结果的提示信息必须识别,如危急结果、超过分析测量范围、提示样本量少、提示干扰、提示异常细胞等,另外一些信息可根据需要选择性识别,如提示超过参考区间或提示结果已复测的信息。
4. 性能验证:应用自动审核程序前必须进行验证。从应用层面来说,验证时只需要关注自动审核通过的报告,确认所有自动审核通过的报告不需要进行其他处理即可签发,即可证明自动审核的准确性。分析不通过原因有助于提高自动审核的通过率。首次使用自动审核程序前应对流程中的关键节点进行验证,如确认程序可识别危急值。验证一般由经验较丰富的工作人员执行,如专业组长、中高级职称的检验技师或医师。除了首次使用时进行验证,一般每年进行一次验证或在有程序变更时进行验证。各家实验室仪器设备、人员、样本量、工作模式不一样,因此很难以科学的方式明确验证所需要的例数或时间,笔者建议至少试运行1个月以上,以确认其准确性。试运行和验证时可将程序设置为只判断是否通过但不签发的模式,由人工进行二次审核后签发,这个过程有利于工作人员熟悉、接受新的审核模式。
四、自动审核的应用管理
检验报告审核是整个检验过程的最后一环,是检验报告到达医生和患者手里之前的最后一个质控节点,实验室应制定制度与文件对自动审核过程进行管理。管理的内容包括人员职责与授权、自动审核程序验证与应用培训等,应保证达到实验室的各项管理要求且符合ISO15189实验室认可的相关条款要求。
自动审核已经在我国各级临床实验室开展应用,对于提高工作效率、缩短TAT、提高报告质量均有重要作用。由于自动审核程序参数设置比较复杂,对技术人员要求较高等原因,该技术在临床实验室的使用率仍较低。要提高其在临床实验室的普及率,需要实验室相关领域的研究人员与信息系统厂商技术人员积极配合,开发更加简单易用的程序。应用自动审核应进行严格的验证评估,符合实验室风险管理及ISO15189条款的要求。
参考文献
Can CH, Vanstapel F, Thelen M, et al. Improving the laboratory result release process in the light of ISO 15189:2012 standard [J]. Clin Chim Acta, 2021, 522:167-173. DOI:10.1016/j.cca.2021.08.013.
ISO. ISO 15189:2012 Medical laboratories -Requirements for quality and competence [M]. 出版地?出版商?2012.
张曼. 检验医学第二次飞跃—检验结果分析与解释[J]. 中华医学杂志, 2018, 98(22): 2. DOI:10.3760/cma.j.issn.0376-2491.2018.22.001.
WS/T 616-2018 临床实验室定量检验结果的自动审核. 中华人民共和国卫生行业标准[M]. 2018.
夏良裕, 程歆琦, 刘茜, 等. 临床实验室生化免疫项目自动审核程序的建立与应用[J]. 中华医学杂志, 2017, 97(8): 616-621. DOI:10.3760/cma.j.issn.0376-2491.2017.08.012.
李映潼, 王学军, 续薇, 等. 血液分析自动审核的周期性验证及其应用适宜性评价[J]. 中华检验医学杂志, 2020, 43(10): 1021-1031. DOI:10.3760/cma.j.cn114452-20200326-00306.
曲林琳, 吴俊, 吴卫, 等. 凝血检验结果自动审核规则建立与验证的多中心研究[J]. 中华检验医学杂志, 2020, 43(8): 802-811. DOI:10.3760/cma.j.cn1144522020032600305.
张慧, 王学军, 樊爱琳, 等. 尿液分析自动审核规则的建立与多中心实践[J]. 中华检验医学杂志, 2020, 43(12): 1217-1224. DOI:10.3760/cma.j.cn114452-20200327-00313.
Valdiguie PM, Rogari E, Philippe H. VALAB: expert system for validation of biochemical data [J]. Clin Chem, 1992, 38(1): 83-87.
Davis g m j l M. Autoverification of the Peripheral Blood Count [J]. 1994, (8): 528-531.
Dorizzi RM, Caruso B, Meneghelli S, et al. The DNSev™ expert system in the auto-verification of tumour markers and hormones results[J]. Accreditation Quality Assurance, 2006, 11(6): 303-307. DOI:10.1007/s00769-006-0160-6.
Narayan T, Leonard B, Tracy N, et al. Process improvement and operational efficiency through test result autoverification[J]. Clin Chem, 2005, 51(12): 2406-2408. DOI:10.1373/clinchem.2005.054395.
Duca DJ. Autoverification in a laboratory information system[J]. Lab Med, 2002, 33(1): 21-25. DOI:10.1309/LXVB-12RU-F5EX-PU9W.
Oosterhuis WP, Ulenkate HJ, Goldschmidt HM. evaluation of LabRespond, a new automated validation system for clinical laboratory test results[J]. Clin Chem, 2000, 46(11): 1811-1817. DOI:10.1093/clinchem/46.11.1811.
Marchand M, Guibourdenche J, Saada J, et al. Real time validation of paediatric biochemical reports using the Valab-Biochem system[J]. Ann Clin Biochem, 1997, 34 (Pt 4): 389-395. DOI:10.1177/ 000456329703400409.
Instituteca LS. Autoverification of clinical laboratory test results: Approved Guideline. CLSI document AUTO10-A.[M]. 940 West Valley Road, Suite 1400, Wayne, Pennsylvania 19087-1898 UAS; Clinical and Laboratory Standards Institute. 2006.
BM. A step-by-step process to 95% autoverification. http://www.captodayonline .com /step -by-step autoverification . 2015.
(CLSI) C A L S I. Autoverification of Medical Laboratory Results for Specific Disciplines.1st ed. CLSI guideline AUTO15 [M]. 50 West Valley Road, Suite 2500, Wayne, Pennsylvania 19087 USA; Clinical and Laboratory Standards Institute. 2019.
王力, 郝晓柯, 杨大干, 等. 尿液常规智能审核规则验证与改进的多中心研究[J]. 中华检验医学杂志, 2020, 43(8): 794-801. DOI:10.3760/cma.j.cn114452-20191225-00751.
Markus C, Tan RZ, Loh TP. Evidence-based approach to setting delta check rules[J]. Critical Rev Clin Lab Sci, 2021, 58(1): 49-59. DOI:10.1080/10408363.2020.1800585.
朱晶, 王蓓丽, 郭玮, 等. 临床生化检验报告自动审核系统的规范化建立和优化[J]. 临床检验杂志, 2018, 36(9): 4. DOI:10.13602/j.cnki.jcls.2018.09.16.
张好良, 卢文雅, 侯立安, 等. 基于患者数据挖掘研究血小板数量对血钾的影响[J]. 临床检验杂志, 2022, 40(1): 71-73. DOI:10.13602/j.cnki.jcls.2022.01.17.




