非侵入式可穿戴动态血压连续测量技术的研究与临床应用价值

邢晓曼,中国科学院苏州生物医学工程技术研究所研究员。先后在中国科学技术大学、宾夕法尼亚大学学习及从事科研工作,研究生阶段师从著名物理学家Arjun G. Yodh。主要从事生理参数测量、可穿戴医疗设备研究,以血液动力学为背景,从临床实际需求出发,以关键技术为突破点,重点研究睡眠中动态生理参数(如动态血压)、糖尿病血管疾病的可穿戴多模态测量技术、核心参数提取以及基于临床大数据和人工智能的干预效果评估技术,从而构筑睡眠障碍及糖尿病整体化解决方案。先后主持4项国家重点研发计划子课题、1项双创人才计划;作为核心人员策划并参与1项国家重点研发计划及多项省市级项目。还与首都医科大学附属安贞医院、中国医学科学院北京协和医院、北京大学第六医院建立长期合作项目。
【摘要】血压是最重要的生命体征之一,与占据全因死亡率第一位的心血管疾病预后紧密相关,通过高血压早期筛查,可有效降低该类疾病的致残致死率,降低心血管意外的风险。可穿戴动态血压监测技术具有筛查窗口前移、临床环境外检测及无感舒适等多种优点,对促进高血压的知晓、治疗和长期管理具有积极意义。但是,目前相关创新技术存在一些固有问题,主要集中在测量稳定性、血压变化准确度、校准、机器学习可解释性以及算法泛化性方面,由于涉及到应用场景判断、置信度评估等,相关标准缺乏,难以获得医疗器械认证,降低了创新技术的可信度,加剧了推广的困难。虽然创新可穿戴血压测量技术暂不能替代袖带血压计进行高血压诊断和管理,但随着理论研究的深入和传感器技术的发展,这些技术仍具有很高的潜力,未来可供临床有条件使用。
【关键词】可穿戴;无袖带;动态血压;校准;机器学习
在1733年,Stephen Hales首次采用侵入传感器测量动脉血压并观察了其动态变化[1]。而血压测量的大规模普及始于1905年,Nicolai S. Korotkoff发展了基于Riva-Rocci袖带的柯氏听音法,能够同时测量收缩压和舒张压,建立了临床血压测量的标准[1]。但是袖带在充气过程中可能会引起患者焦虑和不适,影响测得的血压水平[2]。且袖带血压计仅能在静态条件下实现间歇性测量,无法测量快速和动态的血压变化,为血压的精细管理带来了一定困难。
无袖带可穿戴血压设备能够舒适、连续地记录血压,并检测到血压的快速变化。因为没有袖带的压迫,无袖带血压装置可以提供详细的动态血压模式信息,尤其是夜间血压趋势,无感测量不会干扰正常睡眠,数据更为真实。无袖带装置也可用于ICU或麻醉期间的连续血压监测,以及心律失常、低血压/晕厥等患者,辅助评估影响血压水平和变异性的瞬态条件。鉴于新型无袖带血压计的优点,不少研究人员、医生、患者都希望尽快能使用它们。但由于创新技术的复杂性,用户端很难深入理解技术原理,对它们的局限性和固有问题知之甚少。
一、不同类型的可穿戴动态血压测量技术
最近的一项澳大利亚在线市场的报告称,市面上现有500余种无袖带可穿戴血压测量设备,但没有足够的证据来确认它们的准确性[3]。2014年后,相关研究呈现爆发式增长,截至2022年10月,共有300余篇科学出版物在PubMed上发表,但这些研究中使用的方案,无论是参加人数、测量条件(静坐、活动、冷压测试、呼吸控制等)、参照血压(动脉内血压、诊室血压、动态血压)、统计方法(Bland-Altman、相关系数),还是参照标准(ISO 81060-2标准等),都存在相当大的差异性[4-15]。《2021欧洲高血压学会诊室及诊室外血压测量实践指南》和柳叶刀高血压委员会都表示,除非使用专门的标准对其进行充分验证,无袖带血压测量设备不应用于诊断或治疗决策[16, 17]。
表1. 不同可穿戴动态血压测量技术原理、代表设备、优劣势分析及相关证据
类别 | 方法 | 示意图 | 优势 | 劣势 | 证据 | ||
需要 校准 | 脉搏波传导时间 (PTT) | 无负荷、 无干扰 | 理论研究 较为深入 | 需校准、校准 易失效、对三 级高血压范围 内血压变化不 敏感 | 需至少两个 传感器 | 研究数据多、但鱼龙混杂 | |
脉搏波形分析 (PWA) | 单传感器、 微型化 | 敏感度不够、理论研究相对薄弱 | |||||
视频 (rPPG) | 可直接使用 手机摄像头 | 波形质量差 | |||||
心冲击图 (BCG) | 负荷低、可嵌 入智能床垫 | 受睡姿影响 | 研究数据少 | ||||
无需 校准 | 超声贴片 | 理论基础 扎实、无需 校准 | 血管弹性测量 | 传感器难以正确放置, 价格昂贵 | 处于研究阶段 | ||
容积钳制法 | 逐拍血压测量 | 手指有压迫感,价格贵、 不舒适,多为研究使用 | |||||
1. 需要用户校准的可穿戴动态血压测量技术:对于需要校准的技术来说,血压并非直接测得,一般需获得一个或多个变量与血压的映射关系。部分基于脉搏波传导时间(PTT),脉搏波形分析(PWA)的设备已被监管部门批准并已上市[7, 18],但目前不推荐用于临床[16]。由于需要个体化校准,当前还不清楚创新设备对校准的依赖性,以及校准后跟踪血压变化的能力[4],居家自我校准的规范性和准确性也可能存在问题。
(1)脉搏波传导时间法(PTT):PTT是不同躯体部位之间的动脉波形时间延迟,与主动脉弹性呈负相关[19]。PTT可以由心电图(ECG)和光电容积描记(PPG)之间的时间延迟来计算,也可以由心冲击信号(BCG)代替ECG来计算。采用ECG来计算PTT需要考虑电信号和心脏跳动的时间延迟,误差相对较大。手指 PTT跟踪收缩压比舒张压更稳定,但容易受到局部平滑肌收缩和交感神经活动的影响,导致不可预知的模型失效[19]。
(2)脉搏波形分析(PWA):PWA从脉搏波形中提取与血压相关的特征。它只需要一个传感器,但理论基础相对薄弱,目前主要依靠弹性腔模型及心血管数字模型[20-22]。仅依靠PWA不足以对血压进行精准预测,因为传感器对血容积的客观测量受多种因素影响(如图1),没有参照传感器可以做归一化处理,且存在信息丢失问题。当前比较好的算法需要考虑时间相关性,采用长短记忆模型的算法(例如飞利浦医疗)能够达到较好的血压趋势测量[23]。
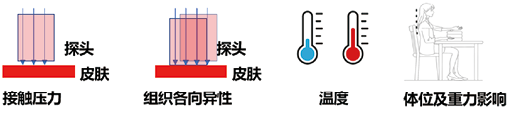
图1. 可穿戴动态血压主要影响因素
(3)人脸视频处理(rPPG):面部视频可通过RGB色彩分离,提取脉搏波形特征,与PWA技术类似[24]。然而,从视频获得优良的波形质量非常困难,光线的微小变化、化妆品等都容易掩盖心脏搏动的细节。此外,由于面部血管对温度非常敏感,它与PWA技术相比,提取血压的困难度更高。
(4)心冲击图(BCG):BCG通过测量颈部或四肢在心跳期间的震颤,反推心脏搏动的射血冲量和血压[25]。由于人体可被视为不同部位的连接,上臂、脊柱、腿部等连接部分对血流冲力而言,可视为弹性连接器和阻尼。多部位的力学耦合可被用来建立传感器波形输入和血压的映射关系。BCG测量容易受到体型、姿态等因素影响,但在特定体位的测量中,能够获得比PWA技术更为稳定的血压关联关系。

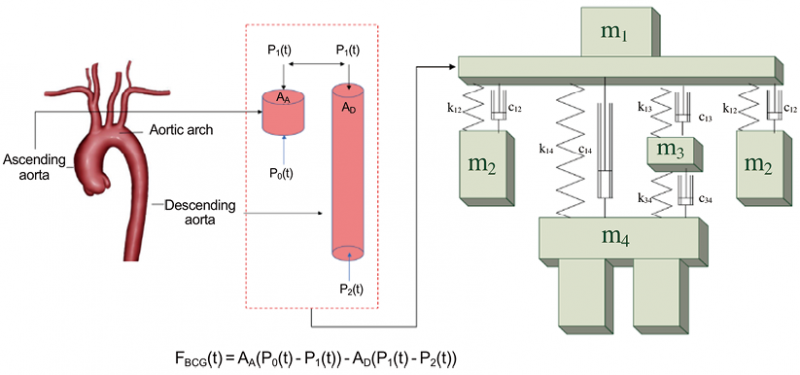
图2. 中心血管血流动力学模拟与躯体微振动的关联模型
2. 不需要袖带校准的技术:这与需校准的技术相比,不需校准的创新可穿戴血压测量技术尚处于早期,主要有超声和容积钳制法。
(1)超声:超声波能够很方便的测量血管横截面积和血流速度,其测量准确性优于PTT技术。血压计算基于流体动力学原理,比PTT技术准确度更高,且无需校准[26, 27]。虽然颈动脉超声贴片技术可能有利于心血管风险分级[28],其佩戴舒适性和位置容错性相比可穿戴腕表等技术略差,且经济成本更高。
(2)容积钳制法:容积钳制可能是目前唯一能进行逐拍连续血压监测的技术。虽然PTT,PWA等技术都能够测到逐拍的传感数据,但由于算法模型需考虑前后时间关联,实际上的血压监测分辨率远不能达到逐拍。容积钳制技术需在手指佩戴小型充气环,通过伺服控制持续施加外部压力,压制PPG幅值,使得一个心动周期内的血容量达到恒定,其反馈压力即为血管内动态压力。由于需要持续向手指施压,容易导致手指麻木,且逐拍血压的临床价值有待商榷,因此一般做科研用途,难以长期使用。
二、技术的预期用途
1. 不同应用场景及其研发重点:从临床的角度来看,重要的是要考虑无袖带动态血压监测的不同预期用途,以方便正确的使用。预期用途也必然会影响设备和算法的设计,以及可能需要的验证程序和准确度。
无袖带血压装置可能有不同的“预期用途”,例如(1)健康人的高血压筛查;(2)确诊高血压患者的长期随访;(3)住院患者短期持续血压监测(例如麻醉期间,或在重症监护室)。在前两种情况下,血压的绝对误差和趋势误差必须要小,需对标医疗用途的袖带血压计。在第三种情况下,血压测量需要能追踪生命体征的快速变化,以确保血流动力学稳定性。对于重症监护和手术期间的快速血压变化,小的血压变化(例如<10mmHg)可能是临床上相对重要性较低的,但是血压测量的采样率重要性较高,在特殊情况下需要考虑逐拍血压测量。
从研发重点来说,前两种情况需要梳理血压测量的理论,确保在不同的应用环境下干扰因素能够被正确的评估和考量。第三种情况需要重点考虑不同疾病的血流动力学建模,考虑心脏弹性、血流阻力、顺应性分布的差异性,可从数字模型优化血压评估算法。
2. 不同场景的无袖带动态血压测量标准:在过去的三十年里,AAMI、英国高血压协会、ESH和ISO已发布不少血压测量设备的临床验证协议[29, 30]。随着无袖带设备市场的快速增长,其评估标准已经不能满足市场需求。
首先,应针对场景应设计不同的验证流程。在麻醉或重症监护期间进行短期血压监测,应注重采样频率,以保证患者血流动力学的生命体征稳定,其测量准确度的容许范围应适当放宽;对于高血压的筛查和管理,测量频率的重要性偏低,应注重单次测量的准确性和校准的持久性和稳定性。
其次,对于动态血压测量,侵入式血压不同于听诊血压(后者给出更低的收缩压和更高的舒张压)[31]。跟踪血压变化是可穿戴设备的优势,也是最有问题的。它涉及血压升降不同的生理机制,可以通过体育锻炼(握拳、自行车、屈膝等)、冷压试验、缓慢呼吸、心算测试、Valsalva动作、药物(如硝酸甘油)诱导血压变化。IEEE和ISO标准未指定改变血压的干预措施,但为了尽可能还原真实场景,这些验证还是必需的[29]。
三、可穿戴动态血压测量技术潜在的问题
可穿戴动态血压监测设备由于采用不同的全新技术模态,大部分并不是直接测量,因此这些设备都存在或多或少的准确度和稳定性问题,这些问题在传统袖带式测量设备中很少出现,大部分都与理论不完善、信号传播链复杂等因素相关。如存在信息丢失,即使是最高级的机器学习算法也无法弥补[4]。
1. 校准和血压变化:大多数无袖带血压监测仪需要初始和定期校准,需要个人用户使用传统的上臂袖带血压计给出“定标”值[4],通过专有算法来调整动态测量值。问题是这些设备能否准确追踪生理血压波动,以及校准流程是否掩盖了算法的缺陷。定期重新校准并无严格的理论基础,可穿戴动态血压测量应用的环境极其复杂,环境温度、佩戴压力、是否服用特定食物、情绪等都有可能影响“校准因子”。因此,除非每一项影响因素都能够获得传感器客观测量,仅凭模型与金标准之间的差异,简单粗暴的用校准抹平是非常不合适的。因此,多传感器的模态融合将成为未来可穿戴动态血压测量的主流,而其适用场景(如专用于睡眠场景的血压测量)也将被严格定义。
2. 机器学习:机器学习使用已知的参数与血压做关联分析(年龄、性别、身高、体重等)。但基于人口学的数据来评估血压,猜测成分居多,在复杂多变的高血压诱因前,机器学习可能起到负面作用。举例来说,对于健康年轻人,仅凭年龄、身高、体重,就能获得与袖带血压计相关性达0.7的预测[4],但这个预测显然没有实际意义,因为人口学特征在短期内不会改变,但是血压会由各种诱因引发剧烈波动。
机器学习的使用需要严格的验证,遵循测试集和验证集的严格分离,与应用场景的严格匹配。最终其效果受到理论极限的约束,即信息从中心动脉压传递到传感器后,有多少信息熵丢失?保留的信息是否足以反推血压?一些前沿的信息学评估工具,可以被用来评估技术模态的理论瓶颈,减少产品开发的成本,少走弯路。
3. 数据呈现问题:由于没有广泛认可的验证无袖带动态血压设备的标准,相关研究多参照AAMI/ESH/ISO通用标准[30]。但对于含校准流程的设备来说,这个标准可能会掩盖算法本身存在的致命缺陷,可能会产生很强的整体相关性(图3 a),而个体内相关性可能接近到零(图3 b)[4]。因此无袖带血压趋势准确性是否达到一定的标准,可能比校准后整体血压误差更有参考意义。
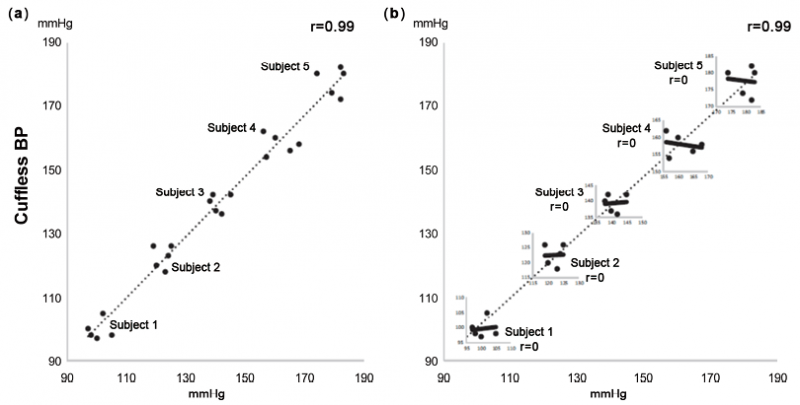
图3. 经校准的血压验证悖论,(a)整体高相关性;(b)针对个体的无相关性[4]
四、未来与展望
综上所述,无袖带可穿戴动态血压测量技术需要解决的核心问题在技术、验证程序、监管标准和临床用途,直接关系到医生和患者对于该技术的接受程度。最终,无袖带血压设备必须证明它们可以为健康人和高血压患者的管理和控制提供额外的价值。鉴于其特定的准确性问题,血压及血管健康数据应该是以更丰富的方式呈现。在此基础上,迫切需要发展国际公认的验证流程和标准,便于无袖带血压装置的认证。在此之前,在临床实践中应谨慎使用无袖带血压装置。期待若干年后,经过充分评估的可穿戴动态血压计可获得临床医生和用户的认可,持续改善当前的血压管理困境。
致谢:本项研究受到国家重点研发计划(2020YFC2003600,2018YFC2001100,2021YFC2501500),国家自然科学基金(62001470),山东省自然科学基金(ZR2020QF021),中国科学院青年促进会的资助。
参考文献
O'Brien E, Fitzgerald D. The history of blood pressure measurement. J Hum Hypertens, 1994. 8(2): p. 73-84.
Asayama K, et al. Nocturnal blood pressure measured by home devices: evidence and perspective for clinical application. J Hypertens, 2019. 37(5): p. 905-916.
Picone DS, et al. Nonvalidated home blood pressure devices dominate the online marketplace in australia: major implications for cardiovascular risk management. Hypertension, 2020. 75(6): p. 1593-1599.
Mukkamala R, et al. evaluation of the accuracy of cuffless blood pressure measurement devices: challenges and proposals. Hypertension, 2021. 78(5): p. 1161-1167.
Bilo G, et al.Validation of the Somnotouch-NIBP noninvasive continuous blood pressure monitor according to the European Society of Hypertension International Protocol revision 2010. Blood Press Monit, 2015. 20(5): p. 291-4.
Sola J, et al. Validation of the optical aktiia bracelet in different body positions for the persistent monitoring of blood pressure. Sci Rep, 2021. 11(1): p. 20644.
Vybornova A, et al. Blood pressure from the optical aktiia bracelet: a 1-month validation study using an extended ISO81060-2 protocol adapted for a cuffless wrist device. Blood Press Monit, 2021. 26(4): p. 305-311.
Degott J, et al. Smartphone based blood pressure measurement: accuracy of the OptiBP mobile application according to the AAMI/ESH/ISO universal validation protocol. Blood Press Monit, 2021. 26(6): p. 441-448.
Boubouchairopoulou N, et al. A novel cuffless device for self-measurement of blood pressure: concept, performance and clinical validation. J Hum Hypertens, 2017. 31(7): p. 479-482.
Ruiz-Rodríguez JC, et al. Innovative continuous non-invasive cuffless blood pressure monitoring based on photoplethysmography technology. Intensive Care Med, 2013. 39(9): p. 1618-25.
Schoettker P, et al. Blood pressure measurements with the optiBP smartphone app validated against reference auscultatory measurements. Sci Rep, 2020. 10(1): p. 17827.
Liu Z, et al. Continuous blood pressure estimation from electrocardiogram and photoplethysmogram during arrhythmias. Front Physiol, 2020. 11: p. 575407.
Miao F, et al. Multi-sensor fusion approach for cuff-Less blood pressure measurement. IEEE J Biomed Health Inform, 2020. 24(1): p. 79-91.
Chowdhury MH, et al. Estimating blood pressure from the photoplethysmogram signal and demographic features using machine learning techniques. Sensors (basel), 2020. 20(11).
Kachuee M, et al. Cuffless blood pressure estimation algorithms for continuous healh-care monitoring. IEEE Trans Biomed Eng, 2017. 64(4): p. 859-869.
Stergiou GS, et al. 2021 European society of hypertension practice guidelines for office and out-of-office blood pressure measurement. J Hypertens, 2021. 39(7): p. 1293-1302.
Sharman JE, et al. Lancet commission on hypertension group position statement on the global improvement of accuracy standards for devices that measure blood pressure. J Hypertens, 2020. 38(1): p. 21-29.
Harju J, et al. Comparison of non-invasive blood pressure monitoring using modified arterial applanation tonometry with intra-arterial measurement. J Clin Monit Comput, 2018. 32(1): p. 13-22.
Mukkamala R, et al. Toward ubiquitous blood pressure monitoring via pulse transit time: theory and practice. IEEE transactions on bio-medical engineering, 2015. 62(8): p. 1879-1901.
Natarajan K, et al. Photoplethysmography fast upstroke time intervals can be useful features for cuff-Less measurement of blood pressure changes in humans. IEEE Trans Biomed Eng, 2022. 69(1): p. 53-62.
Xing X, et al. Blood pressure assessment with in-ear photoplethysmography. Physiological Measurement, 2021. 42(10): p. 105009.
Charlton PH, et al. Modeling arterial pulse waves in healthy aging: a database for in silico evaluation of hemodynamics and pulse wave indexes. American Journal of Physiology-Heart and Circulatory Physiology, 2019. 317(5): p. H1062-H1085.
Radha M, et al. Estimating blood pressure trends and the nocturnal dip from photoplethysmography. Physiol Meas, 2019. 40(2): p. 025006.
Mukkamala, R., Blood Pressure With a Click of a Camera? Circ Cardiovasc Imaging, 2019. 12(8): p. e009531.
Yousefian P, et al. The Potential of wearable limb ballistocardiogram in blood pressure monitoring via pulse transit Time. Scientific Reports, 2019. 9(1): p. 10666.
Seo J, et al. Noninvasive arterial blood pressure waveform monitoring using two- element ultrasound system. IEEE Trans Ultrason Ferroelectr Freq Control, 2015. 62(4): p. 776-84.
Beulen BW, et al. Toward noninvasive blood pressure assessment in arteries by using ultrasound. Ultrasound Med Biol, 2011. 37(5): p. 788-97.
Vlachopoulos C, et al. Prediction of cardiovascular events and all-cause mortality with central haemodynamics: a systematic review and meta-analysis. Eur Heart J, 2010. 31(15): p. 1865-71.
Stergiou GS, et al. Validation protocols for blood pressure measuring devices in the 21st century. J Clin Hypertens (Greenwich), 2018. 20(7): p. 1096-1099.
Stergiou GS, et al.A universal standard for the validation of blood pressure measuring devices: Association for the Advancement of Medical Instrumentation/European Society of Hypertension/International Organization for Standardization (AAMI/ESH/ISO) Collaboration Statement. J Hypertens, 2018. 36(3): p. 472-478.
Picone DS, et al. Accuracy of cuff-measured blood pressure: systematic reviews and meta-analyses. J Am Coll Cardiol, 2017. 70(5): p. 572-586.




