基于患者数据质量控制系统的临床应用

夏良裕,副主任技师。现任中国医学科学院北京协和医院检验科生化免疫专业组长。澳大利亚皇家墨尔本医院访问学者。研究方向:临床生物化学检验、临床实验室质量管理、实验室自动化、信息化、智能化。学会任职:第三届中国中西医结合学会检验医学专业委员会实验室信息智能化专家委员会副主任委员,中国医学装备协会检验医学分会临床检验装备自动化信息化学组委员,全实验室检测系统智能化学组委员,北京医学检验学会医学实验室与诊断产品质量管理分会委员,中国医学装备人工智能联盟检验医学委员会第一届委员。中国合格评定国家认可委员会(CNAS)医学实验室评审员。
当前,临床实验室主要通过检测外部质控物质监控检测系统的质量,通常称为室内质控。室内质控是一种经典的质量控制方式,广泛应用于临床实验室。但其也存在一些无法克服的缺陷,主要包括:(1)只能监控分析中的误差因素,不能评估分析前因素;(2)需要购买特定的质控物质,具有一定的经济成本,某些项目没有质控物质;(3)质控结果不仅受检测系统本身影响,也可能受质控物的基质、配制方式、保存条件、人为处理方式的影响,在有些情况下不能真实反映检测系统的问题;(4)质控物质定时检测,不能实时监控检测系统。
为了弥补传统室内质控的不足,临床实验室开始研究应用患者数据实施质量控制,称为基于患者数据的质量控制(Patient based Quality Control,PQC)。广义上说,应用患者数据分析检验结果是否可靠的方法都属于PQC的范畴。例如审核报告时分析检验项目本次结果与上次结果的变化是否符合疾病的一般变化规律;分析两个或者多个项目之间的关系,例如血肌酐与尿素变化方向是否一致等。这些方法可以统称为传统的患者数据质控方法,较大程度上依赖于工作人员的经验,效率比较低。
1965年,Hoffmann和Waid首先将统计分析患者数据作为质控的方法引入实验室,即“正常均值法”(Average of Normal,AoN),其方法为:在每天工作结束时,统计该项目在正常范围内数据的平均值,并与历史累积的均值及控制范围比较,确认是否失控[1]。AoN可以认为是现代PQC的最初形态。相比于传统的患者数据质控方法,AoN的质量控制思路转移到分析数据分布规律上来,这是区别与传统室内质控和传统PQC的最大不同。
基于分析患者数据分布的质量控制方法可以称为一类新的质控方法,其基本思想是基于特定群体数据分布的稳定性,即某一群体某个检验指标的变异在一定范围内波动。这种变化主要由个体内变异、个体间变异和分析变异组成。在某些特定的群体,某些检验指标的结果变异在一个可预知的范围内,当其变异超过某一范围时,需要考虑某个或某几个变异来源发生了变化,对于已经确定的特定群体,个体内变异与个体间变异认为是可预知的,而剩下的变异即来源于分析过程或分析前过程。由此可见,监控特定的稳定群体的数据变异实际是监控分析前和分析中的变异。在实践中,我们根据时间的变化将监测值绘制到统计控制图上,判断是否超过控制范围。时间范围的长短选择决定了误差检出的时效性。
随着计算方法的增多,在AoN的基础上,又衍生出多种PQC模式,包括BULL法或称移动均值法(Moving Average)[2]、指数加权移动均值法(Exponentially Weighted Moving Average,EWMA)[3]、移动中位数法(Moving Media)[4]、移动百分位数法(Moving Percentile)[5]、移动标准差(Moving Standard Deviation)[6]、移动异常值法(Moving Number of Positive Patients)[7]。近几年,随着计算机技术的快速发展,PQC又进一步发展为基于患者数据的实时质控(PBRTQC)[8],用以对患者数据执行实时监控,误差检出的时效性进一步提高。
一、基于患者数据质控的一般模型
PQC的常用质控图模型与传统室内质控Z分数图类似,以时间为横坐标,患者结果与质控结果为纵坐标。PQC质控图也需要设定中心线和上下控制线。根据移动步长不同,PQC质控图的质控点数量差异很大。例如每日均值质控图每天仅有一个计算值作为监控点(图1)。如果实施实时监控,则每一个患者结果都会产生一个计算值作为监控点(图2)。
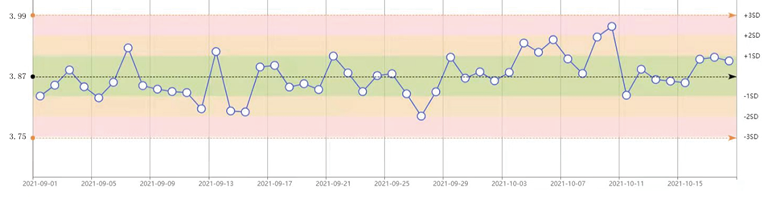
图1. K离子测定结果每日均值质控图
 患者原始结果,
患者原始结果, 指数加权移动均值。中心线:139.7,上下控制限分别为:142.7和136.7,上下排除限值为145和132。权重因子为0.2。
指数加权移动均值。中心线:139.7,上下控制限分别为:142.7和136.7,上下排除限值为145和132。权重因子为0.2。
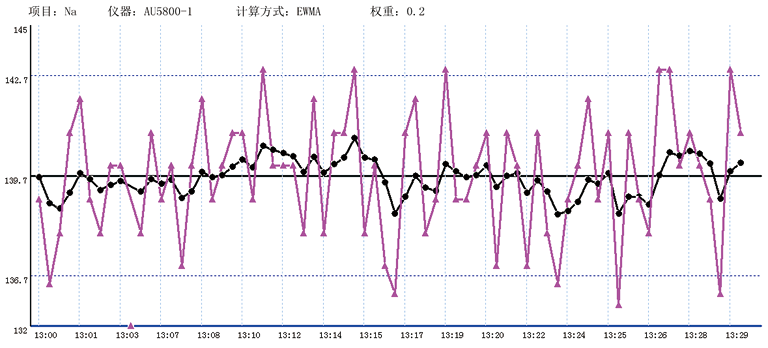
图2. Na离子患者结果实时质控图(EWMA法)
二、基于患者数据质控的实施流程
应用PQC的一般步骤包括:(1)购置或开发软件;(2)确认实施PQC的项目;(3)数据分析与处理;(4)选择监控群体;(5)选择计算方法;(6)参数评估与优化。
1. PQC应用软件系统:PQC系统的运行高度依赖计算机程序,实验室需先购买或自行开发程序软件。程序可以基于中间体软件或实验室在用的信息系统(LIS)开发。
2. 项目选择:当前研究的PQC系统主要应用于定量检验项目,其识别误差的效能主要受项目结果分布特点影响。存在以下情况的项目可优先考虑应用PQC:没有室内质控物质,受分析前因素影响较大,试剂稳定性较差,试剂批间差较大,质控物易产生基质效应,在分析过程中易出现故障。患者数据呈正态分布、变异小的项目应用PQC效果较好。
3. 数据分析处理:检验结果分布特点分析是选择计算方法及进行参数设置的前提。不同医院的就诊人群不同,即使对于相同项目,其数据分布特点也可能完全不同。因此,每个实验室需要根据自身的数据特点设置参数。
数据分析的内容包括数据分布形态以及数据变异大小和变异的来源。数据变异的来源包括年龄、性别、就诊类型(门诊、住院、体检,平诊或急诊)、疾病类型、样本来源科室及其他可影响数据分布的因素。
数据处理:(1)数据剔除:采用算术均值法或指数加权移动均值法需要设置剔除范围,以减少极端值的影响。超出剔除范围的数据可以直接丢弃或者采用截尾的方法处理。移动百分位数法、移动标准差法、移动比率法一般不需要设置剔除范围。(2)数据转换:非正态数据可通过Box-Cox转换使数据接近正态分布。对于有明确影响因素的数据可以通过回归调整的方式减少特定因素对数据变异的影响[9],例如通过回归的方式减少性别因素对血肌酐变异的影响。
4. 监控对象筛选:筛选的目的在于控制数据变异,选择数据稳定(数据变异小)的群体作为监控对象,例如选择监控体检人群的检验结果,或只监控门诊人群检验结果。也可通过排除方法进行筛选,例如排除重病医学科来源的数据,因为该科室均为重症患者,其数据变异往往显著大于其他人群。
5. 计算方法的选择:(1)移动步长(block size):或称移动窗宽,意为用于单次计算的样本量。步长越大有利于发现较小的变异,而较小的步长有利于更早发现较大的误差[8]。(2)移动方式:批量移动和实时移动。批量移动指按照确定的步长分段计算,实时移动指每产生一个数据计算一次。例如对于X1-X100这100个按时间顺序排列的数据,以20为步长计算移动算术均值。批量移动计算的方法为:
实时移动计算方式为:
实时移动比批量移动方法数据利用效率更高,误差检出时效性更好。(3)计算方法:当前常用的计算方法有移动算术均值法、指数加权移动均值法、移动百分位数法、移动标准差法、移动比率法。① 算术均值法:计算设定步长数据的算术平均值。② 指数加权移动均值法[3]:计算公式为:Zn = λ·Xn+(1-λ)·Zn-1。Zn为第n个样本结果对应的指数加权移动均值,Xn为第n个样本的原始结果,Zn-1为n-1号样本对应的指数加权移动均值,λ为权重指数。Zn是由Zn-1与Xn分别以1-λ和λ为权重合成的结果,前面样本的结果所占的权重以指数级递减。在实际应用时,可以将总体均值作为Z0计算Z1。λ取值在0-1之间,较小的λ(例如0.2)意味着当前结果所占比重小,检出误差的特异性较高,但时效性不如较大的λ,即灵敏度相对降低。③ 移动百分位数法:计算设定步长范围内所有结果的特定百分位数,常用中位数。④ 移动标准差法: 计算设定步长范围内所有结果的标准差。⑤ 移动比率法: 计算设定步长范围内高于或低于设定界值数据所占的比率。例如统计每100个心肌肌钙蛋白I测定结果中高于参考区间上限样本所占的比率,或统计每200个乙肝病毒表面抗原测定结果中阳性结果所占的比率。
6. 控制范围:为监控上述计算结果是否在控,需要设置控制上下限。此范围可以结合历史数据(训练数据集)确定。确定控制范围首先要保证假阳性率在可接受的范围内。应用训练数据集中最大和最小的计算值作为控制范围能较好的满足这一条件[10],也可以结合项目的允许总误差及监控量值的变异大小进行计算。
7. 性能评估与优化:通过以上步骤对训练数据集的分析,可得到以下三个方面的参数:(1)质控图参数:中心线和上下控制线;(2)数据处理相关参数(人群筛选条件,纳入或排除标准,数据是否转换及转换方法,包括回归计算方法);(3)计算方法参数(计算公式,移动步长或权重因子)。每一组参数的组合称为一个模型。
在临床应用前需对模型进行评估,主要包括2个方面:特异性和敏感性。特异性可通过统计假阳性报警率(False Alarm Rate,FAR)评估,计算公式为FAR=假阳报警数/总样本数。评估灵敏度的指标为误差检出所需样本数(Number of Patient until Error Detection,NPed),包括平均NPed(ANPed)、中位数NPed(MNPed)或95%位点的NPed(95NPed)。制作偏倚检测曲线图可比较直观地观察模型的灵敏度(图3)[10]。
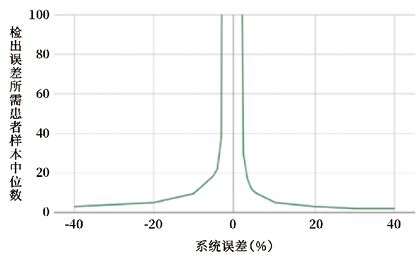
图3. 偏倚检测曲线图
模型优化的目的在于提高特异性和灵敏度。提高特异性的方法有:扩大控制限,严格人群筛选标准,缩小数据纳入范围,扩大步长或缩小权重因子。提高灵敏度采用的方法与提高特异性正好相反。在应用早期,首先应保证特异性,使假阳性率应尽量接近于0,特异性太低易出现报警疲劳而导致PQC系统不易推广。
三、 基于患者数据质控的临床应用
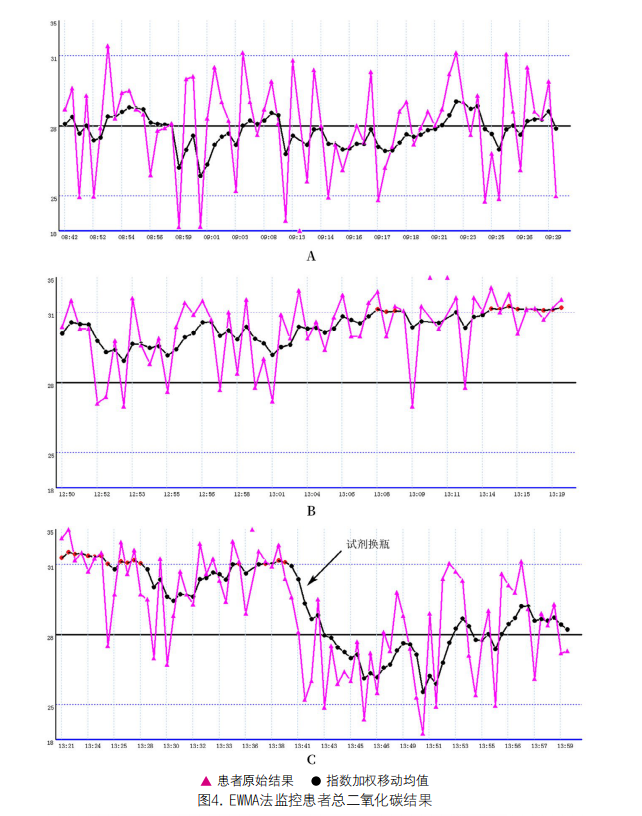
患者数据质控系统应结合传统室内质控应用。PQC系统仅可呈现患者结果出现了的偏移,但它不能提供产生系统误差的原因。当PQC系统出现报警时,首先应排除是否由于特定人群数据集中检测导致,例如连续检测一批糖尿病患者的科研样本可能导致PQC图形上血糖结果呈现整体偏高。接着可通过以下步骤确认系统误差是否存在:(1)加做室内质控;(2)分析检验前影响因素;(3)仪器间比对或留样再测;(4)结合患者病情分析。若确认存在系统误差,需进一步分析原因。图4为EWMA法实时监控患者总二氧化碳结果质控图,A图显示为上午9:00左右,患者数据及EWMA结果均匀分布在中心线两侧,未发现异常。B图显示13:00左右,患者数据与EWMA结果均呈现系统性偏高,13:00之后EWMA值超过控制上限。C图显示13:40后患者结果与EWMA均恢复正常。经调查,13:40仪器自动切换二氧化碳试剂瓶。此次失控原因为二氧化碳试剂问题。
除了应用于监控分析过程中的系统误差,PQC系统也可应用于监控实验室内仪器间结果的一致性,其前提为临床样本在不同分析仪间随机分配。无论是每日均值(图5)还是实时移动均值(图6)都能用于仪器间结果一致性监控。传统方法通过定期比对监控仪器间结果一致性,工作量大、需要一定的经济成本、效率低下且问题检出滞后。PQC法不但方便快捷,不需要额外的经济成本,而且监控效率高,甚至可进行实时监控,是一种经济高效的比对方法。
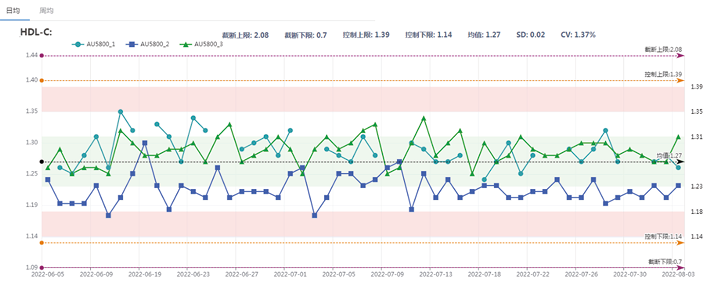
图5. 每日移动均值法比较三台仪器检测HDL结果的一致性
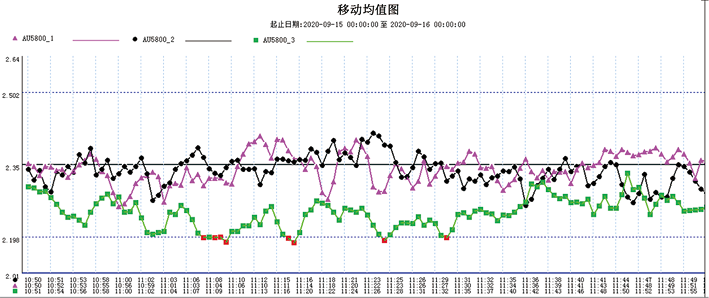
图6. 实时指数加权移动均值法监控3台仪器测定血清总钙结果的一致性
在临床实际应用过程中,PQC模型的设置和参数优化过程比较复杂,需要借助专门的计算机程序以及有计算机背景知识的专业人员与检验专业人员配合才能完成。另外,由于不同医院的患者人群存在差异,同一模型不一定适用于不同医院的实验室,也就是每个实验室可能都需要制定本实验室特定的模型,这加大了PQC系统维护和推广的难度。尽管如此,实验室还是可以通过以下方法逐步推进PQC的应用:(1)首先可应用简单的方法:例如每日均值法,每日异常结果比率法;(2)在应用的早期可设置较宽的控制限甚至不设置控制限。这样的PQC系统可用于观察趋势性变化,对于回顾性分析有很大帮助,后期逐渐调整参数,提高检出特异性和灵敏度;(3)先应用于数据分布接近正态、变异小的项目,例如电解质项目;(4)先用于监控有一定样本量,而且变异小的群体,例如体检人群;(5)设置模型参数时,早期可以设置较大的移动步长或者较小的权重因子(仅在应用EWMA法时有效,例如权重因子小于0.2),在应用的过程中逐渐缩小步长或扩大权重因子。
小结:PQC是一种有效的质量控制方法,不仅可用于监控单个分析设备的系统误差,还可识别分析前影响因素,也可用于监控实验室内不同分析设备间检验结果的一致性。PQC系统可设置多种计算方法实施数据监控,不同计算方法和参数设置可影响系统的检出效能。如何方便快捷地根据每家临床实验室的数据特点选择或制定PQC系统的计算方法与参数是当前需要解决的首要问题。
参考文献
Hoffmann R G, Waid M E. The "average of normals" method of quality control [J]. Am J Clin Pathol, 1965, 43(2): 134-41.
BULL B S, ELASHOFF R M, HEILBRON D C, et al. A study of various estimators for the derivation of quality control procedures from patient erythrocyte indices [J]. Am J Clin Pathol, 1974, 61(4): 473-81.
Linnet K. The exponentially weighted moving average (EWMA) rule compared with traditionally used quality control rules [J]. Clin Chem Lab Med, 2006, 44(4): 396-9.
Bietenbeck A, Thaler M A, Luppa P B, et al. Stronger Together: Aggregated Z-values of Traditional Quality Control Measurements and Patient Medians Improve Detection of Biases [J]. Clin Chem, 2017, 63(8): 1377-87.
Duan X, Wang B, Zhu J, et al. Assessment of patient-based real-time quality control algorithm performance on different types of analytical error [J]. Clin Chim Acta, 2020, 511(329-35.
Liu J, Tan C H, Badrick T, et al. Moving standard deviation and moving sum of outliers as quality tools for monitoring analytical precision [J]. Clin Biochem, 2018, 52(112-6.
Liu J, Tan C H, Badrick T, et al. Moving sum of number of positive patient result as a quality control tool [J]. Clin Chem Lab Med, 2017, 55(11): 1709-14.
Badrick T, Bietenbeck A, Cervinski M A, et al. Patient-based Real-Time Quality Control: Review and Recommendations [J]. Clin Chem, 2019, 65(8): 962-71.
Duan X, Wang B, Zhu J, et al. Regression-Adjusted Real-Time Quality Control [J]. Clin Chem, 2021, 67(10): 1342-50.
Van rossum H H. Moving average quality control: principles, practical application and future perspectives [J]. Clin Chem Lab Med, 2019, 57(6): 773-82.




