尿液分析系统用质控物的研制与临床应用价值
【摘要】目的 制备一种尿液分析系统用质控物,能同时应用于尿液干化学分析仪和尿液有形成分分析仪的质量控制。方法 以健康家猪的血液为原料,提取分离白细胞与红细胞,分别对细胞进行固定化操作,再与尿液干化学分析用质控液混合得到尿液分析系统用质控物。使用尿液分析系统测试干化学结果同时观察有形成分的形态,并按行业标准中推荐的方法评价质控物的均匀性、稳定性和基质效应。结果 尿液分析系统用质控物中的红细胞、白细胞形态与临床样本近似,在仪器上能够稳定识别。各项指标符合行业标准,稳定期能达到6个月以上,且无明显的基质效应。结论 制备的尿液分析系统用质控物包含14项尿液干化学质控项和2项尿液有形成分质控项,能同时满足用户端对于尿干化学和尿液有形成分分析的质控需求,具有良好的分析性能与稳定性,在尿液分析系统的临床应用上具有相当的价值。
【关键词】尿液分析;质控物;干化学;细胞
尿液分析主要包括尿液干化学成分分析与尿液有形成分分析。尿液干化学成分检测的方法有:手工镜检、干化学分析法、干化学分析仪等。尿液有形成分检测的方法有:手工镜检、流式细胞仪、尿液有形成分分析仪等[1]。上述各项检测方法除手工镜检外,其余检测方法均有室内质量控制的需要,以确保仪器、试剂组成的检测系统所得出结果的可靠性和准确性。近年来,尿液分析检验系统应用日趋广泛,尿液干化学分析仪与尿液有形成分分析仪共同组成的分析系统也逐步进入了人们视野。尿干化学和有形成分的测试在仪器端实现了整合,但在很多情况下尿干化学和有形成分还是各自沿用原系统的质控物,这就造成了用户在评价一个测试系统时需要使用两套甚至两套以上的质控物,使用的过程中较为不便。为进一步提高用户的满意度,在系统的质控监控上力求做到一站式地解决问题,我们研制了同时包含14项尿液干化学质控项(维生素C(VC)、亚硝酸盐(NIT)、微白蛋白(MA)、白细胞(WBC)、肌酐(CR)、酮体(KET)、尿胆原(URO)、胆红素(BIL)、葡萄糖(GLU)、蛋白质(PRO)、尿比重(SG)、隐血(BLD)、酸碱度(pH)、尿钙(Ca))和2项尿液有形成分质控项(红细胞、白细胞)的尿液分析系统用质控物,并在尿液有形成分分析仪上评价其分析性能、稳定性与基质效应,从而评估其应用价值。
一、材料与方法
1. 材料:(1)质控物制备使用原材料:猪血(桂林海源生物),尿干化学质控液。(2)仪器与试剂:离心机;甲醛(西陇科学);牛血清白蛋白(伯奥);全自动尿液有形成分分析仪;全自动尿液分析仪;显微镜(日本Olympus公司)。
2. 方法:(1)尿液分析系统用质控物的制备:取猪血进行离心后分离出纯净的红细胞和白细胞,用甲醛固化剂分别将两种细胞进行固化,完成后用牛血清白蛋白溶液将多余的固化剂去除,再将制备得到的红细胞和白细胞两种原料细胞分散于尿干化学质控液中,充分混匀后分装密封,得到尿液分析系统用质控物,保存温度为2~8℃。(2)质控物分析性能的评价:对尿液分析系统用质控物的均匀性与赋值准确性进行研究,测试方法参照中华人民共和国医药行业标准《YY/T 0501-2014 尿液干化学分析质控物》和《YY/T 1530-2017 尿液有形成分分析仪用控制物质》进行。① 均匀性研究方法和要求:尿干化学质控项重复测试的所有结果与参考区间一致性程度应为100%,RBC、WBC的瓶内均匀性满足CV≤15%,瓶间均匀性良好,满足F值≤F(0.05,ν1,ν2),即F≤2.39。② 赋值准确性研究方法和要求:尿干化学质控项测试结果与质控物参考区间一致性程度应为100%,对质控物RBC、WBC的镜检计数结果应在质控物参考区间中间值的±15%范围内。(3)质控物稳定性的评价:对尿液分析系统用质控物各项参数的变化趋势进行研究以评价其稳定性。参考《YY/T 1530-2017 尿液有形成分分析仪用控制物质》中稳定性研究的方式,在质控物配制完成后的第0个月、第2个月、第4个月、第6个月和第8个月对质控物进行取样测试。其中尿液干化学质控项的通过与质控物参考区间比对一致性进行评价;尿有形成分质控项则采用方差分析,计算概率(P)值,在95%的置信水平,P≥0.05表示趋势不显著,稳定性良好。(4)质控物基质效应的评价:在全自动尿液有形成分分析仪上测试尿液分析系统用质控物,比较红细胞和白细胞与临床样本形态的差异,并以镜检法作为比对方法,依据《WS/T 356-2011 基质效应与互通性评估指南》对质控物的基质效应进行评估。
二、研究结果
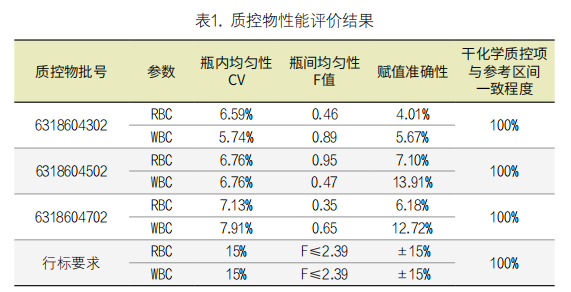
1. 质控物分析性能评价结果:按上文所述的方法制备了三个批次的尿液分析系统用质控物,其分析性能评价的结果如表1所示。可见各批次质控物的瓶内均匀性、瓶间均匀性与赋值准确性均满足行业标准的要求。各干化学质控项的测试结果均与参考区间保持100%的一致性,细胞组分不会影响干化学质控项的测试结果。
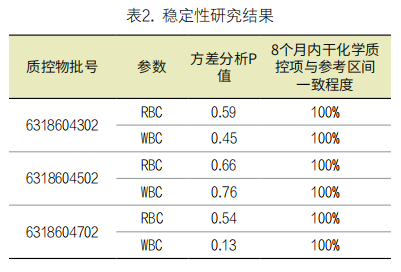
2. 质控物稳定性评价结果:对各批次质控物在配制完成后第0个月、第2个月、第4个月、第6个月和第8个月的测试值进行方差分析,结果如表2所示。可见各批次质控物干化学质控项测试结果均与参考区间一致,红细胞和白细胞的测试结果在95%置信水平,均满足P≥0.05,说明质控物测试值变化趋势不显著,稳定性良好。
3. 质控物基质效应评价结果:尿液分析系统用质控物与临床样本的红细胞、白细胞在全自动尿液有形成分分析仪上的测试图像对比如图1所示。可见尿液分析系统用质控物中红、白细胞的形态与临床尿液中的红、白细胞形态相近,因而在尿液有形成分分析仪和显微镜下,均可被稳定地识别。

注:1. 临床尿液样本红细胞;2. 尿液分析系统用质控物红细胞;
3. 临床尿液样本白细胞;4. 尿液分析系统用质控物白细胞
图1. 尿液有形成分分析仪上红细胞和白细胞测试图像
按《WS/T 356-2011 基质效应与互通性评估指南》对尿液分析系统用质控物的基质效应与互通性进行了评估,评估项目为红细胞和白细胞计数。以行标《YY/T 1530-2017 尿液有形成分分析仪用控制物质》中要求的溯源方法—镜检法作为比对方法,以全自动尿液有形成分分析仪测试法作为评估方法,同步分析临床样本与制备的质控物样本。以比对方法即参考方法测定结果为x值,评估方法测定结果为y值,将样本测试的结果作出散点图。采用线性回归的方法对数据进行分析。以临床样本测试结果拟合出回归曲线,再根据该曲线计算出每个x值对应的y值,以及给定x值下临床样本评估方法测定均值y的双侧95%置信区间。用各个临床样本y值的95%上限结果和95%下限结果,与x值线性拟合得到两条回归曲线。以上述回归曲线和各临床样本、质控物的测试结果作基质效应分析图如图2和图3所示,可见质控物测试的散点均落在临床样本 值与对应的 值的95%预测区间的回归线范围内,说明尿液分析系统质控物无明显的基质效应存在。
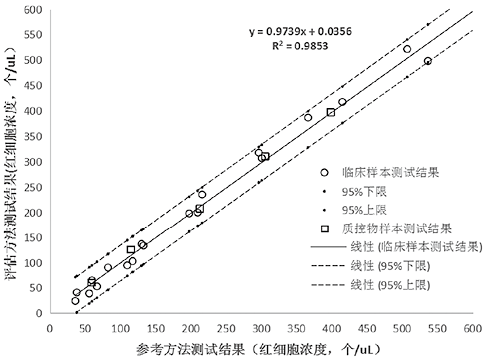
图2. 红细胞计数基质效应分析图
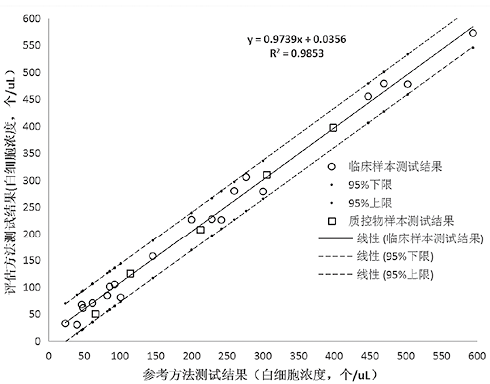
图3. 白细胞计数基质效应分析图
三、分析与讨论
本研究上述研究结果说明,我们研制的尿液分析系统用质控物均匀性、赋值准确性良好,能满足现行行业标准的要求,在8个月的稳定性观察中各项参数无显著变化,同时具有与临床样本相近的性质,能同时应用于显微镜检查与尿液分析系统测试,无显著的基质效应。尿液分析系统用质控物可以同时应用于尿液干化学和尿液有形成分分析的质量控制,具有相当的临床应用价值。
尿液分析系统用质控物由尿干化学质控液与猪红细胞、猪白细胞共同组成,因此其分析性能在很大程度上受两大类组分共存性的影响。干化学质控液中的酯酶、酮体等物质可能破坏细胞的结构从而影响其稳定性,需要通过固化细胞的手段来使细胞结构稳定化,在干化学质控液中能维持其形态从而保证在仪器下的识别率与测试准确性。相对地,细胞固化时使用的试剂如醛类不可避免地会有部分残留,这些组分也有可能对尿干化学质控项的测试产生一定的干扰。在尿液分析系统用质控物制备的过程中对红、白细胞进行了充分的固化之后,再利用过量的蛋白类试剂与剩余的固化剂进行反应,这样既能保护细胞不受干化学质控液中酯酶等组分的破坏,又能避免过量的固化剂干扰尿干化学组分的稳定性,使尿液分析系统用质控物的两种组分能够长时间共存。这种研究思路还可进一步应用于尿液系统用质控物增加管型、上皮细胞和结晶等质控项的研究中去,从而进一步扩宽尿液分析系统用质控物的质控范围,使之能够更加全面、完善地评价尿液检测系统的运行状态与分析性能,这也是尿液分析系统用质控物未来的发展方向。
参考文献
[1] 张时民编著. 实用尿液有形成分分析技术. 北京:人民卫生出版社, 2008.9.
[2] 张云虎主编. 尿液沉渣实录彩色图谱. 济南:山东科学技术出版社, 2003.1.




