糖化血红蛋白标准化 和检测准确度现状
1968年,伊朗生化学者Ranbar S从糖尿病患者的红细胞中发现了不正常的血红蛋白[1,2]。2012年美国糖尿病协会专门为他颁发了杰出发现奖[3]。可惜,就在这一年,Dr. Ranbar S去世了。如果当年不是Ranbar在糖尿病患者中发现了糖化血红蛋白,今天的糖尿病研究也不知道是什么样子。
一、明确糖化血红蛋白在糖尿病治疗和
并发其它疾病中具有监视的价值[4]
1、DCCT临床试验 糖尿病及其并发症的不利影响,在上世纪80年代受到美国卫生部的重视。1983年,由美国卫生部,美国卫生研究院和美国糖尿病、消化病、肾病研究院参与,开展了9年的1型糖尿病控制与并发症研究(Diabetes Control and Complications Trial,DCCT)。为了使研究得到确实结果,决定使用糖化血红蛋白检测作为观察疾病控制或并发症的重要指标。针对当时市场上检测糖化血红蛋白试剂混乱情况,研究专家要求所有在美国各地开展这项研究中涉及的1型糖尿病患者的血液标本,全部送往两个实验室检测;并且指定:密苏里大学实验室为唯一指定的比较实验室,采用伯乐公司的阳离子选择高效液相层析方法的仪器;明尼苏达大学实验室也使用伯乐公司相同型号的仪器,但是必须按照密苏里大学的真实样品结果予以校准。这是在当时既无参考物质、又无参考方法的情况下,以人为指定的方式使检测结果具有可比性的有效手段。
今天以百分值报告的糖化血红蛋白结果,确定糖化血红蛋白结果的参考上限为6.0%;高达7%的患者必须接受治疗的,就是DCCT的研究成果[4]。怎样将DCCT的成果用于临床为糖尿病患者服务,必须要求美国各实验室的糖化血红蛋白结果和DCCT值具有可比性。如果仅确定任何方法的糖化血红蛋白值是否在实验室的“正常范围”,没有意义。需要更精确地了解:这个检测值和DCCT值的关系是什么?因为只有DCCT的结果直接和平均血糖与后果危险有关。
2、英国UKPDS[5] 1998年英国前瞻性糖尿病研究(UK Prospective Diabetes Study,UKPDS)发表了临床试验结果。对2型糖尿病病人进行了10年研究,重复了DCCT的发现,即并发症的减少和糖化血红蛋白的降低有关。UKPDS使用了NGSP认可的糖化血红蛋白测定方法,另外,参与NGSP参考网络仔细的比较过程来确保DCCT和UKPDS 检测结果间的可比性。所以,DCCT和UKPDS二者的GHB结果都可以用于1型或2型糖尿病的病人,评估未来发展为糖尿病并发症的个人危险程度。
二、什么是糖化血红蛋白
(什么是HbA1c的被测量)?
糖化蛋白是食品行业评价烘烤的面包点心的一个重要指标。刚刚出炉的面包上闻到的香味、以及在面包上看到的略带焦黄的颜色,它们都是面包里的糖分与蛋白在烘烤过程中促使蛋白被糖化后的表现。人体一日三餐从食物中摄入淀粉和糖分,在肠胃道内被淀粉酶迅速分解为单个葡萄糖。由肠胃道的血管内的血液吸收循环进入肝脏。在那里又被形成人体的肝糖储存于体内。因此,饮食后的血液里葡萄糖含量会升高。好在人体内的内分泌激素,尤其是胰岛素,在血液葡萄糖含量升高时大量分泌,促使葡萄糖快速从血液中进入肝脏。如果我们不注意有规律地饮食,吃得过多,增加了人体摄入葡萄糖的负担,使大量葡萄糖淤积在血液,血液葡萄糖含量明显升高。长此下去逐渐成为糖尿病,因为堆积在血液内的葡萄糖为了减轻血液内的负担,只能通过肾脏排出体外。
由于血液内葡萄糖含量的升高,使血液内的所有蛋白和代谢物都被高浓度葡萄糖包围。葡萄糖与蛋白的紧密相处,促使葡萄糖吸附在
蛋白上,在蛋白结构的游离氨基处,从吸附葡萄糖到缓慢的分子重新排列,形成了稳定的糖化蛋白。因此,血液中的所有蛋白,凡是具有游离氨基的,都会被糖化。只是血液中的许多蛋白的存在时间或半衰期较短,所以被糖化的量不是很大。其中白蛋白的半衰期为1个月左右,所以检测糖化白蛋白可以大致上反映患者在近一个月内血糖控制的情况。
红细胞是血液中被浸润在甜蜜的血浆中,生存时间最长的一个有形成分,它的半衰期可达3个月。葡萄糖不仅“糖化”了红细胞膜,而且还钻入红细胞膜进入细胞浆内,这样使血红蛋白也处在满是葡萄糖的包围中,同样,在血红蛋白的珠蛋白上,每个珠蛋白长链上有多个游离氨基,它们都会不约而同地与葡萄糖长期相处,逐渐成为“糖化血红蛋白”。因此,检测血液红细胞内血红蛋白的糖化比例可以反映患者在约三个月内血糖控制状态。
上世纪70年代,了解了血红蛋白糖化后,第一个被临床实验室检测的方法是“果糖胺”。这是因为葡萄糖被蛋白游离氨基吸附、并经分子重排后,形成了血红蛋白分子上酮胺结构1-脱氧果糖基。该基团具有氧化还原性质,形成了果糖胺的检测项目。但因没有标准物质,所以难以在不同方法间具有可比性。
早于1955年,研究者注意到成年人血红蛋白为非均相。1958年,Allen报告,在离子交换层析上的人血红蛋白可以被分离出三个小的组分,它们较HbA的负电荷更强。这三个血红蛋白被命名为HbA1a、HbA1b、HbA1c。但是,并没有被认识到与糖尿病的关系。直至Rahbar使用琼脂电泳,报告糖尿病患者的这些小血红蛋白组升高,才被认识到它们与糖尿病的关联。1970年代中期,弄清楚了是葡萄糖对血红蛋白HbA的非遗传修饰,产生了HbA1c;HbA1c与空腹葡萄糖、糖耐量试验时的葡萄糖峰值、葡萄糖耐量试验的曲线下的面积、以及在以往数个星期的平均葡萄糖水平等均有关系。1980年早期,以笼统的糖化血红蛋白检测GHB被广泛应用。可惜当时结果可比性很差。现在已经清楚:天然(非糖化)血红蛋白是Ao(2α、2β链)[HbAo]。血红蛋白β-链N-末端缬氨酸的游离氨基、其他游离氨基;以及包括α-链N-末端缬氨酸、赖氨酸ε-氨基等,均可与不同碳水化合物糖基化形成各种糖化亚组分(HbA1a1、HbA1a2、HbA1b和HbA1C)。所有这些亚组分被称为总糖化血红蛋白[HbA1]。少量的胎儿血红蛋白HbF(2α,2γ链)和血红蛋白A2(2α、2δ链)上,在γ链或δ-链N-末端的缬氨酸以类似的方式糖基化,形成HbA2c等。因此,今天在叙述的糖化血红蛋白其实指的是HbA1c。
由于每个患者的血红蛋白浓度不同,表示糖化血红蛋白的量以相当于总的血红蛋白量的百分数更为合理。
即 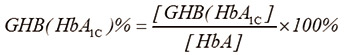
三、NGSP糖化血红蛋白标准化
1、1993年,在DCCT结果公布前,美国临床化学学会(AACC)成立了糖化血红蛋白标准化委员会。委员会的任务是:实现美国实验室糖化血红蛋白可比性,也肯定了实现糖化血红蛋白检测国际可比性的重要性。为此,委员会成员包括了欧洲成员,他们在糖化血红蛋白的可比性和室间评估上有丰富的经验。
AACC委员会围绕DCCT参考实验室发展了可比性方案,该方案在1995年被美国厂商的协调委员会认可。1996年AACC委员会解散,被美国国家糖化血红蛋白标准化计划(National Glycohemoglobin Standardization Program,NGSP)替代,在1996年7月开始工作。1997年美国糖尿病协会(ADA)认可NGSP(注:NGSP是美国政府疾病控制中心负责下的一个行政管理机构。因此,从1996年开始,控制糖尿病成为了美国政府行为)。
2、NGSP标准化做法[6,7]
NGSP实现标准化过程有三个主要步骤:均以新鲜全血进行以下的证实:第一步是对厂商的测定方法进行校准,使厂商实验室糖化血红蛋白结果和NGSP的网络实验室结果具有可比性;第二步是由厂商确认他们的产品,也和NGSP的网络实验室结果具有可比性;第三步是各临床实验室参加室间评估,对具有NGSP实验室网络定值的新鲜全血样品检测,验证他们日常报告的结果可比性。严格讲,全世界的临床实验室只有得到NGSP的认可,方才有资格报告以百分值表示的糖化血红蛋白结果。
ADA建议:实验室只使用被NGSP确认的GHb的检测方法,能提供和DCCT结果具有可比性、可以使用由DCCT建立的参考范围;实验室自身也必须被NGSP确认,它有资格报告符合NGSP要求的结果(%)。在使用被NGSP确认的产品时,实验室接受NGSP新鲜全血样品的考核应符合要求检测性能要求。即方法应具有良好的重现性;它的总不精密度须小于指定水平。
3、NGSP和CAP的协调[7]
NGSP与美国病理学会(CAP)一起协调,通过NGSP为CAP GH2全血能力比对试验样品设定NGSP靶值,采纳和最终收紧以准确度为基础的分级。CAP提供了全球最大的HbA1C能力比对试验调查。1996年CAP开始使用混合新鲜全血标本进行GH2调查。因为样品没有了以往调查HbA1c的基质效应的困扰,结果可以可靠地用于检查方法内和方法间的偏倚和不精密度。近期(2010)登记超过了3000个实验室,许多来自国外。
方法性能上的改善:在2000年到2010年间,低范围的样品(4%~6% HbA1c),所有方法的CV从约7%下降到4%。在6%~10% HbA1c范围的样品,所有方法CV从约5%~5.5%下降为约4%。许多方法现在具有的实验室间CV≤3%,少数的为2%。
医生在使用HbA1C检测去评估病人的血糖状态时经常考虑:患者的血糖控制是否稳定了、改善了、还是不好;另一个问题是:如何将HbA1C结果与个人的目标HbA1C进行比较(近期ADA建议7%为目标,若可行则更低一些更好)。许多医师已经建议,0.5% HbA1c是一个“临床上显著变化”的指标。
CAP的HbA1C的分析目标:CAP在2010年的要求是±8%限值,相当于靶值为7% HbA1c、限值为±0.56% HbA1c;超出了±0.50%的临床要求。2011年±7%限值,使HbA1c水平在7%的结果误差水平相当于±0.49% HbA1c,符合了临床要求。在几乎所有近期CAP调查中,多于90%实验室参加者可通过±7%判断限。当高于7% HbA1c,CAP判断限将必须收紧到0.5% HbA1c。
四、IFCC的HbA1c标准化
1、NGSP标准化出现了问题[8]
糖化血红蛋白(GHb≠真正HbA1c)被美国DCCT研究与在NGSP计划中指定作为比较方法的Bio-Rad 70 HPLC方法,与瑞典推荐Mono S HPLC方法为标准化方法之间,在判断限水平处的差异达20%。日本发表的临床试验也说明,尽管也采用了HPLC技术检测HbA1c,但是HbA1c的值低于美国NGSP的值。DCCT的参考方法检测的值,并不是真正的唯一HbA1c值。DCCT/NGSP的标准化只能依据密苏里大学实验室的HPLC仪器分离结果为唯一标准化的依据。即没有任何HbA1c参考物质或确认该物质的参考方法。
2、IFCC的糖化血红蛋白标准化[9]
1995年IFCC组成了HbA1c标准化工作组(IFCC-WG)以实现检测的统一国际标准,发展和确认了2个侯选参考方法和HbA1c、HbAo(非糖化血红蛋白)参考物,作为全球可比性分析准确度的基础。
(1)首先IFCC确定了HbA1c被测量[9]。IFCC命名、属性和单位委员会(C-NPU)批准了以往被称为‘HbA1c’的参考检测程序(方法)。该程序测量的是单一分子属性;允许计算检测结果为“物质组分的量(mol)”;而不是质量(重量)组分(kg)。在计量上可溯源至国际单位制(SI)。该委员会认识到:在所有β-链的血红蛋白的中,β-链N-纈氨酰-1-果糖基血红蛋白 (valyl-1-fructosylated haemoglobin β-chains),可被IFCC参考测量程序特异地测量,所以在计量上可溯源至具有“毫摩尔每摩尔(mmol/mol)”计量单位某物质组分。因此,现在IFCC标准化检测被测量非常明确。检测的非糖化血红蛋白为β-链的血红蛋白(HbA0);检测的糖化部分为β-链N-纈氨酰-1-果糖基血红蛋白(HbA1c),即[β-(N-脱氧果糖基) 血红蛋白]。
以往(即不规范)的用语和测量(检测)单位:原IFCC-IUPAC的NPU数据库有‘HbA1c’的专用的属性类的词语,该被测量的代码为NPU03835:命名的是血红蛋白(Fe;全血)和血红蛋白A1c(Fe);为物质的组分;其计量单位被假设为“1”。
(2)IFCC的HbA1c参考测量系统
a)2007年欧洲参考物质和参考测量研究院(IRMM),发布了IRMM/IFCC-466号批准的参考物质[10],是人全血分离的血红蛋白,内含非糖化的HbA0和糖化的HbA1c。该物质给出了HbA1c/(HbA0+HbA1c)值(mmol/mol)。
b)2002年发表了批准的检测人全血中HbA1c的IFCC参考方法[11,12]。有两个参考方法:HPLC/电雾离子化质谱方法(HPLC-ESI/MS)与HPLC/毛细管等电聚焦电泳方法(HPLC-CE)。二者原理与工作均很好,并得到一样的结果。这两个方法[13]依据对血红蛋白β链的N-端的特定检测。以胞内蛋白酶Glu-C水解完整的血红蛋白分子,得到HbA1C和HbA0的β-N-端的六肽多肽。这些多肽以反相HPLC分离,并由电喷射离子化-质谱(方法A)或由毛细管电泳(方法B)进行定量。以这些多肽和联用分离技术,有可能克服以往使用的HbA1C蛋白分离系统的不足分辨率。
c)已经实施了参考检测实验室的网络。每年进行两个实验,对分发的物质进行检测比较,也为候选的校准品和控制品定值。自1999年起实施了这些研究,在新技术的信息可用下,定期更新重新确定参考检测程序非常重要[14]。
d)在IFCC参考检测实验室和DCM(现有的指定比较方法,如美国的NGSP)间实施了多次比较研究。这些研究发现,IFCC和不同的DCM系统间和发表的相应回归等式(“一级等式”)的关系是稳定的[15]。
e)以新鲜和冰冻全血组形式已经产生了二级参考物质。这些物质分发给厂商和实施DCM的实验室,使它们的方法校正至IFCC参考系统。
五、实现国际HbA1c标准化
1、2004年ADA、EASD、IDF联合认为实现全球报告HbA1c结果具有可比性无异议。美国糖尿病协会(ADA)、欧洲糖尿病研究学会(European Association for the Study of Diabetes,EASD)、和国际糖尿病学会(International Diabetes Federation,IDF),成立了HbA1c工作组目的是使全球HbA1c报告一致。联合会议认为,对全球报告HbA1c结果具有可比性无异议。可以立即实施的有:1)接受IFCC方法参考方法,作为厂商校准HbA1c检测的新的全球标准。2)使用新的IFCC方法学在现有的国际实验室网络内确定为“国际证实过程”。3)厂商不需改变现有的报告方式,直至完成以后的工作(即证实IFCC值在临床上的应用价值);目前继续使用DCCT/UKPDS值。4)美国要求IFCC对2型糖尿病病人进行类似DCCT的临床试验,确认IFCC在临床上的使用价值。
2、2007年国际实现HbA1c标准化声明。2007年5月4日在意大利米兰召集了讨论协同一致的审核。美国糖尿病联合会(ADA)、欧洲糖尿病研究联合会(EASD)、国际糖尿病联合会(IDF)和IFCC在会议后发表了联合声明[16]:
(1)A1C检测结果应全球标准化,包括参考系统和结果报告。(2)新IFCC参考系统代表了唯一的有效基础,去实施检测标准化。(3)全球报告的A1C结果为IFCC单位(mmol/mol),和使用IFCC-NGSP的一级等式导出的NGSP单位(%),NGSP(%)= [0.0915×IFCC]+2.15。(4)如果继续进行的“平均血浆葡萄糖研究”满足它的先前-特定的指标,由A1c导出的平均葡萄糖值(ADAG),可由A1c结果计算而来,将也可作为解释A1c结果的报告。(5)在临床导则中出现的糖血目标应表达为IFCC单位、导出的NGSP单位、和ADAG。
所有组织同意这个系统声明的提议,尽快在全球实施这些建议。相信这个协议书将进一步为全球A1c结果的可比性、为A1c检测的分析和生物化学特性有关的进展作出贡献。以科学正确的单位表达检测结果,并以临床上对结果的有关解释,并不是不常见的做法(如肌酐和估计的肾小球率过滤)。最后,临床医生将有机会,对在治疗中的病人给予最合适的词语和单位上表达慢性糖血症的概念。
HbA1c的国际标准化是一个重大的决定。它第一次对什么是HbA1c做出了明确的定义,为全球HbA1c的可比性建立了牢固的基础。但是,任何事物总有不足,HbA1c的标准化在进入常规使用中,出现了声明可溯源至IFCC参考系统的免疫检测方法与酶法,和美国NGSP以HPLC方法间的不协调。
六、检测HbA1c准确度的现状
1968年自从发现了HbA1c在糖尿患者群中的升高,很少会已经预示到40余年以后,检测HbA1c会成为糖尿病常规管理和诊断的一个不可缺少的部分。自从里程碑的临床试验(如,DCCT、UKPDS)以来,标准化HbA1c检测已经获得了相当的进展,明确了血糖控制(由HbA1c检测)和并发症的关系[17]。
由于HbA1c检测方法的发展,各个厂商在宣传产品的特点和检测准确度上,很多针对Hb变异体上对检测结果的影响。尤其在我国,厂商竞争做法不太文明的情况下,使我们临床实验室很模糊。其实,任何一个检测方法都有它的特点和优点,当然也一定有它的不足之处。
1、什么是血红蛋白病?
血红蛋白病(hemoglobinopathy)是由于血红蛋白分子结构异常(异常血红蛋白病),或珠蛋白肽链合成速率异常(珠蛋白生成障碍性贫血,又称海洋性贫血)所引起的一组遗传性血液病。
(1)血红蛋白是一种结合蛋白,分子量64000,由珠蛋白和血红素构成。血红素由原卟啉与亚铁原子组成,每一个珠蛋白分子有二对肽链,一对是α链,由141个氨基酸残基构成,在运氧中具重要生理作用。另一对是非α链,有β、γ、δ、ξ(结构与α链相似)及ε5种;每一条肽链和一个血红素连接,构成一个血红蛋白单体。人类血红蛋白是由二对(4条)血红蛋白单体聚合而成的四聚体。不同类型的血红蛋白珠蛋白结构略有不同,但血红素均相同。
(2)正常人出生后有三种血红蛋白:1)血红蛋白A(HbA),由一对α链和一对β链组成(α2β2),为正常人主要血红蛋白,占血红蛋白总量的95%以上。胚胎二个月时HbA即有少量出现,初生时占10%~40%,出生6个月后即达成人水平;2)血红蛋白A2(HbA2),由一对α链和一对δ链组成(α2δ2)。自出生6~12个月起,占血红蛋白的2~3%;3)胎儿血红蛋白(HbF)由一对α链和一对γ链组成(α2γ2),初生时占体内血红蛋白的70%~90%,以后渐减。至生后6月,含量降至血红蛋白总量的1%左右。
(3)血红蛋白的不同肽链是由不同的遗传基因控制的。珠蛋白基因突变而致肽链的单个或多个氨基酸替代或缺如,导致珠蛋白分子结构改变,称为异常血红蛋白(或血红蛋白变异体)。全世界范围内经结构分析证实的异常血红蛋白日益增多,至90年代初期已达600多种,但仅不到1/3的异常血红蛋白伴有临床症状。世界卫生组织估计,全球约有1.5亿人携带血红蛋白病基因,并已将血红蛋白病列为严重危害人类健康的6种常见病之一。异常血红蛋白病在我国以云南、贵州、广西、新疆等地发病率较高,现已发现异常血红蛋白67种,包括α链(34种)、β链(26种)、γ链(4种)等异常,其中19种为我国首见。海洋性贫血多发于华南及西南地区。根据近10年来我国28个省市、自治区近100万人口的普查资料,异常血红蛋白病的发病率为0.33%,α海洋性贫血的发病率为2.64%,β海洋性贫血的发病率为0.66%。
血红蛋白中大多为血红蛋白A(占约98%),因此检测的糖化血红蛋白自然也以HbA中,其他血红蛋白中没有的β链被糖化的部分来表示糖化血红蛋白(%)。血红蛋白病产生的各种血红蛋白变异体,如果是糖尿病患者,这些血红蛋白变异体也会被糖化,或它们的蛋白结构等也会影响糖化血红蛋白检测结果的可靠性。
2、NGSP标准化和IFCC标准化
正如前述,美国糖尿病协会为了得到糖尿病控制是否可以减少糖尿病并发症的结果,针对当时缺乏HbA1c的参考物质和参考方法情况下,采取了武断的标准化措施,得到了全世界第一个结论,即对糖尿病的控制可以减少或减缓糖尿病并发症的发生。美国为了将研究成果在美国和全世界应用,实施了NGSP计划。由于它的实施,全球今天的HbA1c检测结果以百分值(%)表示的,无不展示了美国NGSP的重大影响。但是,只采用了HPLC的层析技术,以此确定为HbA1c的NGSP结果,被证实分离的HbA1c不是单一蛋白。IFCC的完整的标准化,既有参考物质,又有参考方法。确实在标准化上非常完整。因此,以美国NGSP为主的HPLC层析系统的检测方法,美国糖尿病协会(ADA)承认IFCC为全球的唯一参考系列,并且承认美国的NGSP结果应上溯至IFCC的参考物质和参考方法。这在以往的任何领域从未有过。但NGSP全世界报告HbA1c的影响很大,而且伯乐(Bio-Rad)等专注HPLC离子交换技术的公司,多年来也在HPLC技术上有了很大的改进。
IFCC标准化尽管晚了几年,但是,IFCC对HbA1c的贡献,是前人在这个领域所没有过的。为了使IFCC的成果尽快在临床上的应用,多年来已经形成了免疫技术和酶法技术,用于临床实验室或内分泌实验室对糖尿病患者的HbA1c的检测,可以直接报告IFCC结果。由于IFCC参考方法和参考物质的研究与发展成果检测方法几乎是同一个厂商,所以,在推广免疫方法的产品宣传上,强调免疫方法的结果可直接溯源至IFCC系统,而且可以不受任何血红蛋白变异体的影响;指出HPLC的检测方法无法避免血红蛋白变异体的干扰影响。
在国内市场上,直接报告NGSP和IFCC结果对应的公司竞争非常剧烈。尽管国际上承认二者结果都有效。但是,这已经影响了临床实验室在认识上的模糊。尤其是针对检测方法是否可以特异地消除血红蛋白变异体干扰,是今天竞争的重点。
3、HbA1c各个常规检测方法的分析
(1)以往HbA1c差异的原因之一 在IFCC对HbA1c的被测量定义前,任何血红蛋白被糖化的形式,都是“糖化血红蛋白”的一个组分。确实在定量上非常混乱。仅以正常的血红蛋白为例,由于在血红蛋白上有多个具有游离氨基,它们均可以被葡萄糖糖化形成糖化血红蛋白,而且在糖化中,这些游离氨基被糖化的可能性是随机化的。可以在β-N-Val-1(即血红蛋白β链N-端的第一个氨基酸缬氨酸)、在β链的第17、20、和66个赖氨酸(β-Lys-17、β-Lys-20、β-Lys-66)的ε氨基,和在α链-N端的第一个氨基酸(缬氨酸)(1α-N-Val-1)、在α链的第7、16个赖氨酸的ε氨基,被葡萄糖糖化形成糖化血红蛋白。在上述的7个位点可以被葡萄糖糖化处,被糖化的任意点、各个糖化点的任意组合等,都是使各个方法在检测中具有差异的原因。当出现了血红蛋白的变异体时,还有其他变异体可糖化的位点出现了。
(2)IFCC的HbA1c定义 为了使糖化血红蛋白检测标准化,IFCC定义了:为血红蛋白的β链N端的缬氨酸(Val)被糖化的相应血红蛋白,被称为糖化血红蛋白(HbA1c)。在β链上的其他位点即使被糖化的、以及α链上被糖化的位点,均不予认可为糖化血红蛋白。因此,从定义上第一次明确的标准化,完全是充分考虑到“糖化血红蛋白”在分子结构上的复杂性,只有硬性规定了某个分子结构被命名为“HbA1c”,才能是HbA1c的检测结果在全球具有可比性。
但是,没有被IFCC定义确定的糖化血红蛋白,它们是真实存在的。在检测量值上实现了全球可比性,却为临床遗漏了已经发病的糖尿病患者血液中,其他分子结构的糖化血红蛋白!在糖尿病患者诊疗和监视中,免疫检测HbA1c出现了明显的临床问题[18]。
(3)HbA1c常规免疫检测方法和酶法 由于常规检测方法的限制,IFCC参考方法对未糖化的血红蛋白定义为N-端缬氨酸未被糖化的β链血红蛋白。但是在常规中使用一般方法难以分离出这个未被糖化的β链血红蛋白。还是沿用了传统的临床实验室检测血红蛋白方法,以比色检测样品的“红色”程度表示血红蛋白总量。可惜,这个方法检测出的血红蛋白是样品中含有高价铁离子的所有血红蛋白,包括了正常的α、β、γ、δ、ξ及ε链之外,还有各种异常的血红蛋白病中的各种链。这与IFCC对HbA1c定义中的非糖化部分的血红蛋白,仅仅是β链血红蛋白要求完全不同。所以,使最后报告HbA1c结果的分母部分放大。如果免疫方法使用的抗体完全符合IFCC的HbA1c定义,则最后得到的结果要偏低了。这是在形成HbA1c免疫检测方法开始时,认为检测方法受干扰了[19]。作者介绍使用识别HbA的β-链N-端糖化氨基酸的结构免疫检测量化HbA1c。他说:“使用了第一代检测试剂,内含抗体针对抗原决定簇主要分布在Hb的β-链的第4到第10个氨基酸,包含了在HbS和HbC变异体第6个改变的氨基酸位置。但是在这些Hb变异体存在下,HbA1c检测受到干扰。促使发展了第二代检测,使用的抗体包含了第1到第4个氨基酸。结果第二代检测的抗体极大地消除了来自HbS和HbC的分析干扰,在与第一代检测比较中改善了整个准确度。第二代检测抗体通过结合类似于HbA的HbS和HbC变异体,这样为具有杂合子情况的患者提供了临床上有用的HbA1c值,他们的RBC寿命想来基本上是正常的”。这篇文章的解释让人迷惑。明明使用了与IFCC方法中检测β-链N-端的六肽对应的抗体,检测的是从第4个到第10个氨基酸的多肽链,应该与IFCC参考方法一致,怎么会出现“干扰”了?学习后,我理解了,IFCC参考方法只检测β-链N-端起的六肽,原因是充分考虑到,Hb变异体在蛋白结构上的突变多发生于HbA的β链N-端起,计算的第六个氨基酸位置。
正常的HbA链的N端六个氨基酸序列为Val-His-Leu-Thr-Pro-Glu-Glu-;
血红蛋白变异体S(HbS)的N端六个氨基酸序列为:Val-His-Leu-Thr-Pro-Val-Glu-;
血红蛋白变异体C(HbC)的N端六个氨基酸序列为:Val-His-Leu-Thr-Pro-Lys-Glu-。
互相比较,可以发现,HbA、HbS和HbC的第六个氨基酸不同。因此,IFCC专家非常注重此点,只切下六个氨基酸多肽进行分析,消除了HbS和HbC对检测干扰。
现在,经典的免疫方法抗体也遵循了这个特点,避免了HbS和HbC干扰。应该是非常好的。可是,计算糖化血红蛋白的分母部分,因为检测了所有类型的血红蛋白,违反了IFCC对HbA1c的定义,数字放大了。造成最后计算的糖化血红蛋白量的缩小!这个结果被说成是受“干扰”了!
第二代免疫试剂使用的抗体,只针对从N-端的第一个到第四个氨基酸的四肽。这样,被检测的血红蛋白回避了第六个氨基酸是否为谷氨酸的特异性要求。结果任何血红蛋白,只要具有类似HbA的N-端四个氨基酸的各种血红蛋白,全部被检测出来!放大了血红蛋白计算中的分子部分。巧合的是,分母因检测了所有各种非糖化血红蛋白而放大,分子也因检测了各种类似的糖化血红蛋白而放大!二者的放大后数字相除,得到了与IFCC参考方法检测结果非常相似数量!
这样的巧合,可以从某公司资料上非常明确,它们计算的HbA1c结果如下:
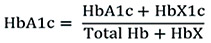
4、让今天HbA1c检测现状回到临床实验室的现实世界
(1)回顾糖化血红蛋白检测的历史 从Dr. Ranbar发现糖尿病患者有异常的糖化血红蛋白起,他是从电泳图谱上发现的。以后,DCCT的实验室在层析分离的图谱上,观察到HbA1c峰,并相对于未糖化的血红蛋白峰(加上HbA1c峰)计算出HbA1c的百分值。IFCC的HbA1c工作组形成的参考方法,还是采用了HPLC技术分离HbA1c和HbA0六肽,然后再定量的!也是看到了分离图谱。因此,今天的临床实验室为糖尿病患者进行HbA1c检测时,如果仅仅使用免疫检测方法或酶法,可以在自动化仪器上检测速度快、成本低。但是只有一个检测值,无法了解这个值的背后究竟有无血红蛋白变异体。有人借用Dr. Sacks的文章[20],宣传说,看看这些HPLC的分离图谱,你就可以知道HPLC分离方法的落后!HPLC方法根本无法分离所有血红蛋白变异体对HbA1c的影响,因为很多变异体的分离峰掩盖了HbA1c的峰。其实,我们的实验室同道没有认真阅读这篇论文!如果好好阅读了,你才会有真正的体会。
Dr.Sacks是世界闻名的糖尿病大家,是他们完成了DCCT的著名临床试验,得出了控制血液糖化血红蛋白与糖尿病并发症的强烈关系。他们正是使用离子交换HPLC方法,采取强制标准化措施,得到这样伟大的结论。至今在NGSP的参考实验室内,依然在使用离子交换HPLC方法检测HbA1c,作为NGSP的参考方法。尽管将离子交换HPLC方法列为NGSP的参考方法,但是这些顶级专家早在21世纪初,就已经以综述形式告诫所有实验室,必须谨慎使用离子交换HPLC!今天,面对免疫检测方法的强大优势,他们很快接受了罗氏的Tina-Quant产品为不会被血红蛋白变异体影响的方法。在很多文章中(尤其在近两年),为了解Hb变异体对各种检测方法的影响,将Tina-Quant和硼酸亲和方法(ultra)列为比较方法,充分说明ADA的明确观点。
今天很多实验室依然采用离子交换HPLC的方法作为检测HbA1c方法的首选。为什么?因为它为每个患者样品的检测提供了一张便于判断和使用的层析图。今天的免疫检测方法尽管在多个评价中,被认为很少受到变异体的影响干扰。但是仅仅一个数据,你能让实验室看到什么?它无法让实验室知道,检测的样品有无Hb的变异体。
(2)上海中山医院临床实验室的做法非常值得大家学习。无论是对一致性计划的调查样品定值、还是在日常对患者样品检测HbA1c,他们都首先使用了离子交换HPLC的方法。理由很简单,可以看层析图,做出判断。当一旦层析图显示难以区分时,他们采用免疫方法检测样品,同时以相同样品的糖化白蛋白和近期患者的血糖表现,综合对患者血糖状况和HbA1c结果做出判断。
罗氏Cobas的HbA1c产品说明书写得非常好。它说:作为原则,必须小心注意具有Hb变异体患者的任何HbA1c结果的解释。不正常血红蛋白会影响红细胞的寿命或体内糖化率。在这些情况下,即使分析上正确的结果不反映在正常血红蛋白患者预期的相同血糖控制。在疑似存在某个Hb变异体(如,HbSS、HbCC、或HbSC)影响了HbA1c值和血糖控制间关系时,必须不可使用HbA1c进行糖尿病的诊断。
因此,尽管都认为免疫方法很少受到Hb变异体的干扰。但是,ADA的导则明确指出:只要具有Hb变异体的患者样品结果,不可任意报告结果为临床做出糖尿病的诊断。仅仅一个结果如何看得出有问题?
上海中山医院的做法值得推广。只有先使用离子交换HPLC,发现问题再以免疫方法去比较。这个做法完全符合ADA导则的精神。
随着经济发展、人员在国内充分流动的情况下,原先在我国南方地区的人群在上海也越来越多。生活条件好了,到处都出现越来越多的新糖尿病患者。因此,千万不可马虎,随时警惕Hb变异体对HbA1c结果的影响。越是到南方,问题更严重。
无论你的实验室采用什么方法检测HbA1c,都应该认真学习Hb变异体对HbA1c检测结果的影响。尤其是在选择HbA1c检测产品时,一定要详细了解具体的资料,阅读厂商提供的说明书。使用免疫方法或酶法检测HbA1c的实验室,最好能另外具有诸如离子交换HPLC的产品。它将在确定有无Hb变异体时发挥作用。对于正在使用离子交换HPLC的实验室,你应有诸如免疫方法或酶法的产品备用。一旦在层析图上出现确定为Hb变异体时,使用其他方法比较,并应及时与临床联系。检查患者的糖化白蛋白、近期使用血糖仪自我监视的资料和临床表现等,防止发出错误报告。
针对我国情况,还有很多经济欠好的地区。特别要注意因营养不良、近期有出血事例、近期有输血的过程等。因为这些均会影响红细胞的寿命。对于这样的患者不应使用HbA1c作为糖尿病诊断或监视的指标。应该采取糖化白蛋白、果糖胺、以及直接葡萄糖检测等项目替代,方能避免错误诊断和延误治疗[17]。
七、总结
1、HbA1c是诊断和监视糖尿病治疗效果的重要指标。感谢IFCC的努力,使全球HbA1c的检测正逐渐趋向一致。
2、但是,所有可以检测HbA1c产品的厂商,都不会客观描述自己的弱点,只强调他们产品的价值,说些让你感觉舒服的介绍。当心上当。
3、为了患者的利益,每个实验室必须完善检测需要的质量管理。必须对使用产品在对患者检测、发出报告前,亲自动手去验证产品的分析性能。只有确认产品的分析性能确实如介绍那样可以信任下,方可使用!可惜,今天的我国临床实验室都做得很差!期望重视!
4、一个实验室必须具备两个检测方法的产品,让你方便地识别患者样品内有无Hb变异体的出现。至今,尽管说免疫方法没有变异体干扰,但是国际上尚未对各个Hb变异体对检测结果的影响,从临床上做出客观的决定。所以,为了患者的利益,我们实验室一定要充分了解更多的信息。需要认真学习!
参考文献:
[1] Ranbar S. An abnormal hemoglobin in red cells of diabetics.Clin Chim Acta, 1968, 22:296-298.
[2] Ranbar S, Blumenfeld O, Ranney H. Studies of unusual hemoglobin in patients mellitus. Biochemical and Biophysical Communication. 1969,36(5):838-843.
[3] Gebal E. The start of something good: the discovery of HbA1c and American Diabetes
[4] The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on delelopment and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med. 1993; 329(14): 977-86.
[5] Stratton IM, Adler AI, Neil HAW, Matthews DR, Manley SE, Cull CA, Hadden D, Turner RC, Holman RR on behalf of the UK prospective diabetes study group.Association of glycaemia with macrovascular and microvascular complications of type 2 diabetes (UKPDS 35): prospective observational study. BMJ 2000; 321: 405-412.
[6] Little R, Wiedmeyer HM, et al. Interlaboratory standization of measurements of glycohemoglobin. Clin Chem, 1992; 38(12):2472-2478.
[7] Little R, Rohlfing CL, Sacks DB. Status of hemoglobin A1C measurement and goals for improvement: from chaos to order for improving diabetes care. Clin Chem, 2011(2):205-214.
[8] Turpeinen U, Karjalainen U, Stenman U. Three assays for glycohemoglobin compared. Clin Chem 1995; 41(2):191-195.
[9] Nordin G,Dybkear R. Recommendation for term and measurement unit for “HbA1c”. Clin Chem Lab Med 2007; 45(8):1081-1082.
[10] EUROPEAN COMMISSION JOINT RESEARCH CENTER. Certified Reference material IRMM/IFCC-466.
[11] Approved IFCC Reference Method for the Measurement of HbA1c in Human Blood. IFCC Scientific Division, Working Group on Standardization and Network of Reference Laboratories of HbA1c. Clin Chem Lab Med 2002;40(1):78-89.
[12] Mosca A, Goodall I, Hoshino T, Jeppsson JO, John WG, Little RR,Miedema K,Myers GL, Reinauer H, Sacks DB, Weykamp CW. IFCC Scientific Division, Working Group on Standardization of HbA1c. Clin Chem Lab Med 2007; 45(8):1077-1080.
[13] Kobold U, Jeppsson JO, Dulffer Th, Finka A, Hoelzel W, Miedema K. Candiate reference method for HbA1C based peptide mapping. Clin Chem 1997;43:1944-51.
[14] http://www.ifcchba1c.net/. Acessed June 21,2007.
[15] Hoelzel W, Weykamp C, Jeppsson JO, Miedema K, Barr JR, Gooddall I, et al. IFCC reference system for measurement of hemoglobin A1c in human blood and the national standardization schemes in the United States, Japan, and Sweden:a method-comparison study. Clin Chem 2004; 50:166-74.
[16] The American Diabetes Association, European Association for the Study of Diabetes, International Federation of Clinical Chemistry and Laboratory Medicine, and the International Diabetes Federation. Consensus Statement on the Worldwide Standardization of the Hemoglobin A1C Measurement. Diabetes Care 2007;30(9):2399.
[17] Little RR, Rohlfing CL. The long and winding road to optimal HbA1c measurement. Clin Chim Acta 2013; 418:63-71.
[18] Sacks DB. Hemoglobin variants and hemoglobin A1c analysis: problems solved? Clin Chem 2003; 49: 1245.
[19] Rhea JM, Koch D, et al. Unintended reporting of misleading HbA1c values when using assays incapable of detecting hemoglobin variants. Arch Pathol Lab Med 2013; 137: 1788.
[20] Bry L, Chen PC, Sacks DB. Effects on hemoglobin variants and chemically modified derivatives on assays for glycohemoglobin. Clin Chem 2001; 47: 153-163.




