西格玛性能验证图在肿瘤标志物检测项目性能评价 及质控方法选择中的应用
随着肿瘤的发生率和患者的死亡率逐年递增,肿瘤标志物在肿瘤的辅助诊断、鉴别诊断、疗效观察、监测复发转移以及预后的评价中的价值越来越受到临床医生的重视[1]。我国各级医疗单位临床实验室广泛开展了肿瘤标志物的检测,在不同实验室或不同检测系统检测同一份样本,通常具有较大的差异。因此我们需要对肿瘤标志物检测进行质量控制,保证其结果稳定可靠。为了保证检测结果的可靠性,实验室需要正确评估实验室性能和选择室内质控规则和每批质控测定值个数。实验室可利用西格玛性能验证图评价检测性能并选择适当的每批质控测定值数量和质控规则。
本文选取参加了卫生部临床检验中心开展的2015年全国肿瘤标志物室间质量评价(external quality assessment,EQA)计划并上报了肿瘤标志物室内质量控制(internal quality control,IQC)数据的某一家临床实验室,将实验室IQC累积在控变异系数作为CV的估计值,用实验室EQA中的百分差值作为实验室的偏倚估计,采用四种允许总误差对实验室性能进行评价,包括三种生物学变异导出的允许总误差(TEa)[2]和目前EQA评价标准的允许总误差。利用临床检验定量测定室内质控规则评价和选择软件绘制该实验室肿瘤标志物所有项目的西格玛性能验证图,并为不同项目选择不同质控规则[3]。
材料与方法
1. 室间质量评价计划样品:2015年肿瘤标志物室间质评计划材料为10个批号不同浓度水平的质控物,冻干品,2-8℃保存。复溶时,每瓶样品中准确加入2ml去离子水或蒸馏水,加盖在室温中放置30分钟,轻轻混匀至完全溶解后使用常规方法对每个批号的质控物进行单次检测并回报结果。
2. 室内质控样品:质控品为商品化质控品,批号为40301和40302。
1. 数据采集:选择2015年卫生部临床检验中心室间质评用户中参加本年肿瘤标志物室间质评的某一家实验室。实验室按照要求按时检测室间质量评价材料和室内质控材料,通过网络平台上报EQA和IQC数据,包括实验室编号、实验室名称、所用方法、IQC累积在控变异系数(coefficient of variation,CV)和EQA结果等。本文选取的肿瘤标志物项目一共八项,分别为:甲胎蛋白(AFP)、癌胚抗原(CEA)、糖类抗原(CA)19-9、CA125、CA153、铁蛋白、β2-微球蛋白和总前列腺特异抗原(PSA)。
2. 不精密度水平估计:选取该实验室2015年9月上报的肿瘤标志物室内质控累积在控变异系数(相同批号质控品累积2个月)作为该实验室不精密度水平的估计值。由于该实验室使用了两个浓度水平的质控物质,使用合并CV对该实验室不精密度进行估计。计算公式为CVt= ((CVlevel 12+CVlevel 22)/2)1/2。
3. 偏倚估计:选取该实验室参加2015年两次肿瘤标志物EQA计划的数据,计算该实验室结果与相应批号EQA样品靶值的百分差值,EQA样品靶值为相同方法组EQA结果中位数。由于两次肿瘤标志物EQA项目包含了10个批号的质控品,所以取10个百分差值绝对值的平均值作为该实验室该项目的偏倚统计。
4. 绘制西格玛性能验证图:将固定格式的允许总误差、偏倚和变异系数数据导入卫生部临床检验中心与北京科临易检信息技术有限公司共同开发的临床检验定量测定室内质控规则评价和选择软件中,绘制西格玛性能验证图。采用四种允许总误差对实验室性能进行评价,包括三种生物学变异导出的允许总误差(TEa)和目前EQA评价标准的允许总误差。
5. 根据西格玛水平选择质控规则:根据西格玛性能验证图,为不同项目选择适当的质控规则。若某项目σ值>6,即13s规则,N= 2,R=1,项目σ水平在5~6则使用13s/22s规则,N=2,R=1,σ水平在4~5则使用13s/22s/R4s/41S规则,N=4,R=1或N=2,R=2,<4σ则使用13S/22S/R4S/41S/规则,N=4,R=2或N=2,R=4。
结 果
对该实验室肿瘤标志物各项目进行偏倚(Bias%)和不精密度(CV%)的评估,并按照计算公式计算各项目的西格玛值,结果见表1。按照生物学要求,当使用基于生物学变异导出的最低允许总误差(TEa%)质量规范,CA153、铁蛋白和β2-微球蛋白项目的σ<3,AFP和CEA项目4≤σ<5,σ≥6的项目有CA125、CA199和总PSA。使用适当生物学变异TEa%时,CEA、CA125、CA199和总PSA项目的σ>3,而AFP、CA153、铁蛋白和β2-微球蛋白的σ<3。使用最佳生物学变异导出的TEa%质量规范,所有项目均无法达到3σ水平。当使用EQA评价标准的TEa%时,CA125、铁蛋白和总PSA项目的σ<3,AFP、CEA、CA125、CA199和β2-微球蛋白能达到3σ最低可接受水平。
使用卫生部临床检验中心与北京科临易检信息技术有限公司共同开发的临床检验定量测定室内质控规则评价和选择软件,将固定格式的允许总误差、偏倚和变异系数数据导入软件中,绘制西格玛性能验证图,见图1-4。图中斜线划分的区域从右上到左下依次代表“σ<2(不可接受)”、“2≤σ<3(欠佳)”、“3≤σ<4(临界)”、“4≤σ<5(良好)”、“5≤σ<6(优秀)”和“σ≥6(世界一流)”。当使用生物变异导出的最低TEa%质量规范,有3个项目可达到σ≥6(图中蓝色斜线以左),而有3个项目σ<3。当使用生物变异导出的适当TEa%质量规范,仅有1项的σ>5,4个项目<3。当使用生物变异导出的最佳TEa%质量规范,所有项目的σ<3。根据EQA评价标准的TEa%质量规范,有3个项目未达到3σ水平。

图1 根据生物学变异导出的最低TEa%质量规范的肿瘤标志物西格玛性能验证图

图2 根据生物学变异导出的适当TEa%质量规范的肿瘤标志物西格玛性能验证图

图3 根据生物学变异导出的最佳TEa%质量规范的肿瘤标志物西格玛性能验证图

图4 根据EQA评价标准的TEa%质量规范的肿瘤标志物西格玛性能验证图
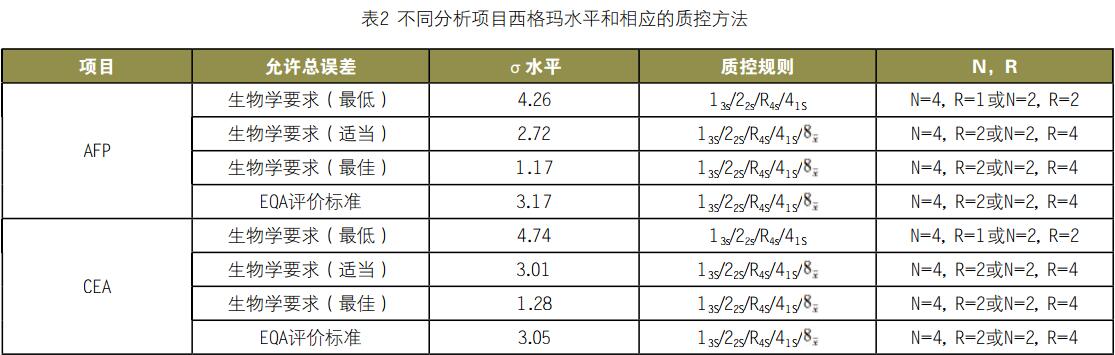
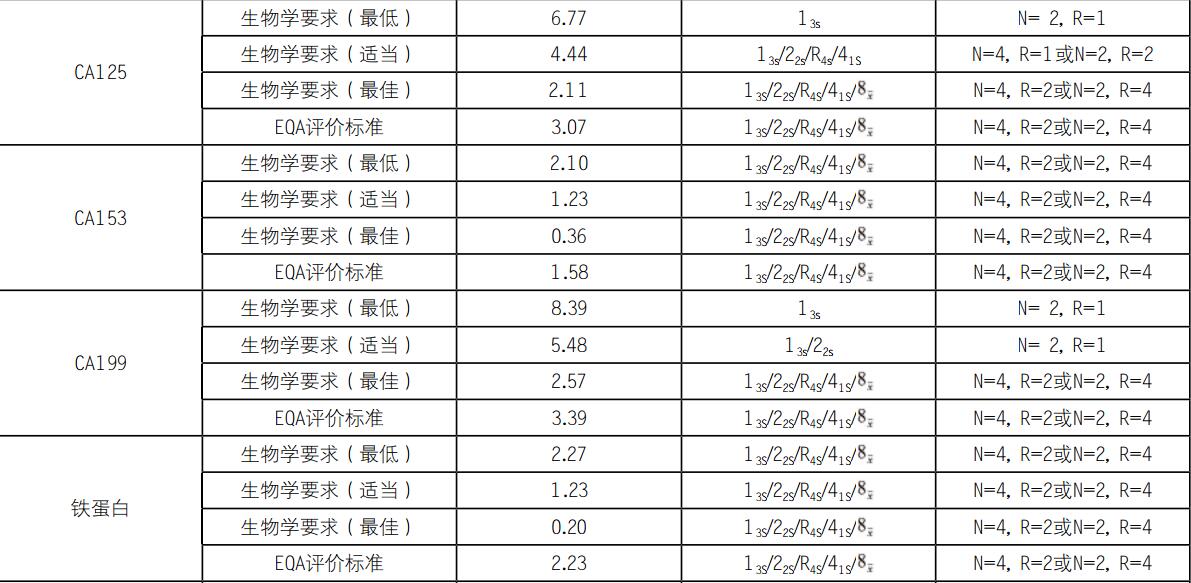
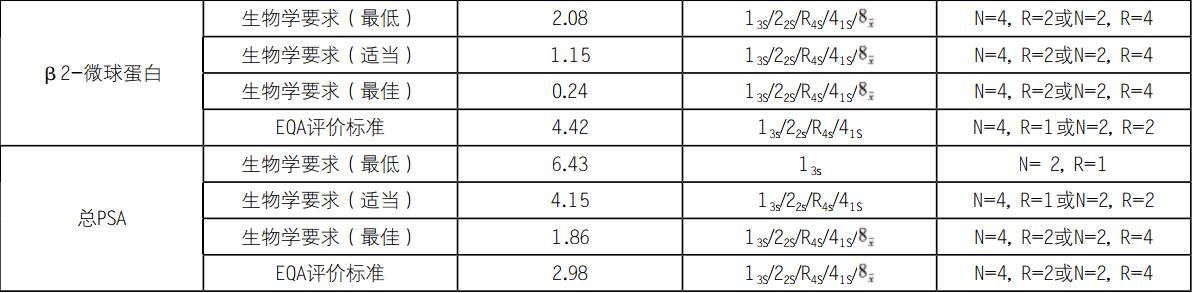
对于AFP和CEA项目,根据生物学要求的最低TEa%质量规范的σ分别为4.26和4.74,应选择13s/22s/R4s/41S规则,N=4,R=1或N=2,R=2,其他3种要求的σ<3,应选择13S/22S/R4S/41S/规则,N=4,R=2或N=2,R=4。对于CA153和铁蛋白项目,所有TEa%质量规范的σ均小于3,应选择13S/22S/R4S/41S/规则,N=4,R=2或N=2,R=4。对于CA125和总PSA项目,根据生物学要求的最低TEa%质量规范的σ≥6,可选择13s规则,N=2,R=1。具体各项目选择规则见表2。
讨 论
σ是一种评估产品和生产过程特性波动大小的统计量,其大小可以反映质量水平的高低[4]。6σ管理最早用于工业管理,在检验医学中的应用最早由国外学者Nevalainen提出,将实验室差错或缺陷率转化为σ水平进行评价和管理[5],6σ质量水平意味着100万次机会中有3.4个缺陷的可能,或者由公式σ=(TEa-|Bias|)/CV(TEa:允许总误差,Bias:相对偏倚,CV:变异系数)计算获得。6σ可用于检验全过程的质量管理,对检验中阶段,可通过测量变异的方法利用公式计算评价实验室检测性能水平,并根据σ水平设计最优的质量控制方法,这种方法无需考虑各项目的不精密度、偏倚和总误差是否满足要求,评价过程简单易行。对于检验前阶段和检验后阶段,可以通过测量结果的方式,将百万缺陷数转换成σ水平,对过程进行有效的评价[6]。
将上述的公式变形成为σ=(1-|Bias|/TEa)/(CV/TEa),即可得到西格玛性能验证图。在西格玛性能验证图中,横坐标为CV/TEa,纵坐标为|Bias|/TEa,相当于将不精密度和偏倚通过TEa进行标准化,所以即使不同的检测项目具有不同的允许总误差,也能在同一张西格玛性能验证图上展示出多个实验室的西格玛性能水平,可以直观地获得各实验室西格玛水平的分布情况。西格玛性能验证图是一种方便实用的工具,可清楚的展示出各个项目的σ水平分布区间,实验室仅需将允许总误差、偏倚和变异系数数据导入西格玛性能决定图绘制软件中,就能找到某项目所在的西格玛水平区间,选择相应的质控规则和每批质控测定值个数。
精密度是在规定条件下,对同一或类似被测对象重复测量所得示值或测得值间的一致程度[7],通常用不精密度来表示,包括标准差、方差或CV。其估计值应尽可能真实地反映实验室日常操作中的性能,所以最佳的估计不精密度的方法为采用常规的、历史的不精密度,有时也称为累积CV。本文中采用该实验室的长期累积在控的质控数据计算得到的CV,即累积在控CV来作为其不精密度估计,能真实地反映其检测项目的精密度水平。其他估计不精密度的方法还包括计算:(1)总不精密度,也叫做中间精密度;(2)日内或批间不精密度;(3)批内不精密度。为了满足较好的精密度,实验室应该注重整体的室内质控情况,对出现问题的检测项目进行及时的整改。同时需要进一步建立和执行书面的质量控制程序来监测和评价分析过程,以确保患者检测报告的准确性和可靠性。实验室还应考虑目前的实际情况,评估自身能达到的质量水平,为实验室设置合理的标准。实验室的正规操作,仪器的定时保养和校准,试剂的保存和使用,校准品、质控品的复溶、保存和使用等均会影响室内质控的变异系数。
偏倚是系统测量误差的估计值,是检验结果正确度指标,指同一实验室用同种方法多次独立检验分析同一样本所得结果的均值与靶值之间的差异。目前肿瘤标志物室间质评多采用冻干质控材料作为样品,按照方法学分组,去掉离群值后将同一方法组的中位数作为靶值,实验室测定结果与靶值间的偏差作为偏倚的估计,由于质控材料具有基质效应,且测定结果由实验室单次测定获得,获得的偏倚具有一定的局限性。
本文中在西格玛性能验证图上显示了某一实验室所有肿瘤标志物项目的性能水平,采用了四种评价标准,分别为生物学变异导出的三种质量规范和EQA评价标准。从生物学变异上看,多数肿瘤标志物的个体内和个体间变异较大,其导出的质量规范也较宽,β2-微球蛋白的个体内和个体间生物学变异较小,对检测系统或方法的要求较高,因此在采用基于生物学变异导出的质量规范时β2-微球蛋白的σ水平较小,需要采用的质控规则更为严格。总的来说,该实验室的肿瘤标志物项目的检测性能有待提高。
参考文献
[1] Meany DL, Sokoll LJ, Chan DW. Early detection of cancer ; immunoassays for plasma tumor markers [J]. Expert Opin Med Diagn, 2009, 3(6):597-605.
[2] 王治国主编. 临床检验生物学变异与参考区间[M].北京:人民卫生出版社, 2012.
[3] 费阳, 王薇, 王治国. 临床检验室内质量控制规则设计新工具—Westgard西格玛规则[J].现代检验医学杂志. 2015, 30(1):149-152.
[4] 王治国. 临床检验6σ质量设计与控制[M].北京:人民卫生出版社,2012.
[5] Nevalainen D,Berte L,Kraft C,et al.Evaluating laboratory performance on quality indicators with the six sigma scale[J].Arch Pathol Lab Med,2000,124( 4) : 516-519.
[6] 章晓燕,王薇,赵海建,王治国. ISO15189:2012与六西格玛级别[J]. 临床检验杂志,2015,33(11):846-848.
[7] JJF 1001——2011. 通用计量术语及定义[S].中华人民共和国国家质量监督检验检疫总局,2012.




