ISO 17043认可的国际EQA计划— ESfEQA
正确度(偏倚)的评估 —— 室间质评而非室内质控
通俗地说,对于医学实验室而言,检测系统的质量控制,有两个最基本的监控指标,一个是稳,另一个则是准。稳和准,是两个不同的概念,前者是反映检测系统的随机误差即精密度,主要的监控手段是室内质控(IQC);后者则是反映检测系统的系统误差即正确度,主要的监控手段是室间质评(EQA)也称之为能力验证(PT)。
虽然有不少医学实验室希望通过室内质控同时监控精密度和正确度,比如认为使用定值质控品,通过与赋值表比对,就可以监控正确度,这种做法本身是缺乏足够理论依据的。“鱼与熊掌不可兼得”,定值质控品的赋值表仅仅只有参考价值,室内质控目的也仅仅只是监控检测系统的精密度,不能作为判断正确度的手段。
在CLSI GP27-A2 Using Proficiency Testing to Improve the Clinical Laboratory; Approved Guideline—Second Edition文件当中这样写道:In addition to providing processes for tracking laboratory performance, this document includes guidance for other reviews of performance of different methods, such as reproducibility and bias, which should be performed by the providers of PT and by laboratory oversight bodies. 也就是说,室间质评(即能力验证)才可以评估不同检测系统的再现性(Reproducibility)和偏倚(Bias)。
ISO 17043 — 室间质评/能力验证的国际标准
目前越来越多的中国医学实验室谋求通过ISO 15189认可,因为ISO 15189是国际通行的对医学实验室质量和能力的认可准则,国际标准化组织(International Organization for Standardization, ISO)本身的权威性也是不容置疑的。正如ISO对医学实验室制定了相应的国际标准,ISO也同样对室间质评/能力验证的组织者也制定了相应的国际标准 —ISO 17043。
ISO 17043 : Conformity assessment -- General requirements for proficiency testing对室间质评/能力验证组织者提出了10项技术要求和15项管理要求,作为室间质评组织者必须在人员、室间质评计划的设计(样品准备、样品的均一性和稳定性评价、统计设计、靶值确定)、室间质评计划的运作(给参加者的指导,室间质评样品的处置和存储,室间质评样品的包装、标识和分发)、数据分析和室间质评计划结果的评价(数据分析和记录、能力评定)、报告、与参加者的沟通、保密方面按准则要求建立完整的管理体系。
多多益善 — 室间质评/能力验证
Mayo Clinic(梅奥诊所)是全美规模最大、设备最先进的综合性医疗体系之一,2014~2015 U.S. News & World Report将其排名为全美医院的第一名。素有“医学麦加”之称的Mayo Clinic下属医学实验室,如何对待室间质评/能力验证计划,是一个值得讨论的话题。图1为Mayo Medical Laboratories所参加的部分室间质评/能力验证计划的列表。概括起来,就是四个字:多多益善。

全球最顶尖的医院,它的实验室参加如此之多的室间质评/能力验证,不能不说是对中国医学实验室的一个启迪。其实国内医疗管理部门也是鼓励医学实验室参加不同层级的室间质评计划。如下图,在《三级综合医院评审标准实施细则(2011年版)》,鼓励三级医院同时参加省级、国家和国际室间质评/能力验证计划。

德国医学实验室质量管理标准 — RiliBÄK
德国的医学实验室管理一向以严格著称,德国医学委员会(BÄK)针对医学实验室最基本的质量要求,制定了RiliBÄK标准(类似于美国的CLIA)。RiliBÄK的质量要求基本保持与ISO 15189同步,提出了特定的质量要求、允许误差和不确定度的建议。2007年版的RiliBÄK(目前最新版本为2014版)所规定的项目涵盖了67项血清和全血检测项目、10项尿液检测项目,以及7项CSF的检测项目。
RiliBÄK采纳了一套和我们过去所学有所不同的质量控制统计方法,它以至少15个质控结果作为一个质控周期(Control Cycle; CC),计算%RMSD (%Root Mean Square Deviation),公式如下:
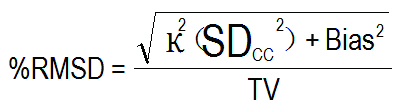
RiliBÄK对德国医学实验室的室间质评也做出具体要求,如果上述项目连续二次室间质评不合格,实验室必须向BfArM(类似于美国的FDA)报备,否则最高罚款可达25,000欧元。
ESfEQA — 立足德国、面向欧洲、覆盖全球
ESfEQA(European Society for External Quality Assessment)是由德国ESfEQA推出的主要面向全欧洲的国际性医学实验室室间质评计划,并已通过ISO 17043认可。ESfEQA室间质评计划主要分为生化、免疫、血液和细菌四大主要领域。ESfEQA室间质评计划主要有以下特色:
•国际性
ESfEQA室间质评计划,为中国医学实验室加入高水准的国际性室间质评计划提供了一个机会。
•ISO 17043认可
来自德国的ESfEQA室间质评计划秉承德国标准,通过ISO 17043认可,凸显其优异品质。
•互通性
由于室间质评样品被用于评估不同的检测系统,保证结果的互通性是室间质评计划的重点。ESfEQA室间质评计划所有的样本全部来自于人源,最大程度保证了结果互通性,使评估结果更为科学、有效。
•全程可信赖
ESfEQA围绕整个室间质评计划流程:质评样本的生产和材料选择,发货物流以及电子数据和结果处理等环节,建立可信赖的全面质量管理体系。
•基于网络的数据录入及结果反馈
ESfEQA室间质评计划提供一个易用的网络访问界面,使参与的医学实验室能够轻松录入质评结果,并以PDF形式获得易于存储的电子化质评报告。
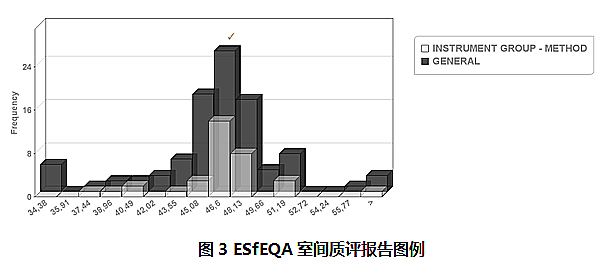
结 语
正如CLSI GP27-A2所指出的,良好的室间质评是提升医学实验室质量管理水平不可或缺的重要工具之一,遵循ISO 17043的欧洲ESfEQA国际室间质评计划将有利于中国医学实验室进一步提高检测质量,与国际先进水平接轨。
上海昆涞生物科技有限公司 供稿





