HCV感染诊断和管理中的检测问题
Patricia Slev,犹他大学病理学专业副教授,ARUP实验室医学主任。David R. Hillyard,犹他大学医学院病理学副教授,ARUP分子病理学实验室分子传染病、分子肝炎/逆转录酶病毒和分子测序医学主任。两位教授同时在2015 AACC年会中就“HCV和HIV在感染诊断和管理中的检测问题”进行报告,现编译、整理HCV相关问题,呈现给读者。
文章以病例为开端介绍HCV感染诊断和管理中的检测问题。
HCV 病例1
55岁男性,无高风险行为历史,出生在美国,到初级护理医师处进行每年例行体检;该男性进行了常规实验室检测,出现了肝酶浓度升高的状况。假设患者出现了这种肝酶升高的结果,并假设患者的年龄,那么这样的患者应该接受什么样的检测,应对患者进行哪种类型的肝炎病毒检测?正确选项是丙肝病毒检测。
HCV在1989年被发现,是一种输血后的非甲非乙型肝炎。丙型肝炎病毒属于病毒科,是一种小型包裹式单链阳性RNA病毒(直径50nm)。丙肝病毒会在肝细胞中进行复制。美国已有上百万人感染了这种病毒。在发病高峰期的上世纪90年代早期,该种肝炎可以在血液、献血者和器官捐献者中筛查出来,但是当时的技术条件不能跟踪这种病毒的发病,感染的机理等问题,所以还是出现了肝硬化发病的一个较小的高峰。
丙型肝炎的自然病程还表现为急性丙型肝炎很少被诊断出来,然后约85%的急性丙型肝炎发展为慢性丙型肝炎,然后约20%的慢性丙型肝炎发展为肝硬化,最终约1-5%的肝硬化患者发展为肝癌。丙型肝炎是美国导致肝脏移植,肝硬化和肝脏衰竭的头号疾病。每年约有10000人死于丙型肝炎。
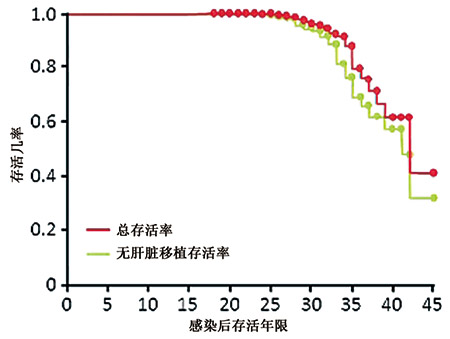
图1. 上世纪70现代澳大利亚感染丙型肝炎病毒的485名血浆献血者
(平均随访年限为31年)
■第一次肝脏移植:感染后18年
■首个死亡案例:感染后28年
HCV的传播途径主要有以下几种:1 药物或毒品注射传染占到总传染比例的60%;2 性接触传染占到总传染比例的15%;3 未筛查的输血和器官移植占到总传染比例的10%;4 医护工作者被感染或围产期妇女或新生儿传染占到总传染比例的5%;5 还有10%的传染是未确定的风险因素。
根据上述传染途径,建议筛查要有针对性地进行,筛查的主要目标包括:进行过或正在进行药物或毒品注射的人群(即使仅注射过一次);有可能接触到HCV病毒的人群、HIV人群、血液透析人群、转氨酶升高的人群;在1992年以前接受过输血或器官移植的人群;母亲为HCV感染的儿童人群;暴露于HCV环境的医护工作者;性伴侣感染HCV的人群。婴儿潮时代出生的人群(1945-1965年出生的人)应该至少接受一次筛查。HCV的筛查变得越来越重要,但是我们已经不需要RIBA(重组体免疫印记分析)等方法了,因为HCV的筛查已经被大大简化了。实验室对HCV感染的测试包括血清学测试即抗HCV抗体筛查测试(EIA或CIA)以及病毒检测-HCV RNA 定性PCR或定量实时PCR。
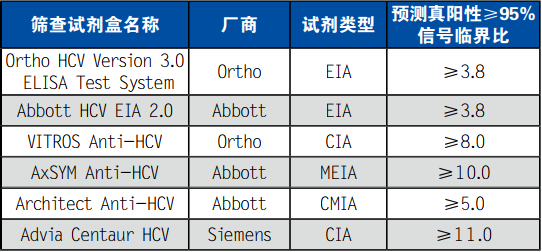
表1. 一些厂商所生产试剂的临界比
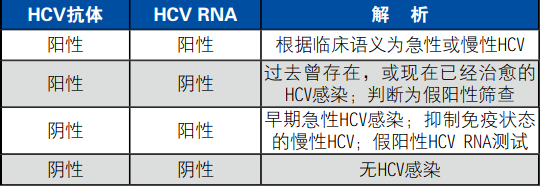
该规则为HCV检测规则的2013年版本,规则如下:首先患者应接受HCV抗体测试,如测试结果为阴性则说明患者无HCV,可以终止进一步的测试;如果患者的HCV抗体测试有反应,则患者应接受HCV RNA测试,如HCV RNA测试未检测到RNA,则可以认定为当前无HCV感染;如果检测到HCV RNA,则认定为当前有HCV感染。检测结果的解析则可以参照下表的规则(见表2)。
表2. HCV检测结果的解析
HCV会引起慢性肝病,而慢性肝病会引起渐进性肝纤维化进而发展为肝硬化和肝细胞癌,肝硬化也可以引起肝细胞癌。因此渐进性肝纤维化的诊断和检查是非常重要的。目前肝纤维化的评估主要有三种方式:1、活体组织切片检查;2、血清生物标志物检查;3、瞬变弹性图检查。
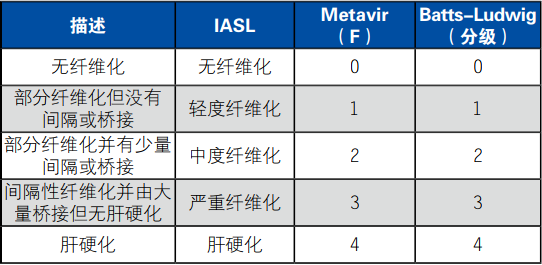
活体组织切片检查是检查的黄金标准因为这是最直观准确的检查。血清检查的痛苦较小,但是近来随着成像技术的进步瞬变弹性图成为检查的主流。任何一种形式的检查都必须有相应的评判规则,表3为肝纤维化检查的评判规则。
表3. 纤维化组织学分级评分规则
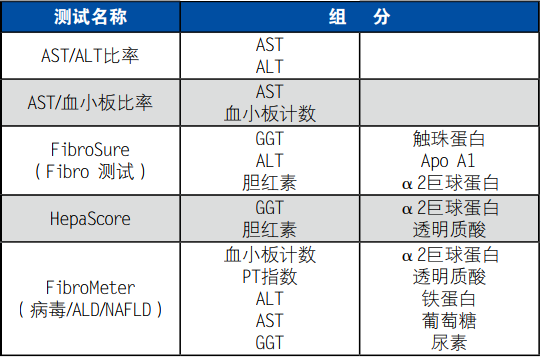
除活体组织检查之外可以通过间接测试,已经有一些生物标志物用于肝纤维化的检查与诊断,通过对生物标志物的浓度等指标的分析判断肝纤维化的存在及发展程度。通过直接测试即实验室非常规测试进行细胞外间质重新分布。直接测试包含ECM酶、胶原退化片段等分类详见表4。
表4. 常见直接测试
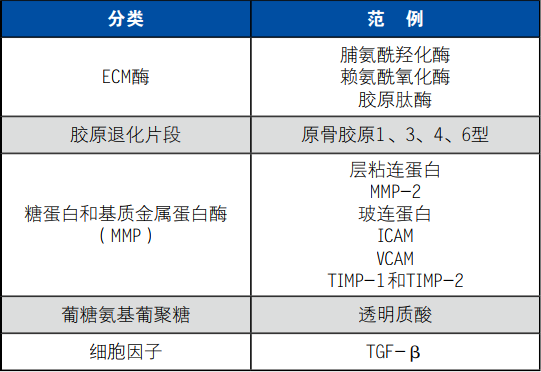
间接测试就是临床实验室普遍执行的测试(有些例外),通过反映肝功能改变的生物标志物检测肝脏损伤和炎症,常见测试见表5。
表5. 常见间接测试
肝脏活体组织切片是管理患有HCV引起的慢性肝脏疾病患者的基础,而且目前仍然是评估肝纤维化的重要参考方法。在HCV感染的个体中,结合两种或更多血清生物标志物试验或更多生物标志物试验的规则以及瞬变弹性图可以用于提高肝纤维化分级的准确度并减少所需活体组织检查的次数。
HCV 病例2
一名被视为具有高慢性HCV的患者正在急诊室接受治疗,对于这样的患者应该申请什么样的测试,进行相关即时诊断应该有什么样的测试申请考虑?在急诊室这样的环境首先会用灵敏的试验对患者筛查,但是即使再灵敏的试验都需要仰仗试验的特异性,特异性是试验的关键,试验要进行分子试验进行确认。对于急诊室环境中具有高慢性HCV感染风险患者,肯定需要进行大量的跟踪试验进行观察,如果患者最初的筛查结果为阳性,那必须进行分子试验确认。
HCV分子试验能做出诊断(对先前试验进行确认),可以对预后进行指示如基本病毒载量(弱)和基因分型(强),还可以进行治疗监视包括终止一些治疗规则。通过对患者的用药和输血记录进行审查可以得到非常可靠的信息,这对开始下一步的疗法至关重要。阳性或真阳性的概率通常为50%,所以必须对先前试验进行分子试验确认。在得到这些信息之后,就要进行病毒载量检测,病毒载量预测值能为将来使用抗病毒疗法提供少量参考依据,之所以把病毒载量测试作为第一步是因为他是监视疗法和引导治疗以及引导用药的先决步骤。基因分型是DNA指导治疗和指导用药的先决步骤,具有同样的重要性。治疗的规则取决于治疗中某些疗法获得的数据的临界值。在使用一种新的药物时,考虑基因分型、病毒载量,做出诊断,然后决定治疗间隔。即使在最近的3年内,仍然很多人惊奇于治疗规则为何变化如此之快,治疗规则的变化完全是根据患者的具体情况而定。
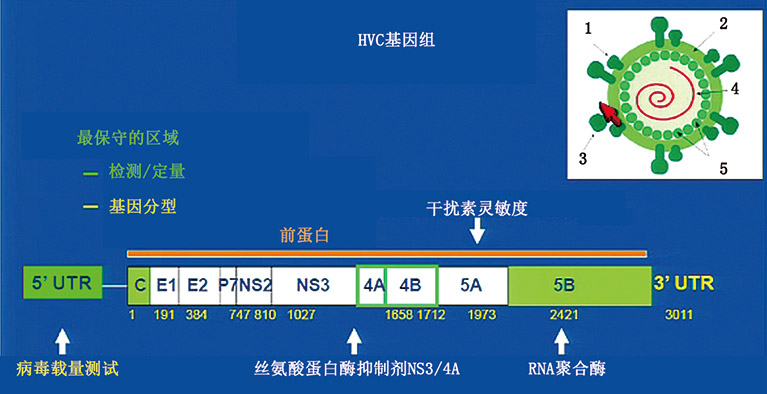
为了让读者能更清楚地理解试验是如何靶定病毒,靶定病毒哪些位置的问题,下图为病毒示例以及试验靶定病毒的5个区域(见图2)。所有的病毒载量试验均以这几个区域为目标。在早些年,基因分型试验也以这些区域为目标。大概十年以前,基因分型针对的其实是子类型。在那个时候1A和1B都不能进行可靠的区分。不同厂商生产的不同试验对同一区域产生的结果也不同,直到近年来出现了统一标准和PCR试验,问题才得到解决。最早的病毒载量测试针对C区域,丝氨酸聚合酶抑制剂NS3/4A可以针对4A和4B区域;干扰素可以针对5A区域,RNA聚合酶针对5B区域,从5个非编码区域可以靶定发现到3个非编码区域也可靶定。目前可行的实时HCV试验有Roche V2和Abbott,这两个试验均经过FDA批准,下一代的试验平台即将出现,而其他厂商也在着力于该平台的研发,如西门子的KPCR。
图2. 图中白色图片五个区域是:1、包膜糖蛋白(E1);2、囊膜脂质;3、包膜糖蛋白2区(E2);4、SS-RNA 基因组[-9.6kb];5、衣壳蛋白(病毒核心)
不同厂商的试验有不同的检测下限,这些下限的确认彼此之间也不相关。因此在检测患者是否为阴性时,多低的试验检测下限代表患者为阴性呢。检测的下限以能检测到病毒为主,但能检测到病毒不一定就是下限,下限无法进行量化。实践提醒我们要在不同的浓度进行采样并进行多次重复试验,对病毒载量进行重复检测并报告。由于PCR和采样出现断点时要进行确认,检测要包括低于检测限的样品,出现不合格或阴性结果时注意进行重复试验,测试良好但不能完美协调时也许重复试验,出现少于预期的不合格时重复试验。在动态中把握下限的检测。
确认应注意的问题有再确认时要使用“灵敏的”HCV RNA试验;所有当前HCV病毒载量试验必须非常灵敏,但都不是FDA批准的试验,所以不可用于诊断(虽然是确认的标准);使用定量试验进行确认时要注意处理过程和耗费的经济性,因为要建立基准病毒载量进行治疗监视。
需要注意的问题筛查和PCR确认之间有时间差;通过CDC允许的PCR对筛查样品进行重新检测可能面临污染的风险;2代试管PCR血清测试可能出现假阳性;血清学和潜在分子测试之前要预先等分;未满足的要求:筛查试验/过程需要统一。
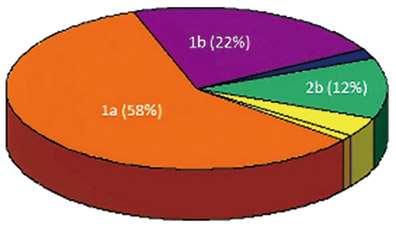
在美国最常见的基因分型是1a和1b,约占到总病例数的80%。1a比1b数量要多,而且不幸的是1a可能是最难以治疗的分型。虽然1a并不是最具侵袭性的分型,但是侵袭性和难以治疗是两个概念,1a是最难以治疗的分型(见图3)。
图3. 美国的HCV基因分型
HCV的基因分型方法可以通过LiPA(反向杂交线性探针)的方法,这个方法使用了很多年,并能针对5’UTR和病毒核心进行分型,所以这种方法在以前用于对1a和1b进行分化,效果不佳;核酸筛查试验针对5’UTR,病毒核心和NS5,所以这种方法可以对子类型进行基因分型;引物特异性PCR是FDA唯一批准的PCR试验,针对5’UTR和NS5B,该试验具有大量的引物可以根据SNAP确定是否进行扩增;GenMark针对的也是5’UTR和病毒核心,具有与前者类似的功能。
基因分型面临的问题有5’UTR靶定试验不能有效的区分1a和1b,和1型及罕见的6型病毒,但是对1a和1b以及1型和6型进行区分却很重要;而且使用病毒核心和NS5B进行区分的方法在解析方面序列可变性可解析百分比很低,根据试验设计的人群不同,这个百分比为3%,或5%-6%。当出现这个比率又要进行分型确定疗法时,只有综合使用多种方法进行分型一条途径,PCR方法可能更加恰当一些。
HCV 病例3
一名接受治疗10年的患者却在肝功能出现恢复后被查出出现了早期慢性HCV感染(SVR),这有没有可能一种SVR HCV治疗后的复发?其他与临床诊断相关的那些感言应被考虑?应该申请哪些测试?出现第一个问题提到的情况可能是患者在终止先前疗法并开始新疗法的时候又被感染了,这可以继续进行治疗。对于第二和第三个问题,则可以进行重复测试。
这是丙型肝炎治疗方法的沿革,从标准干扰素发展到干扰素/病毒唑,在发展到长效干扰素,再到长效干扰素/病毒唑,再到最新的PI+长效干扰素/病毒唑,但是患者对这种方法并不满意。因此需要替代疗法和预后的预测因子。替代疗法的使用年龄要大于18岁,要能区分疾病所处的阶段并无处方禁忌症等条件都具备才能使用,而且预测因子也很复杂,涉及年龄、性别、种族、是否出现肝脏纤维化、是否有胰岛素耐药性等等,所以指导疗法势在必行。
指导疗法的趋势一是基因分型指导疗法,这包括一些分型时间较短的处方疗法(GT2、3,干扰素病毒唑疗法);还包括其他分型时间较长的处方疗法(GT1、4、5、6,干扰素病毒唑疗法);另一个趋势为应答指导疗法(传统疗法)。
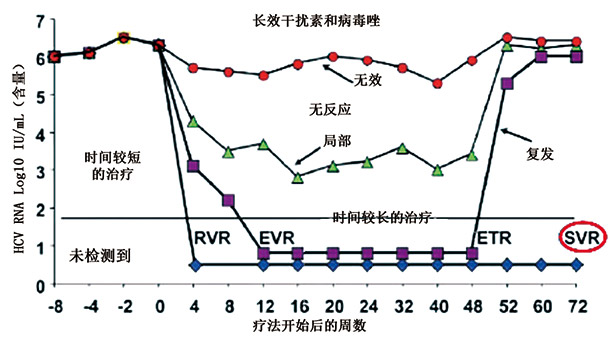
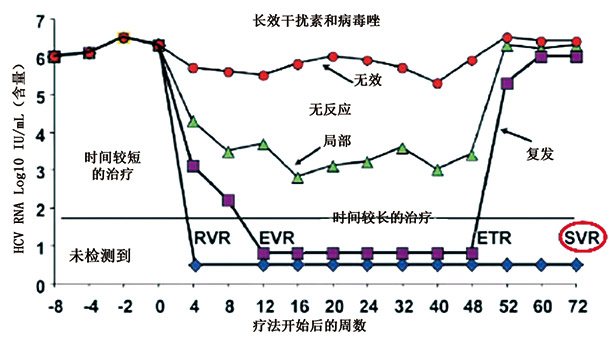
由图4可见传统疗法受到最初诊断后的病毒载量,并与采用疗法后的效果相连。按上图所示由蓝色点形成的线虽然病毒载量降到了很低的范围,但始终具有持续病毒应答,这就进入了治疗时间较长的阶段;紫色点构成的线虽然也显示出疗法的显著,但是在出现结束疗法应答后出现了复发;绿色点构成的线显示出疗法部分有效,而红色的线则说明疗法无效,对疗法无反应。紫色点构成的线反应患者需要接受新的DNA疗法,而绿色点构成的线则表明患者在最初的阶段病毒载量估计不足。
治疗的目的在于结束病毒应答,最终检测不到病毒存在。而在不可检测到病毒但出现持续病毒应答时,说明有了较好的治疗效果。SVR基本上代表着病毒学概念上的治愈,在这个阶段,病情不会再发展,出现肝脏组织有所好转,呼吸困难现象减少、肝细胞癌风险降低、死亡率降低的等诸多临床受益现象。所以应答指导疗法是第一代的直接抗病毒疗法,并取得了良好的效果。
图4. 疗法应答的差异性
HCV 病例4
一名新近被诊断出HCV感染的患者希望接收治疗。医生建议的治疗方法为联合使用sofosbuvir(SOF)和Simeprevir(SMV)。应该额外采用什么测试指导这种疗法?需要考虑测试性能的什么问题?再解释这两个问题之前必须指出的几点有NS3/4蛋白酶抑制剂对转译和聚合酶过程的作用、NB5B聚合酶抑制剂对RNA复制的作用,NS5抑制剂在HCV生命周期中的作用尚未明确,这几点都和药物的使用有关。建议HCV GT1型患者采取的非抗病毒治疗方法见下表6。
表6. 建议HCV GT1型患者采取的非抗病毒治疗方法
*HCV RNA<6百万IU/ML接受预先治疗的患者考虑是否缩短病程应由治疗提供者自己裁度并应该谨慎完成。
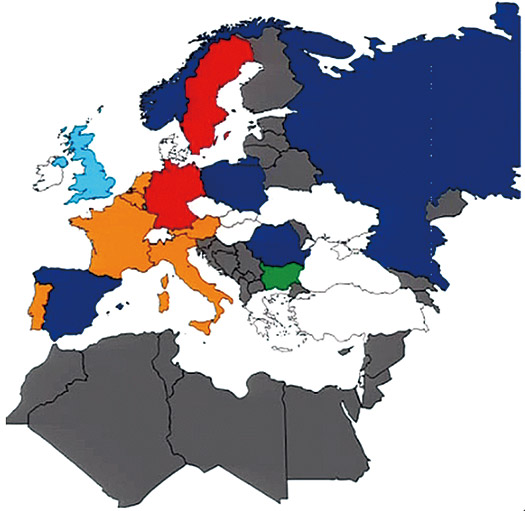
患有1a基因型HCV的患者比患有1b基因型HCV并接受某一疗法的患者具有更高的复发率。1a基因型的患者应该接受更加积极的治疗方法。不能进一步分为子类型的基因型1 HCV感染应视为基因型1a感染进行治疗。1a基因型HCV感染具有NS3Q80K多态性,这使得SMV/PEG/RNV的实际效价大打折扣,在联合使用sofosbuvir和simeprvir的患者中,1a基因型HCV并具有Q80K突变的患者具有更低的持续病毒应答率。HCV Q80K多态性的流行性分布(基因型1患者在欧洲的分布)见下图5。
绿色区域为无Q80K多态性分布的区域;蓝色区域为Q80K多态性分布小于5%的区域,橙色区域为Q80K多态性分布5.1%-10%的区域,红色区域为Q80K多态性分布10.1%-15%的区域;天蓝色区域为Q80K多态性分布15.1%-20%的区域;白色区域为HCV基因型1a分布小于20%的区域和HCV基因型1分布小于40%的区域,灰色区域为无数据区域。
图5. HCV Q80K多态性的流行性分布(基因型1患者在欧洲的分布)
面对如此严峻的形式必须对HCV的诊疗进行革新。HCV诊疗的革新应包括如下几个方面:病毒的发现,这是进行诊断和治疗的基础;改进治疗学,加深对HCV的认识;革新检验技术、综合使用高质量分子试验对HCV进行检测和分型;推广更大范围的人口筛查;通过教育,筛查和资源整合,并基于有效的管理建立专业团队;建立经济学模型让慢性HCV感染得到经济有效的医疗护理。
编译:张凯
审校:王小茜




