精准医疗是不是癌症治疗的未来 ——针对患者特征在正确的时间进行正确的护理
Richard L. Schilsky,FASCO医学博士,美国临床肿瘤协会医务副主任。Schilsky博士在2015 AACC年会发表题为《Is Precision Medicine the Future of Cancer Treatment》的报告。
一、癌症治疗的临床实践
临床环境中多年的实践证明,每名癌症患者的经历都是各不相同的。对患者进行针对性治疗和用药也不是什么新鲜话题了。针对患者的不同临床表现和预后状况,为患者指定不同治疗和生存计划。DNA检测技术彻底改变了传统的癌症治疗理念,通过对患者DNA和肿瘤组织的全面检测,人们认识到每个肿瘤都有独一无二的特征。通过大量的研究现在已经大大加强了对大细胞性淋巴瘤和乳腺癌的预测。作者多年从事非小细胞肺癌的研究,发现非小细胞肺癌具有众多独一无二的子类型,这个特征与许多其他类型的癌症具有共同性,这表明不同的子类型需要不同的诊疗计划。实体肿瘤通常会发生基因组改变,这对癌症的治疗形成了巨大的挑战。癌症基因有貌似可控的长尾效应,很大一部分的癌症可能都包含至少一种潜在的可控基因组改变,因此在这种情况下传统的临床试验设计很有可能不可行。面对这种情况就需要对癌症类型进行重新分类。通过对癌症的重新分类,并对分类进行细化,每种细化的癌症分类采取针对性方案,是一种行之有效的手段。并由此诞生了新的癌症病理学。
新型癌症病理学-新型肿瘤组织切片检查
新型肿瘤或组织切片检查分为两种类型。一种是组织切片病理学检查,另一种是基因组病理学检查。组织切片病理学检查可能检查出非小细胞肺癌,黑色素瘤和胶质瘤,但疗法归结为EGFR TKI疗法,使用这种方法只有很少的患者产生临床受益反应。另一种基因组病理学检查则可以通过三种不同的检查基因组ALK改变、MET扩增和EGFR突变实现三种疗法ALK TKI疗法、MET TKI疗法和EGFR TKI疗法,从而实现大部分患者的临床反应使其受益。
癌症生物标志物和抑制剂对治疗的意义
随着技术的日益发展,生物标志物的可信性越来越高。生物标志物已经可以用于癌症的预防、治疗和治疗后存活期的监测。生物标志物可以检测癌症的风险,进行预后预测并监测治疗反应。为靶向疗法的实施奠定了基础。实施靶向疗法需要进行标靶的确认,确认肿瘤组织中的目标是否表达,过度表达或突变;标靶在细胞增殖、细胞死亡和转移中是否具有重要作用;以及标靶抑制剂是否抑制了肿瘤的增殖和扩散。这对治疗具有重要的意义,癌症标志物和抑制剂对治疗的意义见图1。
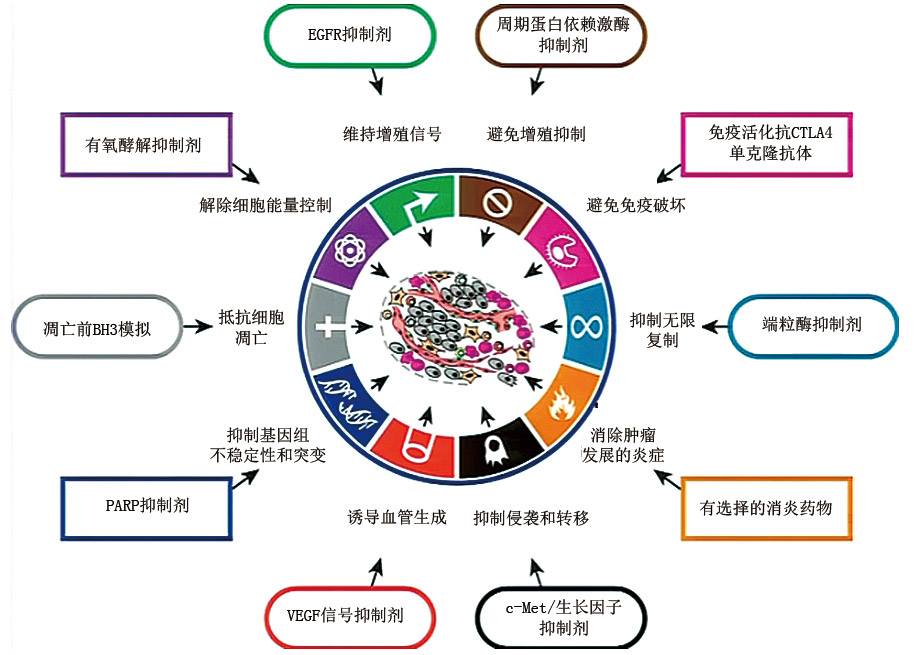
图1. 癌症标志物对治疗的意义
二、靶向疗法的要求
靶向疗法的要求包括:1、可信的分子标靶;2、具有可靠的试验来测量标靶或途径表达/能力;3、区分肿瘤细胞内的标靶表达;4、具有具备良好药物性能的强力特异性抑制剂;5、在使用抑制剂后,可以论证人体肿瘤细胞内的标靶是否得到抑制。
易瑞沙泛亚洲研究的设计
这项随机开放临床研究共纳入了1217例非小细胞肺癌患者。所有肺癌患者无吸烟史或有轻度吸烟史,组织学检查结果为肺腺癌。随机化后,609例肺癌患者接受吉非替尼250 mg/d治疗,608例肺癌接受卡铂+紫杉醇(CP方案)治疗。研究主要目的是在意向治疗分析人群中比较吉非替尼与CP方案治疗的无进展生存(PFS),次要终点包括总生存(OS)、客观有效率(ORR)、生活质量改善、症状改善和患者对药物的耐受性。
经22个月随访发现,吉非替尼组肺癌患者PFS显著优于CP方案组。值得注意的是,在治疗的前6个月,CP方案组PFS优于吉非替尼组,但随后16个月则吉非替尼组PFS显著优于CP方案组。这可能与肺癌表皮生长因子受体(EGFR))突变相关,在治疗的前6个月,常规化疗对无EGFR突变肺癌患者疗效较好,但化疗疗效不能长期维持。而吉非替尼的疗效则长期稳定,显示了吉非替尼的优势。EGFR突变分析结果显示了这一点,在突变人群中,吉非替尼治疗者PFS期长于CP方案治疗者,在无突变人群中则相反。另外,吉非替尼组ORR显著高于CP方案组该组肺癌患者耐受性较好,生活质量显著提高。图2为患者的CT结果比较,可以看到,使用ALK抑制剂后,患者的肺部阴影有明显的好转。
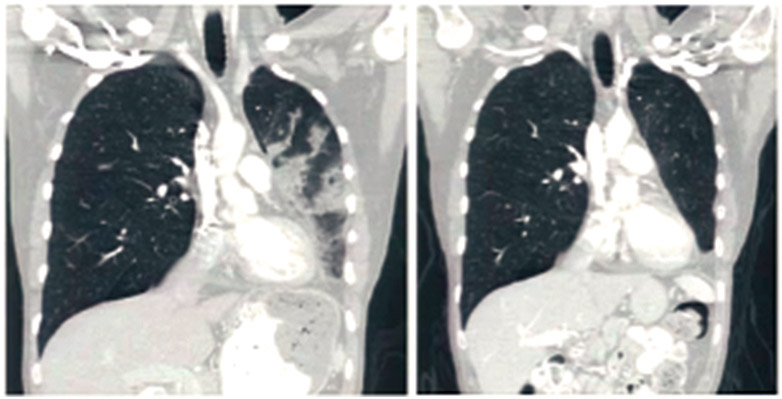
图2. 使用ALK抑制剂前后患者肺部CT对比
肺癌的治疗经过长期的发展,许多发现已经被应用到治疗体系中。1997年,EGFR抑制剂开始进行临床开发。1997-2004年间,发现肺部恶性肿瘤EGFR突变对吉非替尼和埃罗替尼敏感。2004年,埃罗替尼被证明可用于转移型或未转移型非小细胞肺癌的二线疗法。2004-2005年间,发现EGFR T790M 突变是TKI耐药性的机制之一。2005年,BATTLE研究上线,活体组织检查成为非小细胞肺癌治疗的主流。2007年,肺癌ALK重排被首次指出。2010年,证明埃罗替尼是接受4个周期一线化疗后为发展患者的维持疗法,同时第一个ALK克里唑蒂尼耐药点突变被证明。2010年后期,鳞状细胞肺癌的FGFR1扩增被发现。2011年初,克里唑蒂尼批准用于ALK阳性肺癌的治疗被提上日程。2012年,完成鳞状细胞肺癌的TCGA基因组特征分析。2013年,埃罗替尼和阿法替尼批准作为转移型非小细胞肺癌并且肿瘤发生EGFR外显子19del或L858R mut的突变患者的一线治疗方法。2014年,ramucirumab批准作为非小细胞肺癌的二线疗法,同时肺部恶性肿瘤的TCGA基因组特征测定完成。2015年,Nivolumab批准用于肺部鳞状细胞癌的二线治疗,同年发现突变负载与抗PD-1疗法的反应有关。
在具有肺部腺癌致癌因子的患者中,接受靶向疗法的患者的生存可能性明显高于未接受靶向疗法的患者;同时具有5种最常见癌症突变因子的患者,接受靶向疗法的,生存的可能性更高。接受Vemurafenib患者的总存活率比使用Dacarbazine的患者更高。接受Trametinib治疗的患者比化疗患者的生存率要高。
三、基因组驱动癌症医学所面临的机遇和挑战
肿瘤学已经作为基因组驱动框架的基础,这个框架在其他医学专科中独树一帜。但是这个框架具有一个众所周知的缺陷就是大量的基因组数据可能缺乏机遇临床实践、数据分析和解析,从而带来风险。基于上述两点,是否能通过基因组标签匹配疗法改善患者预后;以及通过基于基因组标签指定患者用药是否能够产生有益的效果成为两个关键的问题。但是大量的事实已经证明患者接受与肿瘤分子谱相匹配的疗法能实现更长的无进展存活期。
新型临床试验的设计
新型试验的设计基于以下两种类型一种是伞状类型—检测癌症的一种类型中不同药物对不同突变的影响,这些试验包括BATTLE、Lung-MAP、I-SPY 2和FOCUS4,另一种为篮状类型,检测在多种癌症类型中一种或多种药物对一种或多种突变的影响,这些试验包括NCI MATCH和NCI MPACT。
其中在法国进行了一种名为SHIVA的试验。SHIVA是一种基于肿瘤分子谱进行的随机化2期试验,同时将试验的结果与传统的疗法进行了比较的实验,两种试验涉及的患者均患有难以治疗的癌症。其中SHIVA的试验步骤是:1、患者登记;2、肿瘤组织切片检查;3、进行下一代基因组筛查;4、生物信息学研究;5、分子生物学匹配;6、试行可行的特异性疗法;7、找到合格的患者;8、再次进行患者知悉确认;9、通过后进行基于分子谱的靶向疗法;最终得到存活期终点。传统疗法则在患者确认后遵医嘱进行治疗。试验的结果是使用分子谱匹配疗法的患者存活中值为2.3个月,而使用传统疗法的患者存活中值为2.0个月。
SHIVA是为数不多的成功案例之一,其他试验的效果并不是十分的理想。为什么实现精准医疗的难度如此之大呢?原因反映为如下方面:1、基因组测试显示疗法缺乏有益性;2、未检测到可控的变异体;3、没有适用的药品;4、患者与不适于使用匹配的药品;5、患者预后不可估计。
四、疗法选择的分子学分析—NCI匹配,
一种联合NCTN/NCI的临床试验
NCI匹配试验的过程如下:1、基因测序;2、检测可控突变;3、研究药品;4、如果病情稳定,能实现完全或部分反应,则继续研究药品直到病情出现发展,如病情恶化则检测额外可控突变,如在第4步之初就出现病情恶化,则直接检测额外可控突变,如此循环往复。如果病情恶化却未检测到额外可控突变则终止研究。匹配逻辑如下:附带子协议的主协议要求多个合格的2期分子试验;协议模板指示的要求是在不影响其他方法的前提下可以添加或删除方法;单一药品或联合用药时,建议使用已知的2期药物剂量,并使用FDA批准的或研究的药物或联合药剂;通过机构审查委员会的审查,可以进行审查的地点包括2400个NCTN点;最后试验需经过CLIA实验室网络确认。在此基础上就可以对患者进行个体化用药,个体化用药需要具备以下条件:1、肿瘤已经经过组织切片或组织学分类;2、 提取了肿瘤活体组织切片检查;3、提取了肿瘤的DNA活体组织改变谱系;4、对可控突变肿瘤分子图谱进行了定义;5、使用基因改变图谱选择个体化靶向治疗方法。由于患者体内存在遗传异质性,所以上述个体化用药的方法不足以监视或理解出现的病情恶化和药物耐药性等现象。
耐药性问题
耐药性问题是治疗面临的重大问题之一。现在已经发现不同的基因组类型可以发展出不同的耐药现象。耐药性大部分为获得性耐药。获得性耐药有几种表现如目标发生改变,目标基因扩增,目标基因第二位点突变等;另一种是信号旁路,出现一种“补偿性回路”使药物绕过抑制的目标等,当然还有许多未解释的耐药性机制。以非小细胞肺癌为例,这种癌症的EGFR抑制剂耐药性机制的频率如图3所示。
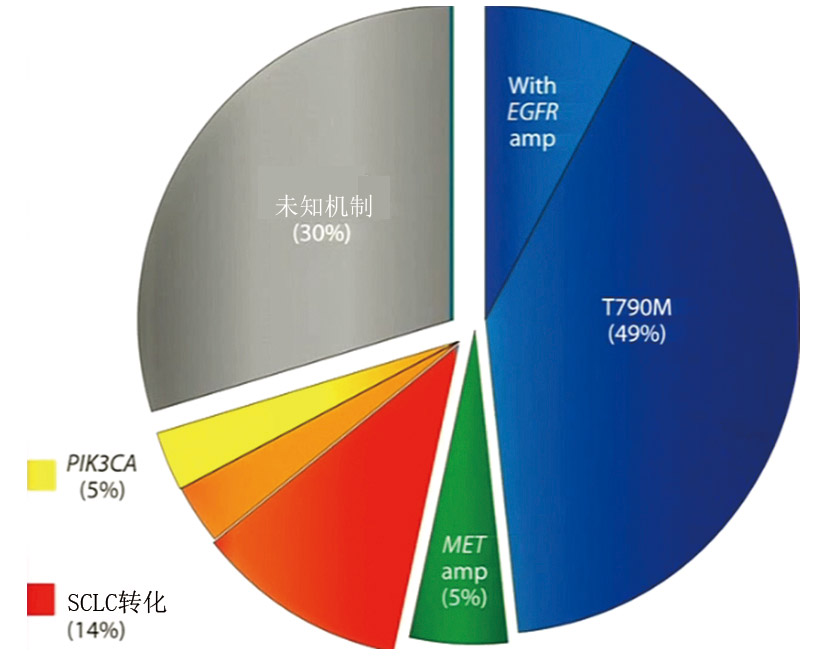
图3. 非小细胞肺癌EGFR抑制剂耐药性机制的频率
五、结 论
面对如上所述的机遇和挑战,以及面对诸如耐药性等诸多问题,精准医疗到底是不是癌症治疗的未来呢?目前精准医疗是癌症治疗的重要组成部分,但是迅猛出现的药物耐药性限制了精准医疗的治疗效果,结合靶向用药或将靶向用药与免疫疗法相结合可能是癌症治疗非常重要的途径,例如在晚期黑色素瘤的治疗中结合BRAF和MEK抑制剂就取得了不俗的效果。随着技术的向前发展,随着对生物标本和分子途径的更加详尽的分析,生物标志物和试验的不断革新,医疗器械设备和信息化水平逐步提高,以及由此带来的能对临床诊断的支持和对患者监视的改进,精准医疗会成为癌症治疗的未来。
编译:张凯
审校:王小茜




