急性冠脉综合征脂质标志物的风险评估
摘 要
本文的目的是总结急性冠脉综合征(ACS)患者常规和新型血液脂质和脂蛋白预后价值的证据。
最近研究发现的数据支持了ACS条件下的风险和非高密度脂蛋白胆固醇(Non-HDL)以及血浆神经酰胺之间存在明确关系。ACS条件下载脂蛋白B(apoB)和脂蛋白(a)[Lp(a)]的预后价值和临床可实践性尚未经过彻底检验,欧米伽-3脂肪酸的数据和氧化的低密度脂蛋白(Ox-LDL)的数据也尚未经过检验或呈现多样化。
测量基础脂质时应该将非高密度脂蛋白胆固醇(non-HDL-C)包括在内,ACS指南在叙述ACS时强制要求进行non-HDL-C的测量。血浆神经酰胺能为指导治疗决策和随访提供有用的信息。以ACS患者为目标,对apoB、Lp(a)和Ox-LDL进行额外研究是非常必要的。
简 介:评估ACS条件下的脂质
积极的风险因素调节和治疗改进(药理学改进和干预改进)能显著降低ACS相关的住院死亡率。美国心脏病学会/美国心脏协会(ACC/AHA)建议(I类)在确认ACS的24小时内快速获取脂质情况。制定这一建议参考的研究可以追溯到上世纪50年代,该研究显示ACS发生后低密度脂蛋白胆固醇(LDL-C)可以下降20%,这一水平在其后几个月内仍会发生变化。发生这一现象部分因为脂蛋白是急性反应物;脂蛋白的浓度和脂蛋白粒子的成分在ACS期间会发生变化,这可能是脂蛋白脂肪酶导致的结果。现在冠脉事件仍然高发,治疗往往要求达到更低的LDL-C水平,这些物质的变化产生的临床影响较小。
有数据显示他汀类药物能改善ACS的管理。使用高剂量他汀的MIRACL研究采用积极的降胆固醇方法,该方法取得了一定的效果,因此医学实践中,ACS患者往往使用他汀进行治疗。因此早期脂质测量的主要价值是强化了生活方式变化与治疗测量的重要性,刺激患者的依从性以便最大化二级预防的效果。本文总结了急性冠脉综合征(ACS)患者常规和新型血液脂质和脂蛋白预后价值的证据。
非高密度脂蛋白胆固醇(non-HDL-C)
Non-HDL-C[总胆固醇减去高密度脂蛋白胆固醇]的计算已经成为指南支持的常规脂质参数达十多年之久。该测量减少了由于甘油三酯升高,LDL-C水平假性下降导致的混淆以及与较低LDL-C水平(<70mg/dL)变化性的相关问题。因此,non-HDL-C可能比LDL-C更加准确。实际上,最近的人群(n=27533)研究表明当non-HDL-C水平不一致地升高时(HR 2.92;95%CI 2.33-3.67),与LDL-C水平不一致升高相比心血管疾病的风险更高。
一项称之为普伐他汀或阿托伐他汀事后分析和心梗溶栓感染疗法评估(PROVE IT)的研究得到的证据支持在ACS确认后利用non-HDL-C的测量结果。在使用non-HDL-C对患者进行分层后,使用80mg阿托伐他汀外加40mg普伐他汀治疗non-HDL-C持续升高的患者的效果逐步显现。
认同目标导向疗法的指南建议ACS患者的LDL低于70mg/dl。包含685名ACS患者的使用罗苏伐他汀对ACS进行有限降脂治疗的试验(LUNAR)表明较低的non-HDL-C目标(低于90mg/dl)更加合适。
载脂蛋白B
载脂蛋白B(apoB)是所有导致动脉粥样硬化脂蛋白的基本结构单元。美国国家脂质协会(NLA)和欧洲心脏病学会/欧洲动脉粥样硬化学会(ESC/EAS)认可在一级和二级预防中测量apoB,因为它在测定心血管疾病风险方面比LDL-C更准确。和non-HDL-C一样,它能避免较高甘油三酯水平和极低值的变化带来的问题。但是关于apoB在ACS条件下应用的报告寥寥无几。
根据PROVE IT试验的分析报告ACS发生10天以内测量apoB对他汀疗法的潜在受益和后续风险预测作用。使用罗苏伐他汀或阿托伐他汀治疗效果(apoB/apoA-1比率)比较的试验(CENTAURUS)发现ACS确认后3个月内使用罗苏伐他汀和阿托伐他汀治疗的个体的apoB水平显著下降(~35%)。最近更多的比较罗苏伐他汀和阿托伐他汀的研究确认了这一结果,这些最近的研究是在ACS期间和随后四周内开始使用罗苏伐他汀和阿托伐他汀治疗的。
脂蛋白(a)
脂蛋白(a)[Lp(a)] 是唯一一种极端致动脉粥样硬化的脂蛋白粒子。它的结构和LDL类似,核心是含apoB的粒子,但是它共价结合到称之为载脂蛋白(a)[apo(a)]的亲水聚糖基蛋白。该粒子在1963年被首次发现。1987年apo(a)的遗传分析揭示它是和人类纤维蛋白溶酶原类似的蛋白中的一个序列。还有一个包含不同数量(3—50+)重复序列的域,称作Kringle IV域。Apo(a)大小的多样性使得Lp(a)粒子也出现广泛的多样性,因此使实验室测量面临挑战。人们认为Lp(a)的kringle重复数量较少,所以致动脉粥样硬化的效果更大。测量Lp(a)胆固醇比测量Lp(a)质量要容易的多。从遗传学角度来看,Lp(a)的表达是可以定义的。其血浆水平不受饮食、环境或最常见的药物疗法如他汀影响。目前人们对Lp(a)的生物学功能知之甚少,但是它有时却被称之为最常见的致动脉粥样硬化粒子,是最强大的独立心血管疾病遗传风险因素。最近的数据显示Lp(a)是主动脉瓣狭窄和冠心病的重要的风险因素。
烟酸和脂蛋白清血法被证明能够降低Lp(a)的水平。非随机研究已经显示Lp(a)水平较低的个体,心血管疾病的风险也较低。但是最近2项观察性研究暗示使用清血法降低Lp(a)的水平能减少心血管事件的发生。最新的降脂疗法—PCSK9也很有前景。最近的meta分析报告称该方法能平均降低26%的Lp(a)。但是需要能证明使用这些疗法能改善患者结局的研究来确认是否应该在Lp(a)水平升高的患者中推广这些疗法。
将风险Lp(a)的表达水平纳入预测评估能改善其性能,这对于处于中间风险的人群尤为重要。一些发表的研究结果也已经表明使用Lp(a)可以将个体重新分入正确的风险组。患有ACS的患者很有可能被列入高风险组并使用最积极的降脂疗法,因此对于同时出现高水平Lp(a)表达的ACS患者的管理最终可能需要更新的方法。
血浆神经酰胺
神经酰胺是所有细胞和脂蛋白表达的复杂的鞘脂类。不像其他胆固醇,神经酰胺只是在脂蛋白或荷尔蒙生化结构单元内慢慢通过。神经酰胺具有很强的生物活性,并在细胞膜完整性、细胞应激反应、炎症信号和细胞坏死中发挥核心作用。从饱和脂肪和鞘氨醇中生成神经酰胺的反应会在所有组织中发生。在血脂异常和热量超标期间,神经酰胺重新合成并在不适合脂肪储存的组织内累积(图1)。
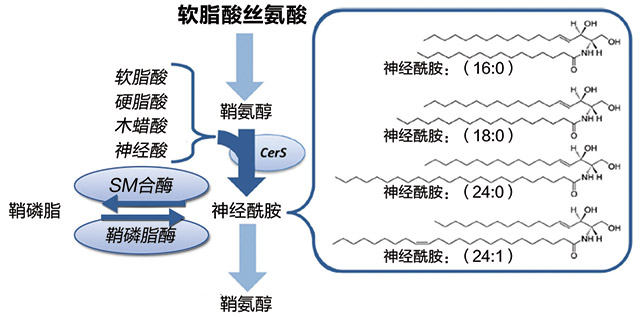
神经酰胺会在所有脂蛋白内出现,包括LDL。LDL内神经酰胺成分的增加促进渗透到血管壁。动脉斑块内的ApoB脂蛋白由于神经酰胺的作用增加了50倍。炎症细胞因子干扰素γ、肿瘤坏死因子α(TNFα)、细胞白介素-1β刺激神经酰胺合成。最终神经酰胺通过一氧化氮信号通路解偶联与血小板活化和内皮功能紊乱有关。除了在动脉粥样硬化进展中发挥作用外,升高的血清神经酰胺浓度还与多种CVD风险因素如高血压、心衰和2型糖尿病有关。因此,和脂蛋白相关磷脂酶A2(LP-PLA2)一样,神经酰胺浓度可能表明其活性以及粥样硬化斑块的易损性。
无目标代谢组学分析在血管造影术确认的冠状动脉狭窄人群中鉴别了三种与心血管死亡明显有关的神经酰胺。与心血管死亡相关的神经酰胺是棕榈酰基鞘氨醇[神经酰胺(16:0)]。硬脂酰基鞘氨醇[神经酰胺(18:0)]和神经酰基鞘氨醇[神经酰胺(24:1)]。这种相关性独立于年龄、体重指数、吸烟状况、他汀使用状况、甘油三酯、LDL和总胆固醇。神经酰胺归于十四酰鞘氨醇,会有额外的预测价值[神经酰胺(24:0)],疾病不会影响高丰度血浆神经酰胺。
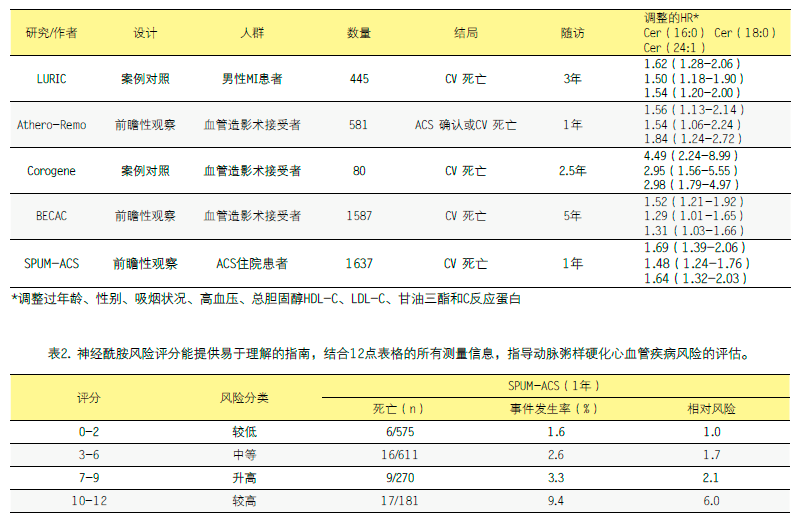
多个已经发表的研究再次确认了神经酰胺的强大预测价值(表1)。血浆神经酰胺带来的风险独立于年龄、性别、体重指数、吸烟状况和血液胆固醇等传统的风险因素。此外,在调整过其他标志物如C反应蛋白(CRP)、apoB和LP-PLA2后,神经酰胺依然具有很高的预测价值。
在一项对ACS患者进行积极护理的多中心前瞻性研究中(n=1637),测量了血浆神经酰胺的基线浓度,随访患者1年时间。随访过程中51名出现CV相关死亡事件的患者的血浆神经酰胺水平显著升高。在调整过MI、糖尿病、胆固醇、HDL-C、LDL-C和GRACE评分后,神经酰胺的预测力仍然显著。
该研究建议根据三种预测性血浆神经酰胺及其与第四神经酰胺的比值建立神经酰胺评分。每个高于中值或第三四分位数评分分别增加1到2分。因此,神经酰胺的潜在风险总结为12点表格。应用这项神经酰胺评分的两项大型观测性研究(人数超过1500名)揭示:与得分等于或低于2分的患者相比,得分在10-12分的患者死亡事件风险要高4-6倍(表2)。
神经酰胺作为预后生物标志物最有前景的方面是能指导有效的干预。基于神经酰胺测量的随机临床试验尚未得出报告。但是,一些报告已经发现通过限制高热量饮食、胃旁路手术、有氧运动和他汀疗法能显著降低神经酰胺的浓度。服用辛伐他汀的受试者的血浆神经酰胺水平显著下降。一项对代谢综合征患者的研究发现每天服用10mg罗苏伐他汀5周后,神经酰胺出现显著下降。尽管缺乏结局研究报告,但是我们已经知道这些调节血浆神经酰胺浓度的疗法在降低复发事件风险方面是有效的。
欧米伽-3脂肪酸
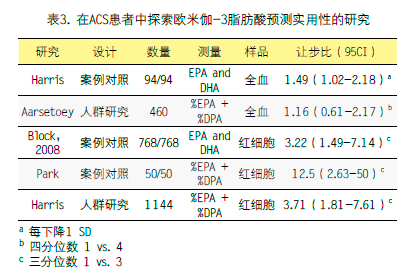
多元不饱和欧米伽-3脂肪酸尤其是二十五碳五烯酸9(EPA)和二十二碳六烯酸(DHA)具有保护心脏的作用。一些测量ACS患者EPA和DHA的研究已经发表,但结果呈现多样化(表3)。一项对ACS患者(n=460)进行研究并随访2年的试验表明EPA和DHA(全血内测量)显示出低浓度EPA、DHA和CV死亡率之间存在一种相关性,但是不显著。TRIUMPH注册中的一项更大的研究(n=1536)发现EPA和DHA(红细胞膜内测量)显著加强GRACE评分对2年死亡率的预测力。
由于缺乏标准方法,存在于血浆和红细胞膜内的EPA和DHA在作为生物标志物使用时其潜在的性能出现混淆。实际上,一项研究报告的一份血样内测量EPA和DHA结果会随着其向不同的实验室发送而不同,结果间的差异高达4倍。McConnell及其同事发现单一的3.6g剂量的EPA+DHA(等同于一份三文鱼)可以在6小时内使血浆EPA和DHA浓度增加50%,并在24小时内持续升高。但是在相同时间段内分离的红细胞内测量的EPA和DNA与基线水平不会有很大不同。这些数据确认了先前红细胞欧米伽-3水平在生物学上表达EPA和DHA可能更准确的结论。
研究EPA和DHA补充效果的随机临床试验普遍得出积极的结论,尽管一些研究的结果在关于不同产品间EPA和DHA的生物可利用性上存在差异。ACC/AHA和NLA的指南建议日常饮食摄取EPA和DHA,补充EPA和DHA可以降低CAD的风险。目前人们的关注点包括EPA的和DHA的饮食和药物来源的多样化以及补充这两种物质的最合适人群。
氧化的LDL
氧化的LDL(Ox-LDL)是一种内皮功能紊乱和动脉粥样硬化不稳定型的标志物。氧化通过过氧化氢、一氧化氮(NO)、丙二醛(MDA)、4羟基壬烯醛(HNE)或多种其他活性氧传播。不饱和脂肪酸尤其易于氧化。取决于活性氧的参与,氧化可能截断不饱和脂肪酸或在不饱和脂肪酸上建立分叉。
存在LDL时,脂蛋白的多样性导致多种氧化机制混合。氧化以单一LDL为目标,包括磷脂质、胆固醇酯类、甘油三酯或多种LP-PLA2。目前,免疫分析可以测量Ox-LDL。多种方法报告的Ox-LDL取决于使用的抗体的目标。其复杂性限制了Ox-LDL作为稳定生物标志物的应用性。
尽管存在诸多局限性,ACS期间采集的样品中使用Tsimikas及其同事开发的方法,在血纤维蛋白溶酶原同系邻近位点结合到Lp(a)唯一抗体(E06)测量的Ox-LDL对不良事件具有很高的预测价值。不仅如此,治疗中的Ox-LDL所受的影响最小,表明Ox-LDL是一种不依靠他汀的生物标志物。积极降低胆固醇水平预防中风试验(SPARCL)也确认了类似结果。
结 论
脂质是多种生物标志物的集合。临床数据支持合理使用non-HDL-C、apoB、神经酰胺作为生物标志物预测ACS患者的风险并指导ACS患者的治疗。Lp(a)在一级护理环境中对处于中间风险的患者进行再分类时十分有效,这对有早期CVD家族史的患者尤为重要,但是由于缺乏证明降低Lp(a)可以改善患者结局的数据,所以限制了Lp(a)在ACS患者中的应用。数据支持红细胞欧米伽-3成分是omg-3生物可用性的高级指标。但是目前来看,需要就欧米伽-3的补充来源以及最佳的目标人群达成一致。Ox-LDL是一种具有极端多样性的生物标志物,需要基于逐个案例研究其作为生物标志物的实用性。
编译:张凯
审校:王小茜
(摘自《Curr Cardiol Rep》,版权归其所有,仅供内部参考)




