关于IgE抗体的检测质量—— 您的结果,Phadia的使命
为什么质量对过敏原检测如此重要?
测试质量指的是关于给出真实的和可重复的IgE抗体结果的综合表现。要达到这点,许多方面和因素需要考虑到,包括精密度,重现性,最低检出限,同时,整个产品体系的质量保证(Quality Assurance)也至关重要。
可靠性和临床可用性高度依赖于检测的精密度和重现性,这样即使随着时间的推移,数值也能标准化或具有可比性。这点对过敏原体外检测尤为重要,因为IgE介导的过敏没有明确的临床cut-off值,通常是依靠量化的结果,来呈现出与发生临床症状风险之间的关系。IgE水平越高,发生临床症状的风险越高,但即使IgE浓度处于较低水平,也意味着存在风险。测试分析技术高度决定了测试结果的可靠度,从而影响了患者的诊断和治疗。
Phadia ImmunoCAP方法展现出的高重复性,高再现性,高准确性使其获得了EN ISO 15189认证。 Phadia生产的大部分产品均通过CE以及FDA的认证。
半定量检测所提供的结果报告已经过时
CLSI发布的《人免疫球蛋白E(IgE)和特定特异性过敏原的分析性能特点和临床应用;批准指南-第2版》(I/LA-20-A2)中明确指出:sIgE半定量检测所给出的过敏级别的结果,已经过时,不应该再被临床继续使用。
Phadia ImmunoCAP是唯一为IgE抗体独身定制的检测技术
IgE抗体测定比大部分免疫测定更复杂,受到许多的影响因素。ImmunoCAP不仅仅是一项检测,而是一项将所有影响因素考虑在内的,专为IgE抗体测定而研发的测定系统。
● 血清中IgE浓度极低(μg/l);
● 每种过敏原包含了大量的可能会激发IgE抗体反应的蛋白质/组分;
● 对每种过敏原,测定必须足够灵敏以捕获所有IgE抗体,甚至相关组分;
● 检测系统与IgE的结合能力远远高于其它免疫球蛋白,排除竞争性结合对于检测结果的影响。
Phadia ImmunoCAP的溯源性是检测结果定量准确的基础
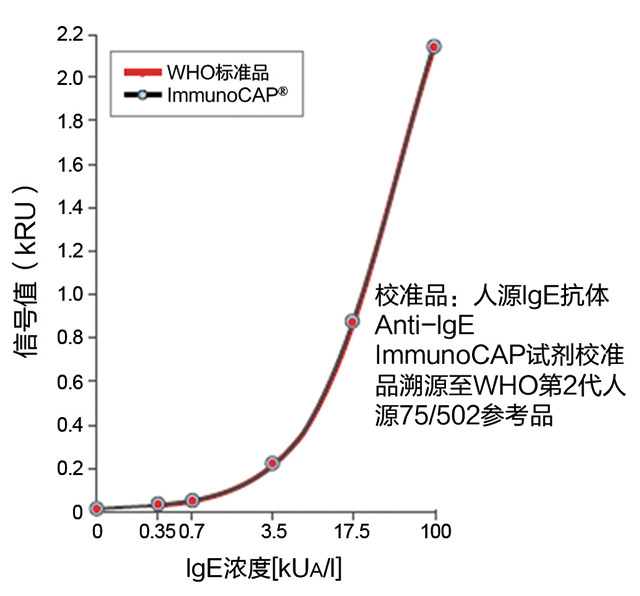
ImmunoCAP sIgE校准品与WHO标准品
校准品是否能够溯源至WHO人源IgE 75/502国际参考品是定量检测IgE抗体的前提条件,也是以kUa/l(或IU/ml)作为报告单位的先决条件。
Phadia ImmunoCAP具有极佳的线性和平行度
平行度是定量免疫分析的又一个特点,也是一个条件。校准品和样本血清产生平行的剂量-信号的曲线。系列稀释样本是检查定量分析表现的一个简单方法。
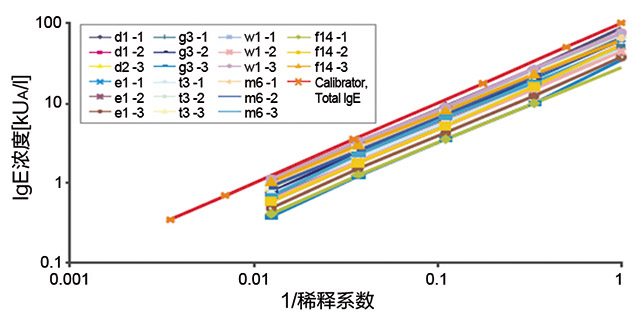
Phadia检测21份血清中7种过敏原,样本按梯度稀释多次检测。测量结果与校准品相比,都显示出极佳的线性和平行度。
Phadia ImmunoCAP:25年检测结果始终如一
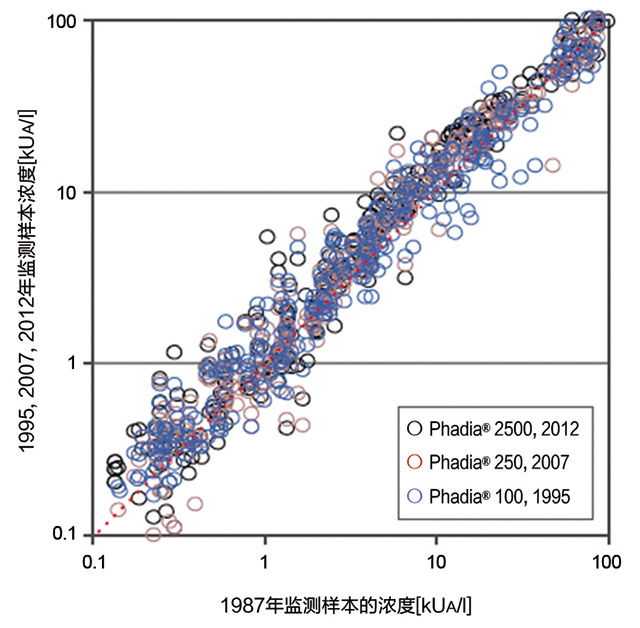
75份样本存放在-20℃,在4个不同年份不同检测平台上,进行11个过敏原的检测,所得结果基本保持一致,品种包括:d1,d2,e1,e3,e5,g3,g6,m2,m3,t3,t6
Phadia ImmunoCAP被检验、临床和学术界一致公认为IgE检测“金标准”
● 超过70个国家的3000余家实验室使用Phadia ImmunoCAP,承担全球70%以上的过敏原体外检测;
● 唯一在国际指南中(CLSI、EAACI、NIH/NIAID)被推荐的检测技术;
● 全球超过4000篇学术文献采信Phadia ImmunoCAP的过敏原检测数据。
质量是检测的生命。IgE检测结果的质量是我们的先决使命。在Phadia总部,瑞典乌普萨拉,不同岗位的员工分工合作,控制生产流程的每一个环节,确保您得到我们承诺的质量标准的产品。
■赛默飞世尔科技(中国)有限公司 供稿




