分子诊断之生物感测芯片
>> 生物芯片历史
1950年代,随着美国生物学家沃森(James Watson)与英国生物物理学家克里克(Francis Crick)发现了DNA的双股螺旋结构,解开了基因之谜,至此开始了生物科技上的大跃进。1980年代后期,生物芯片开始蓬勃发展,其一次可在短时间内分析大量数据的特性,加上与半导体、生化、微机电、医学与化学等技术配合,在硅芯片或玻璃表面固定上生物分子(DNA、蛋白质等),使原本必须在一整间实验室进行的实验,能够缩小到一个小小的芯片即可执行,其最大的优点在能微小化并且快速大量地处理样品>的同时大幅减少样本和实验耗材的使用。2000年代随着人类基因组计划(Human Genome Project,HGP)的完成而掀起另一波跨世纪的生技热潮,过去探讨基因表型只能一次检测单个或少数几个基因,若要研究多个蛋白质需要耗费大量的人力资源与时间,但自从生物芯片的发明以及逐步改进的技术,同时检测数万个基因或蛋白质如今已不是难题,生物芯片也成为了蛋白质组学或基因组学研究的一项主流工具。
目前应用生物芯片研究的领域相当广阔,例如:探讨基因表型、新基因的发现、癌症检测、新药开发、单一核苷酸多型性(Single nucleotide polymorphism,SNP)等。以癌症检测为例子,对于生物学家来说,一直是一个复杂且需要解决的课题。癌症的发生原因并不是单一因素而是多重迭加而成,虽然已经找到了抑癌基因以及致癌基因,但根据目前研究癌症还牵涉到许多基因之间的交互作用,必须同时观察多个基因之间的相关性,生物芯片因具有同时可观测数万个基因的能力而成为研究癌症课题的一个利器。
根据生物芯片的发展历史,从1980年代至今已有各式各样的生物芯片可使用,根据其特性可分成三种类型:
(一)实验室芯片(Lab-on-a-chip):此为透过微电机和电子技术,将微流体和微反应整合于一块芯片上,让复杂的实验流程例如样品处理、反应与检测分析得以在一个微小的芯片上执行(如图1)。操作上将数个微升甚至纳升的液体样品通入微形管道之实验室芯片中,并控制液体样品在设计好的微型化环境中,进行一连串与一般实验室相同的操作工作如分离、纯化、培养等实验步骤。目前主流实验室芯片为聚合酶连锁反应芯片(Polymerase Chain Reaction,PCR chip)、毛细管电泳芯片(Capillary electrophoresis chip)等。

图1. PCR芯片
(二)纳米线场效晶体管(Nanowire FET):随着微电子和半导体技术迅速发展,近年来将纳米线晶体管开发为生物芯片的研究与应用如雨后春笋般浮现,例如利用FET之特性作为癌症早期诊断的工具。举例来说,恶性肿瘤的晚期治疗相当困难,但若能早期发现则治愈率可大幅上升,因此若能利用FET早期检测出血液中的癌细胞或是肿瘤标志(Tumor marker),对临床上癌症医疗会有很大的帮助。在FET表面固定上欲辨认的生物标记(Biomarker)的抗体,当样品中出现目标抗原后并成功被抗体捕捉后,FET会因为阻抗的改变造成电流与电压的变化,根据此原理便可检测到样品中是否有欲检测之抗原(如图2)。相较于传统免疫标定,纳米线场效晶体管检测目标分子的固有和交互电特性,并可以在样品量极低之情况下实现检测,同时检测速度快并可与电路整合,所收集到的讯号可实时上传云端并进行实时数据分析,为近年发展前景看好之技术。
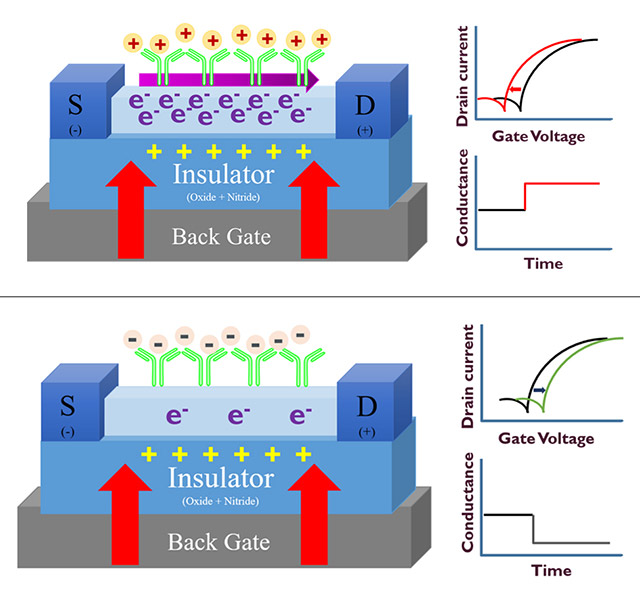
图2. 纳米线场效晶体管工作原理
(三)基因芯片(Gene-Chip,DNA microarray):是一块带有DNA微数组(microarray)的特殊玻璃片或硅晶圆片,在数平方公分的面积上放置数千或数万个核酸探针,利用核酸互补原理与样本中的DNA、cDNA、mRNA、lncRNA、miRNA等目标核酸片段杂交结合,藉由荧光或电流方式检测,可实现高通量检测。例如可为目标基因设计一系列不同的探针(Probe),并利用互补原理精确辨认对应的基因片段,得知样本中各基因表达情形。近二十年发展中,基因芯片可说是五花八门并各有长处,常见的应用为DNA微数组(如图3)、microRNA微数组、SNP芯片等。经由一次测试,可提供庞大的基因相关信息,已成为基因组学和遗传学研究的基层工具。Microarray 最大的优势是能在单次实验中,同时观察上万种核酸之间的相对量变,但也因为平行处理之故,无法对个别探针做优化,所以大部份的结果都还有赖Northern blot或Real-time quantitative PCR再做确认。虽然Northern blot在过去扮演过非常称职的角色,但microarray筛选出来的基因,往往是上千个之多,以传统方法来验证,确实是耗费人力物力。Real-time quantitative PCR近年开始普及,优势在其高灵敏度与快速,但对上千个标的,光是PCR primer的投入(包括许多primer的序列,都有专利保护),及因专一性需求而加入的probe等所需的大量寡核酸之合成,是不容小觑的。

图3. Illumina 微数组芯片
>> From Chemical FET to Biological FET
从1970年代开发出离子选择性场效晶体管(Ion-Sensitive FET,ISFET),当时可用来测量溶液中的离子浓度,当离子浓度(例如pH值)改变,通过晶体管的电流将相应的改变。随后又进一步研发出金属氧化物半导体场效晶体管(Metal-Oxide-Semiconductor FET,MOSFET),藉由环境中氢离子浓度的改变,场效应晶体管的绝缘层与溶液(或气体)的界面形成双电层。这种双电层所产生的电场能够引起半导体表面导电性的变化,此现象可用于检测化学物质的量。使用场效化学晶体管能开发出检测气体、离子、分子、水分等化学成分的传感器,可用于火灾警报、湿度感测等用途,典型的化学传感器为pH计,感测组件为作用电极与参考电极的电解液,测量溶液的氢离子与各电解液产生之电动势。
Biological FET为基于ISFET之工作原理,不同的是在其表面引入生物识别层,因此对选择的生物分子或化学分析物敏感,成为具有对生物讯号有感测能力的微型生物传感器,在其感测层固定生物材料,例如核酸、抗体、酵素等等,通过结合目标生物分子造成表面离子改变,引起阻值变化造成电流改变实现生物传感器之功能(如图4)(M Kaisti,2017)。举例来说,使用硅烷(Silane)或EDC-NHS耦合等方法将DNA探针共价修饰到FET表面,并利用核酸序列互补之原理抓取样本中目标核酸,读出电流变化量并量化数据。目前经典的已开发生物传感器为血糖仪,原理为利用测量血液中的葡萄糖与试纸中的葡萄糖脱氢酶反应产生的电流量测量血糖。
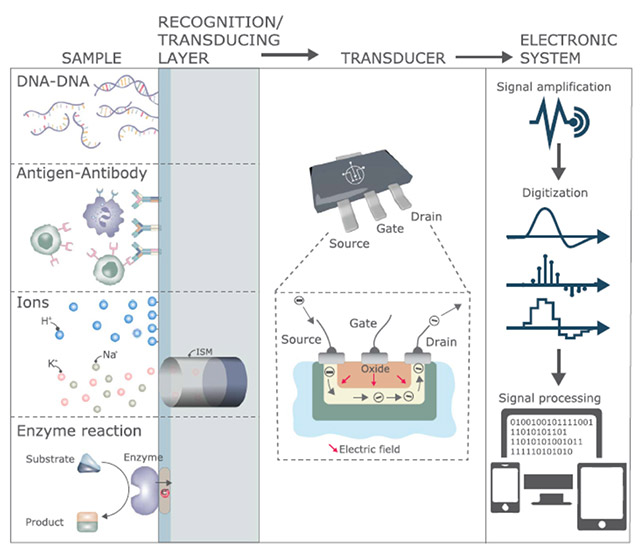
图4. 化学FET传感器与生物FET传感器工作程序
近年纳米线场效晶体管(Nanowire field effect transistor)为生物传感器开发之趋势,建立于传统FET感应电荷变化的基础上,在纳米级的尺寸之下,许多新的应用与优势开始浮现。例如纳米线体积微小,其高表面积/体积比例,使其灵敏度可符合生物感测之需求,并能根据不同需求以化学或物理方法将需要的生物分子(核酸、抗体等)修饰至纳米在线实现感测。
>> Detection of Macromolecules
高分子化合物(核酸、蛋白质等)的检测可分为间接性与直接性检测,例如酶标记就是一种间接性的检测(图4 Enzyme reaction),利用物理性或化学性的方法将酶固定在晶体管闸极上,样本中的受质若出现则会被酶催化,产生的电荷变化引发晶体管电导变化而产生讯号。第一种在ISFET运用此概念的研究是将青霉素酶固定在晶体管上,当样本中存在青霉素时,酵素催化青霉素水解成青霉酸,过程中释放的氢离子将会改变闸极附近的pH值,这种变化将可以被FET检测到,实现青霉素的检测。
无标记检测(Label-free detection)为近年检测器发展的开发趋势,此类无须多余标记步骤的检测方法,可大幅减少样本前置准备时间以及减少因多余步骤带来的误差值。寡核苷酸(Oligonucleotide)是比蛋白质小得多的生物分子,是一类只有20个以下碱基的短链核苷酸,德拜筛选效应(Debye screening effect)不会对其检测产生强烈影响,因此可将此短链核苷酸直接修饰FET表面作为探针。DNA-FET是将特异性的探针通过静电吸附或共价修饰固定在晶体管闸极,互补的标的与探针高特异性的杂交(Hybridization)后带负电的DNA骨架引发闸极附近的电位发生变化,进而达到感测目的。近年来更开发出nDNA探针(Neutralized DNA,图5),由于nDNA没有如DNA或RNA上的磷酸基团,因此nDNA与DNA之间缺乏电性相斥的现象,使两者之间的结合强度大于DNA与DNA,能够增强讯号,同时可以在较低的盐浓度之下两股杂交(Hu,2018)。在单核苷酸多型性(SNP)检测方法中,双股探针是一种新的方法,其中一股固定于表面并有另一股较弱的互补股杂交,从表面末端开始,数个碱基保留为单股状态,当样本中有完美互补股时,较弱的互补股将被替换下来,而非完美互补情况下,例如具有单核苷酸多型性的单股,将不会发生替换情形。
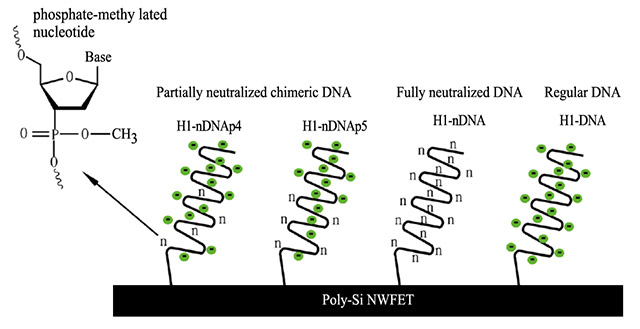
图5. 中性DNA(Neutralized DNA,nDNA)作为探针应用于硅纳米线场效晶体管
与核酸的检测类似,抗体-抗原间的直接无标记检测也引起了研究者极大的兴趣,蛋白质除了在特定的pH之下净电荷为零,其他情况下通常为带电分子,根据FET感测原理,当样本中出现抗原时会与作为探针的抗体形成复合物,并根据环境pH值呈现正电性或是负电性,改变晶体管电导产生讯号上的差异。虽然某些研究认为抗体-抗原复合物的大小远远超过FET可以侦测的范围,检测应该难以实现,不过在成功检测出抗体-抗原复合物的研究中指出能进行检测的原因为唐南效应(编者注:唐南效应指带电粒子接近半透水薄膜时影响薄膜,有时甚至影响薄膜两边性能的效应。这是由于带电粒子不通薄膜,在带电粒子的薄膜这边产生不均匀电荷和电场的缘故。),根据该理论,蛋白质被认为是电极表面上的膜,微小离子可以在溶液和这种蛋白质膜之间移动。当蛋白质被固定而形成固定电荷时,在膜和溶液之间的界面上出现离子浓度的差异,离子的重新分布在界面电位中产生可检测的变化。
>> Silicon Nano-wire Bio-Sensor的挑战
由于Nanowire FET感测平台的优异性以及具有的潜力,许多学术和营利单位致力于开发这项技术并商业化。然而,这些Nanowire FET生物感测平台仍处于研发阶段,尚未获得FDA或CE/ISO批准的常规应用。作为Nanowire FET生物传感器开发的先驱,来自哈佛大学衍生公司Vista Therapeutics,Inc(美国圣塔菲)的Charles Lieber和他的团队首次推出了用于癌症诊断与病毒和生物毒素检测的Nanowire FET生物传感器原型。该公司提供完整的解决方案,包括样品处理,处理平台,读出仪器以及数据处理,大多数活跃在该领域的公司都是大学研究小组的副产品(Tran,Duy,2018)。
尽管技术取得了重大进展,但兼容于CMOS的Nanowire FET生物传感器技术的商业化仍在早期阶段,与其他传统固态感测技术类似,仍存在重大挑战,还需要进一步改良。由于微电子和半导体制程的进步,Nanowire FET的大型图案化和跟CMOS整合不再是问题,但制造成本的规模经济化以及大量制造后须确保每个组件的一致性仍是一大挑战。另一个重大挑战则是测量典范(Measurement paradigm),针对低离子浓度溶液中的带电目标生物分子的测量,需要开发新的样品处理方法及新的测量方法,以实现快速、可靠和可重复的诊断设备,并同时需要开发出具有超低噪声以及多信道读取装置,才能符合实际的应用需求。
>> 瀚源生医技术平台
瀚源生医(Helios Bioelectronics,Inc., HBI)的目标为开发一种超灵敏半导体诊断平台,以满足精准医疗的需求,此平台可收集具有生物学意义的基因讯息以及蛋白质表达,并可实时连续监控分子间的动态变化,以利于复杂疾病的诊断。该平台快速且易于操作,具有高通量(High-throughput)、多路复用(Multiplexing)以及实时定量功能(Real-time quantitation),可将量测到之数据实时上传云端并进行AI分析。
从监测健康风险到疾病诊断,以及疾病预后和追踪,HBI提供解决方案,以满足不同阶段的未满足需求。
2016年全球精准医药市场价值435.9亿美元,预计到2026年将达到1470亿美元(BIS Research,2017)。精准医学的实施在很大程度上取决于分子诊断学和POCT的进步,预计这两者在全球IVD(体外诊断)市场中的增长速度最快(Frost&Sullivan,2013)。快速增长主要归因于慢性病和传染病、癌症、不断增长的人口老龄化和医疗设备技术的持续进步。由于其广泛的应用以及来自新兴市场与成熟的欧洲、美洲市场之需求,分子诊断和实时检验(POCT)的市场预计将快速增长(Frost&Sullivan,2013)。POCT是全球IVD终端用户市场排名中为第二大,预计将成为全球IVD技术市场增长最快的一环。
HBI正致力于开发硅场效晶体管生物感测技术平台,该平台具有许多优势,可满足科学/临床研究,精准医疗和POCT市场的未满足需求。其特点为:
1. 可移植性高:HBI设备原型的当前尺寸为30×19×3公分,可容纳四个FET生物传感器盒(如图6所示)。 每个闸盒包含一个FET生物传感器芯片,尺寸为9×3.5×0.4公分。

图6. HBI硅场效晶体管生物传感器原型机
2. 快速且易于操作:HBI的无标记(Label-free)和无须放大技术(Amplification-free)显著减少了生物检测所需的时间和精力。无标记意味着可节省大量样品制备时间; 另一方面,无须放大不仅简化了繁琐的测定程序,而且大大缩短了培养时间(Incubation time)。这项优势有助于增加终端用户市场,不仅是从实验室到POCT甚至是患者在家自行测试。
3. 高通量和多路复用:HBI硅场效晶体管生物传感器采用不同的专有设计,目前每个芯片包含多达128×128个感测组件,总共等于16000个检测点。值得注意的是,这个数字还可以再进一步提升,因此,每个芯片可以同时检测超过1M的生物标记物,这对基因/遗传表达分析非常有利。
过去十多年有很多的研发团队投入以nanowire FET为基础的bio sensor chip研发与创新,更有很多以此为技术基础进行创业。分析这些团队可以发现大部份都是以生物或医学的观点进行研发nanowire FET sensor chip的有效性及可行性,但nanowire FET bio chip要能够进入量产(Mass production)必需先要有一个可以稳定生产的半导体制程,并以制程下开发出可信的量测方法与量测环境。
HBI利用亚洲丰富的半导体资源,并邀请半导体原厂投入资金与技术,共同开发生物感测芯片,引用他们过去在制程制造上累积的经验,透过HBI对生物感测芯片特定需求的解读,转化出可以稳定生产、精准监控与快速回馈的制程方法;除了监控组件制程外,也考虑后续生物固定化与量测的需求,打造不同的sensor与其对应的量测模式,要能全程掌控制造上的所有环节,达到bio sensor quality的一致性与稳定性。
>> 结 论
生物芯片从早期的基础开发开始,至今已有各式各样用途及特色之产品,而在后基因体时代,生物芯片提供了一个高效率且方便的实验技术平台,已被广泛应用在各类的生医研究上,包含基因调控机制的研究,如单核苷酸多型性芯片(SNP array)、甲基化芯片(Methylation microarray)、微型核糖核酸芯片(microRNA microarray)等等不同主题的研究,蛋白质芯片也紧随在后成为热门的研究重点。这些芯片帮助研究者快速的对生物体的基因体变化有更全面的认识,面对复杂且未知的疾病时能锁定特定的目标基因,更可能找出未知的关键基因。举例来说,癌症因其多变不稳定的特性,且受到多重基因控制而非单一基因,若使用传统方法一次测定单个基因不仅效率不佳且容易失败,但若使用生物芯片一次可产出的数据跟传统实验相较之下可能高出几千几万倍,可以一次性得到完整的癌症组织基因表现量之变化,作为后续治疗与评估用。
在癌症领域里,日趋普遍的伴随式疗法(Companion therapeutics),就是结合伴随式诊断(Companion diagnostics)与治疗,随着精准医疗的发展逐渐明确,也将带动诊断试剂、生物芯片、体外诊断医疗器材相关市场的发展。精准医疗需要的便是高功能的检测配套,以及大数据的方式处理基因图谱的平台,生物芯片可实时针对生物体内数以千计的核酸包含DNA、miRNA、lncRNA、以及microbiota 等,进行表现量分析与动态的观察,并提供这些数据间彼此相关性比较。未来可结合生物信息市场的发展,利用网络与信息科技,云端技术的进步,提供医学研究,药物开发者重要的开发工具。
参考文献
1. Kaisti, Matti. "Detection principles of biological and chemical FET sensors." Biosensors and Bioelectronics 98 (2017): 437-448.
2. Hu, Wen-Pin, et al. "Synergetic improvements of sensitivity and specificity of nanowire field effect transistor gene chip by designing neutralized DNA as probe." Scientific reports 8.1 (2018).
3. Tran, Duy, et al. "CMOS-Compatible Silicon Nanowire Field-Effect Transistor Biosensor: Technology Development toward Commercialization." Materials 11.5 (2018): 785.
4. Frost & Sullivan, Analysis of the Global In Vitro Diagnostics Market.




