B·R·A·H·M·S PCT产品 检测病人样品检测结果的溯源性
降钙素原(Procalcitonin)在了解病人有无细菌感染和败血症等问题上,具有非常特殊的价值。目前,国内为了减少抗生素的使用,更加关注诸如降钙素原(PCT)检测的项目。为此,国内许多厂商纷纷自行开发或引进这个检测试剂。
很多厂商声明,他们的降钙素原产品与国际知名B·R·A·H·M·S的降钙素原,在检测病人样品上相关性良好。而且,检测结果也具有溯源性。可惜,很多体外诊断产品厂商与临床实验室人员,对如何理解溯源性上概念很模糊。而且,不少临床实验室对降钙素原的基础内容也不甚清楚。
一、什么是降钙素原
降钙素(calcitonin)是正常人体组织的一个激素,调节体内钙的浓度。正常情况下,它在甲状旁腺的滤泡C细胞内合成,初始形式为降钙素原前体(分子量为17000,Preprocalcitonin),为146个氨基酸的多肽,是CALCI基因产物。降钙素原前体经剪切掉N端信号肽后,成为降钙素原(Procalnitonin);降钙素原再切掉N-端侧肽后,形成的降钙素即包裹于分泌颗粒中。再剪切下C端侧肽,成为下钙素。成熟的降钙素分子(32个氨基酸,分子量为3400)和下钙素(21个氨基酸)是共同等摩尔分泌的。
在正常代谢情况下,活性降钙素在甲状腺C细胞表达分泌,降钙素原蛋白在细胞内水解产生。由于PCT以正常的代谢速度被水解,健康人体PCT通常小于0.1μg/L。在细菌、真菌、寄生虫和败血症引起严重感染下,血液中整分子的PCT浓度可能超过500μg/L。在全身性炎症反应时,有迹象表明多种器官如肝脏的巨噬细胞和单核细胞参与PCT的合成和释放。在体内,PCT分析非常稳定,半衰期为22~29h(平均24h)。 体内降钙素原的来源和代谢可参见下图。

图1. 降钙素原的代谢
二、降钙素原的临床应用
降钙素原是一个116个氨基酸的多肽,它是调节体内钙浓度激素的前体。尽管近期对降钙素原的兴趣集中于它作为细菌感染标志物的价值,这个多肽最初用于癌症的血清标志物。1970年代,多个研究者注意到在神经内分泌肿瘤患者的血清中,成熟激素降钙素在循环中水平升高。这个升高也发现于甲状腺髓样癌、良性肿瘤和肺部的小细胞癌患者。降钙素接着被用于随访患者接受治疗效果的血清标志物。很快,发现降钙素的前体,包括降钙素原在神经内分泌肿瘤的患者中也升高,可等同地被作为癌症的血清标志物。
1990年代,注意到具有严重全身性炎症患者血清降钙素原浓度的升高,包括烧伤中吸入性伤害、肺吸入、胰腺炎
和中暑等。1993年,Assicot和同道报告了严重细菌感染儿童血液中降钙素原的高浓度。在这个里程碑的预期研究中,从79例疑似感染的住院儿童中确定了降钙素原的价值。86%病毒性感染的儿童,他们的降钙素原依然保持较低的水平(0.1~1.5μg/L),在细菌感染儿童中降钙素原为6~53μg/L。
另外,降钙素原与疾病严重性和接受抗生素治疗快速下降相关。在这个标志性的报告后,降钙素原很快被认可为成年人和儿童二者细菌感染的有价值标志物。
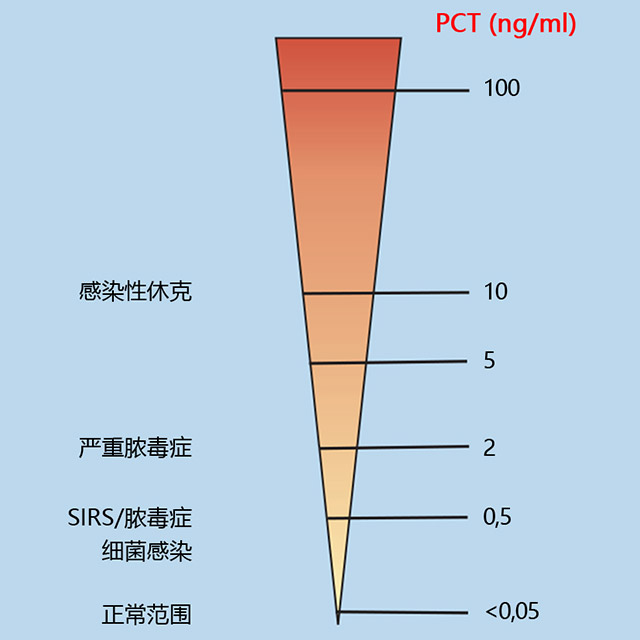
图2. 临床上降钙素原对感染疾病的使用。PCT(μg/L=ng/mL)

图3. PCT用于诊断“全身炎症反应综合征”(SIRS)、无脓毒症、全身炎症反应综合征、炎症脓毒症及感染性休克的表现。
FDA列举的PCT结果判读原则:“PCT>2μg/L(ng/ml):ICU入院第一天的值达到这个水平的,提示病人发展为重症脓毒症或感染性休克的风险很高。”“PCT<0.5μg/L(ng/ml):不能排除感染的可能,因为局部的感染(没有全身性炎症反应)同样可以达到这个水平。若在疾病早期进行PCT检测的(如在起病6小时之内),则结果也可能仍然处于较低水平。”
三、ISO 17511规定了5种计量上可溯源链的上端
1、测量结果可以在计量上可溯源至SI的被测量。有可用的一级参考测量程序和一个或多个(经认证的)一级参考物质(作为校准品)。达到这样水平的有约25~30个类型的量,具有良好确定的组分,如:一些电解质、代谢物、甾体激素及一些甲状腺激素等。
2、测量结果不能在计量上可追溯至SI的量。
1)有可用的国际约定的参考测量程序(不能被称为一级参考测量程序)和一种或多种用此参考检测测量定值的国际约定校准物质。符合这些条件的量的组分,象HbA1C(糖化血红蛋白)。
2)有可用的国际约定参考测量程序,但是没有国际约定校准物质。符合这些条件的约有30种类型组分的量,如:凝血因子。
3)有可用的一个或多个国际约定校准物质(用作校准品)及赋值方案,但是没有国际约定参考程序。符合这些条件的约有300多种量,如:使用世界卫生组织(WHO)国际标准的量,像蛋白激素、某些抗体和肿瘤标志物等。
4)既无参考测量程序,也无校准的参考物质可用。制造商自行建立“自用”测量程序和校准品,为产品校准品定值。符合这些条件的约有300种组分的量,如肿瘤标志物和抗体等。
上述这些内容来自2003年ISO 17511文件。
3、至今国际上还没有公认的降钙素原参考物质或参考测量程序(方法),制备厂商只能自行建立“自用”的检测程序和一级校准品,为公司的产品校准品定值。BRAHMS公司对降钙素原的校准做法,正是ISO 17511导则规定了溯源链上端中的最后一个做法。
最重要的是,B·R·A·H·M·S公司为了确保公司不同时代、不同系列的降钙素原的产品,对相同患者样品的检测结果一致,建立了自己的“金标准”参考物质和校准程序,由此形成了公司自己的经典溯源体系,很具有特点。
四、B·R·A·H·M·S PCT LIA校准品对于参考物质的溯源性
1、B·R·A·H·M·S标准物质的发展
B·R·A·H·M·S公司开始形成第一代降钙素原产品时,公司人工合成了第一个自己的降钙素原的参考物质PTN47。该物质由47个氨基酸组成。确定某一批的PTN47为准,成为公司的降钙素原的最高级校准品。并将另一批的PTN47作为公司产品校准品,以最高级校准品为准,通过病人标本比对,确定产品校准品与某批号检测产品组合下的校准值。与公司该批号产品一起销售给临床实验室。
在使用PTN47为参考标准时,公司考虑到它仅是完整分子的一个多肽。所以,在配制标准液时,按照多肽与完整分子的比率多称了PTN47,期望给予纠正多肽不长的补偿。当时,将PTN-47形成的校准体系,称为“Urstandard PTN-47”,意即“金标准PTN-47”。
但是,PTN47仅为47个氨基酸的多肽,在参与免疫检测反应中检测信号较微弱。为此,以后公司又合成了一个第二个降钙素原的115个氨基酸多肽,称为PCT115参考物质。
由于PCT115参与免疫反应的能力增强,与PTN47校准的检测产品间的结果有很大的差异。为了确保公司任何一代产品对相同病人样品检测降钙素原结果的一致,也与以往PTN47校准的产品对病人检测结果的一致,公司均以PTN47校准的B·R·A·H·M·S PCT LIA为准。
为了确保所有各代产品以后对病人样品检测结果的一致。首先必须完成由PTN-47与B·R·A·H·M·S PCT LIA产品的组合,和PCT115与B·R·A·H·M·S PCT LIA产品的组合间,在对病人样品检测结果一致下,校正PCT115的“标准”值。也即PCT115不可以自身在免疫检测中具有的实际检测值为准,它必须被调整到确保病人检测结果在这两组系统中的一致,以PTN-47与B·R·A·H·M·S PCT LIA产品的组合为准的值。
2、完成PTN47与PCT115交换
实际检测显示的一组标准稀释液(即免疫检测中为形成校准曲线需要的系列标准),在PTN47与PCT115间,在相同的B·R·A·H·M·S PCT LIA产品下的结果比较呈曲线表现。因此,不可应用PTN47所有系列稀释液阅读点的直接校准。
为确保临床检测结果的一致性,使用Urstandard-PTN47与B·R·A·H·M·S PCT LIA产品2h版本校准的,以标准样品S3(2μg/L)为准。依据S3单点结果,计算出Urstandard-PCT115范围其他标准的系列稀释液的临床显示浓度。以后,公司可以Urstandard-PCT115为准,与B·R·A·H·M·S PCT LIA产品2h版本组合,由PTN47 S3为准校正的PCT115,经系列PCT115稀释液去形成在PCT LIA下的校准曲线,对病人样品进行检测。这些病人样品再次在PTN47与B·R·A·H·M·S PCT LIA组合的比较下,证实与PCT115和B·R·A·H·M·S PCT LIA组合的结果比较,符合公司认可的一致性。这样,完成了PTN47与PCT115在B·R·A·H·M·S PCT LIA产品中得到了病人结果一致性的转换。
使用Passing Bablok回归分析PTN47与PCT115在B·R·A·H·M·S PCT LIA产品结合的两个方法比较,确定偏移。该方法允许在X和Y变量下得到检测误差,它没有假设检测误差呈正态分布,Passing Bablok对于离群点处理非常稳健。使用Passing-Bablok分析显示了,对347例相关血清检测时,与LUMItest PCT 2h-版本在完整的检测范围内具有良好的相关(y=1.01+0.05)。
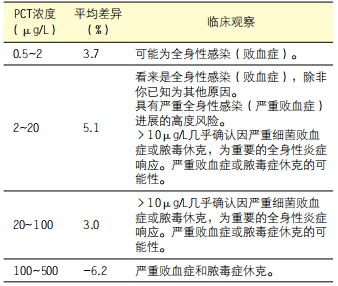
在不同浓度范围的有关相关,观察到相关线为非线性表现(斜率下降和在X上的截距上升)。这是因PCT115的较高免疫反应性,被使用S3的单点校准所致。直至100μg/L PCT浓度,平均偏离在检测范围(0~500μg/L)之内,符合临床要求。在使用PCT115校准与使用PTN47校准比较时,如果PCT浓度大于100μg/L,观察到患者结果偏低(平均约6%)。(见表1)。
表1. 使用PCT115代替PTN47校准引入平均差异
3、校准等级和溯源性流程图
(见图4)
五、确定标准浓度的控制范围
1、公司内部一级校准品的监视
为了监视公司内部一级校准品的稳定性,要求有一个约两年的老标准范围系列样品(血清)与相应0血清。这些组分必须被储存于≤-15℃。每两年对公司内部一级校准品检查一次,必须对在≤-15℃下储存的10个标准范围样品进行检测。
该检测做法按下面第2点实施。
2、检测标准浓度的校准
1) 检测操作
至少在两天内至少进行10批间检测,使用以市售的0血清复溶(配置)的检测样品,同时检测内部一级校准品和0-血清的组合和独立的(与试剂盒无关)的控制血清。所有样品在荧光光度计上检测。可以使用相应的市售组合。
2)按以下顺序进行双份检测:
(1)公司内部一级校准品(标准和控制品)、以0-血清复溶的样品;
(2)至少有4个独立的控制血清(天然混合血清),浓度必须覆盖完整标准范围。
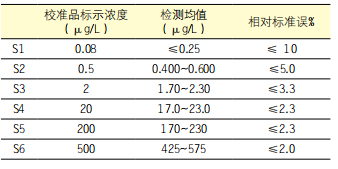
3)监视检测PCT-浓度的要求见表2。
表2. 检测中检测PCT浓度
六、概要和结论
B·R·A·H·M·S PCT LIA的校准历史覆盖了厂商的检测程序、厂商的校准品、厂商的一般检测程序和厂商的产品校准品。校准品依从了ISO 17511的要求。
校准品实际是可溯源的,通过校准品的不间断链,到参考物质PCT115、PTN47标准曲线(2h-版本)的标准样品3(S3)(2μg/L)。
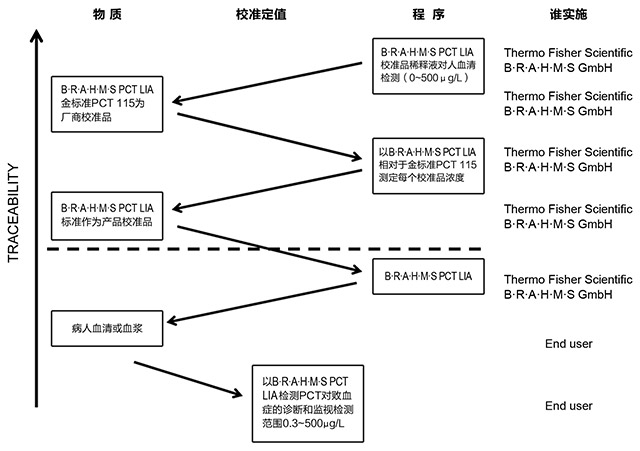
图4. B·R·A·H·M·S PCT LIA检测校准品溯源性等级。
这是B·R·A·H·M·S的PCT产品校准“溯源示意”。
1)图中的右上第一个方块是,以PTN47为准,与B·R·A·H·M·S PCT LIA产品结合,检测了一组病人血清样品,确定了这些
血清的PCT检测结果。
2)图中左侧的第一个方块是,将PCT115与对B·R·A·H·M·S PCT LIA产品结合,以上述这批病人样品的检测结果进行校
准,使这个组合检测得到的这组病人样品检测结果,与上述的这组病人样品在PTN47与B·R·A·H·M·S PCT LIA组合检测结果一致。实际上是通过方法学比较,调整了PCT115与B·R·A·H·M·S PCT LIA组合中,PCT115应表达的值。这样确立了PCT115成为公司的内部的一级校准品地位。(由于B·R·A·H·M·S提供的资料中,没有特别注明所有图示中的PCT115的区别。因此,需要说明的是,图左侧的最上那个方块内的PCT115,是公司指定了某批PCT115,作为公司的内部一级(master)标准。图示称为厂商校准品。也即被以后称为的公司的PCT115金标准。)
3)按照溯源程序,现在到了右侧的第二块方块。方块中“以B·R·A·H·M·S PCT LIA相对于金标准PCT115(意即被调整了标
示值的PCT115)的组合,去测定每个校准品的浓度。”这段话说明了,以后不论哪个产品型号,它们使用的校准品的“显示”浓度值,都必须在B·R·A·H·M·S PCT LIA与金标准组合下,与任何B·R·A·H·M·S PCT产品型号和产品校准品组合,通过病人标本比对中,去调整产品校准品的值,使之达到两组系统对病人样品检测结果最佳一致。由此确定该校准品在某个B·R·A·H·M·S PCT产品型号某个批号的组合下的定值。形成了左侧第二块内的产品校准品。(同样需要指出的是,这里说的产品校准品,是公司使用的另一批的PCT115。)
4)图中右侧向下的第三个方块,是公司的B·R·A·H·M·S PCT LIA的产品,它与左侧第二个方块内的产品校准品一起,提供
给终点用户,即临床实验室。临床实验室对病人血清或血浆进行检测,得到样品的PCT检测结果。然后,该检测结果提供给中间最下方,意即为临床诊断和治疗提供PCT信息。




