IVD国际动态

西门子、贝克曼、BD等公司于3月份获得FDA批准的产品
根据美国食品和药品监督管理局(US FDA)的网站显示,在3月期间,西门子、贝克曼、BD、雅培等公司的体外诊断检测获得了批准。
西门子(Siemens Healthineers)的Dimension Vista高敏肌钙蛋白I检测,获批使用本公司的Dimension Vista系统测定血浆中的心肌肌钙蛋白I。FDA表示该检测可用于诊断急性心肌梗死。去年6月,西门子的高敏肌钙蛋白I检测被FDA批准使用本公司的Atellica IM和Advia Centaur XP/XPT免疫分析仪进行心肌梗死的早期诊断。

在Dimension Vista系统上进行高敏肌钙蛋白I检测
贝克曼(Beckman Coulter)的三个产品获得了510(k)批准。第一个产品是DxH 520血液分析仪,这款分析仪是为小容量的实验室设计的,包括诊断和医生办公室。该分析仪于去年4月获得了CE认证。

DxH 520血液分析仪
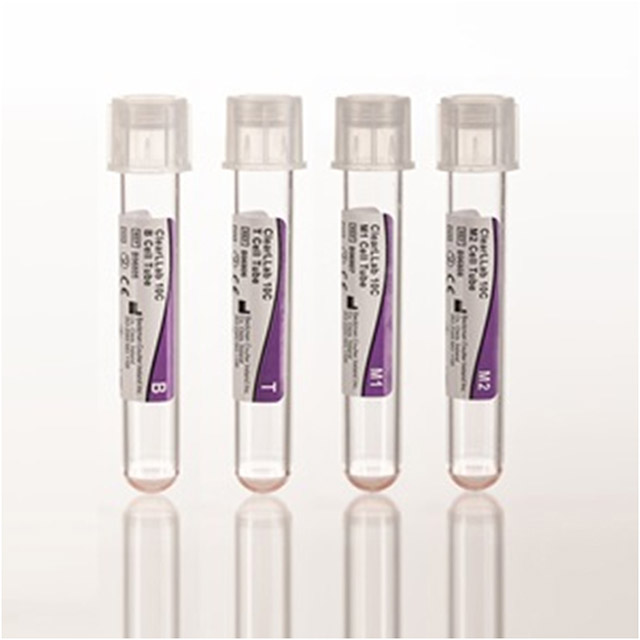
第二个产品是ClearLLab 10C Panels,通过多参数免疫表型鉴别细胞群,在贝克曼的Navios和Navios EX流式细胞分析仪上运行。此Panels包含的试剂用于鉴别诊断患有或疑似患有以下造血组织肿瘤的患者:慢性白血病、急性白血病、非霍奇金淋巴瘤、骨髓瘤、骨髓增生异常综合征和/或骨髓增生性肿瘤。
第三个产品是应用了早期脓毒症指标的UniCel DxH 800 Coulter细胞分析系统。早期脓毒症指标预期用于,因脓毒症症状到急诊科就诊且临床医生为其申请了白细胞分类检测的成年患者。
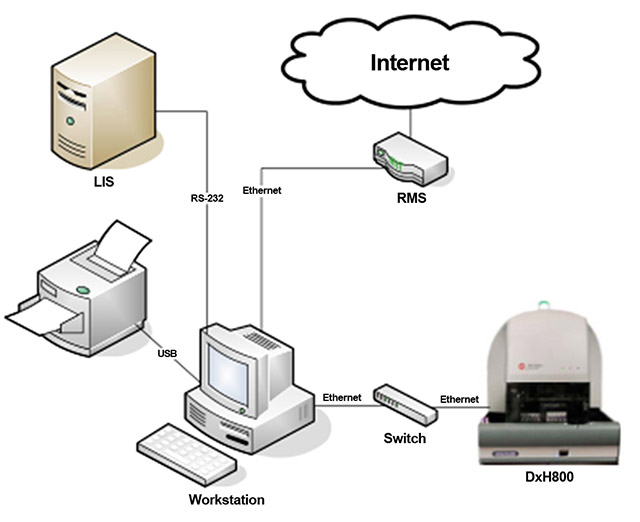
DxH 800系统配置
BD(Becton Dickinson)的BD Vacutainer Eclipse UltraFill采血针获得了FDA批准。该一次性医疗器械包含一个防护罩,在采血完成后立即启动盖住采血针,避免意外被采血针刺伤。
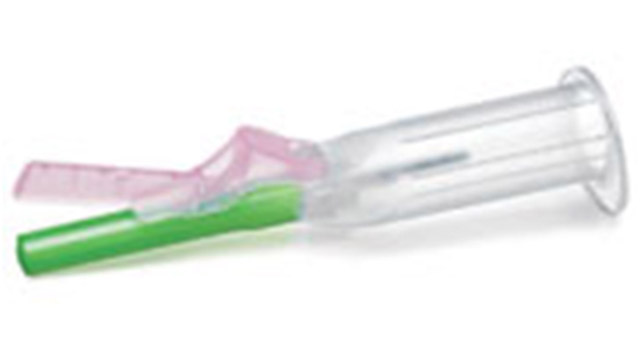
BD Vacutainer Eclipse UltraFill 采血针
雅培(Abbott)旗下Alere的ID Now Influenza A & B 2检测,获批在其ID Now仪器上运行。该快速分子诊断检测利用等温核酸扩增,对具有呼吸道感染体征和症状的患者进行甲流和乙流病毒RNA检测和鉴别。
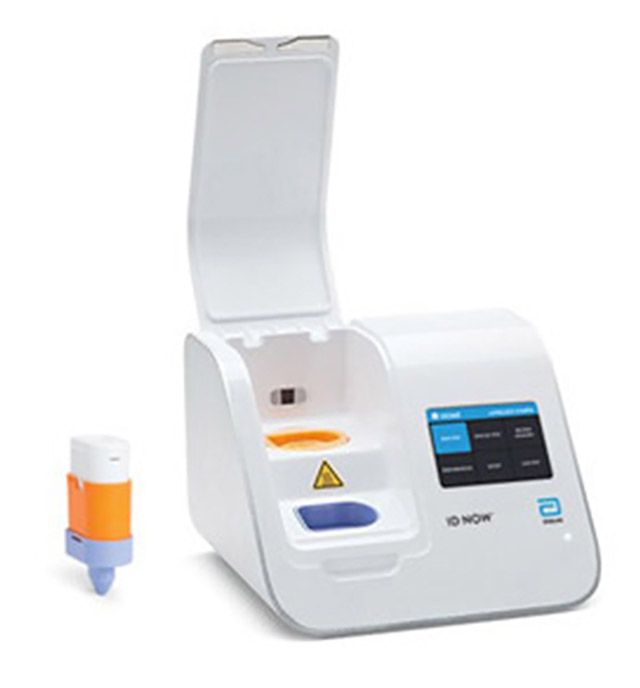
在ID Now仪器上运行ID Now Influenza A & B 2检测
BioMérieux的Vitek 2 AST-Gram Negative Delafloxacin检测获得了510(k)批准,在本公司的Vitek 2和Vitek 2全自动微生物鉴定及药敏分析系统上运行,用于革兰氏阴性杆菌的药敏检测。根据FDA对德拉沙星(Delafloxacin/Baxdela)的标注,该抗菌剂对大肠杆菌、阴沟肠杆菌、肺炎杆菌和绿脓杆菌的大多数菌株具有抗菌活性。

Vitek 2 AST鉴定卡
FDA批准了杭州奥泰生物技术股份有限公司的一种快速色谱免疫测定,即Single and Multi-Drug Rapid Test Cup With Adulteration(Urine),用于检测尿液中的单药和多药及药物代谢物。FDA表示该检测提供了初步的分析检测结果。

奥泰生物的单药快速检测
赛默飞(Thermo Fisher Scientific)旗下Phadia的EliA Celikey IgG、EliA GliadinDP IgA和EliA GliadinDP IgG免疫测定获得了FDA批准。EliA Celikey IgG免疫测定,用于检测血清和EDTA血浆中组织型转谷氨酰胺酶的IgG抗体,在Phadia 2500和Phadia 5000平台上运行。EliA GliadinDP IgA和EliA GliadinDP IgG两项免疫测定,用于检测人血清或血浆中的醇溶蛋白抗体,以诊断乳糜泻。
另外,GenePOC公司用于检测A群链球菌的一项快速分子检测获得了批准。Hitachi Chemical Diagnostics的Optigen AP 3600大容量过敏检测系统获得了批准。
罗氏(Roche)的Ventana PD-L1(SP142)Assay获批作为伴随诊断,用于鉴别哪种三阴性乳腺癌患者的肿瘤浸润免疫细胞上的PD-L1表达升高,并更可能有益于Tecentriq(atezolizumab)免疫疗法与化疗。
FDA批准了Aggredyne的血小板聚集检测试剂盒
Aggredyne近日宣布US FDA批准了其AggreGuide A-100 ADP Assay,该试剂盒用于测定以一种血小板受体P2Y12为靶标的抗血小板药物的效果。
Aggredyne表示,获得批准意味着可以在美国境内销售该试剂盒,并进一步扩展了可用于本公司A-100仪器的检测菜单。2013年,FDA批准了A-100仪器和配套A-100 AA检测试剂盒,用以测定阿司匹林对血小板活性的影响。
Aggredyne总部位于休斯顿,为了获得批准,在美国几个临床试验中心使用经FDA批准的双重抗血小板治疗组合,包括硫酸氢氯吡格雷(Plavix)、替格瑞洛(Brilinta)和普拉格雷(Effient)等药物,对A-100 ADP试剂盒进行了评估。
Aggredyne表示,ADP试剂盒在微流体反应室内模拟全血流动,类似于人体内的血液流动。配套A-100仪器利用激光散射来快速量化样品中的血小板聚集情况。单次测试仅需几滴全血。
Aggredyne的CEO和总裁Robert Hux表示,获得批准后,公司可以为美国的医院、诊断实验室或经正式认证的任何单位提供完整的血小板检测技术组合。目前他们正在获取必要的法规分类,以便直接在医生办公室放置血小板检测设备。

AggreGuide A-100仪器
伯乐的两款产品获得FDA批准
近日,伯乐(Bio-Rad Laboratories)的两款产品获得了US FDA批准。
第一款产品是IH-500全自动、随机存取的血型定型和筛查系统。该系统是为了中小型实验室设计的,在凝胶卡技术的基础上进行全自动血型定型和筛查,用户干预程度最低。它可以处理Bio-Rad的所有IH凝胶卡,用于ABO血型定型、反定型、表型测定、Rh亚组测定、抗体筛查、抗体鉴定、单抗原检测、直接AHG检测和交叉配型。

IH-500血液学分析仪
第二款产品是莱姆病检测Lyme Total Assay。这项免疫测定利用包被了配体的磁珠检测多个靶标,在本公司的全自动和随机存取多路平台BioPlex 2200 System上运行。
根据公司网站显示,用户将一盘一级试管装载到系统上以后就可以走开。它每小时能够处理100份样品,并在约60分钟后获得第一批结果,后续样品检测每30秒即可完成。
Bio-Rad的临床诊断部总裁John Hertia表示,BioPlex 2200 Lyme Total assay扩展了BioPlex 2200 System的传染病检测菜单,使实验室能够在早期检出莱姆病,因而满足莱姆病管理中的重大医疗需求。
BioPlex 2200的检测菜单还包括自身免疫疾病和其他传染病的多重组合。去年,Bio-Rad的BioPlex 2200 25-OH Vitamin D Kit获得了FDA批准,用于评估维生素D缺乏症。
Bruker的肺结核检测、PCR平台获得CE-IVD认证
Bruker近日宣布其FluoroCycler XT PCR系统和FluoroType MTBDR 2.0 Liquid Array检测,获得了CE-IVD认证,用于检测肺结核和抗生素耐药性。
Bruker表示,基于PCR的MTBDR检测可在3小时内直接从患者样品中鉴别出病原体,无需进行培养。它还能检测60多种TB基因突变,提供多达522种抗生素耐药模式的信息,有助于指导治疗。
该检测和平台均基于Bruker购买Hain Lifescience的大部分股份而获得的PCR技术。后来形成了Bruker-Hain Diagnostics,成为公司微生物学&诊断部的业务部门。
Bruker-Hain Diagnostics的总经理David Hain表示,在创新性FluoroCycler XT平台上引入FluoroType MTBDR 2.0 Liquid Array进行肺结核深入检测后,Bruker为跨国医疗保健机构改进急性肺结核的诊断和个性化治疗提供了支持。
马德里自治大学临床微生物学科的一名医生Jaime Esteban表示,他们科室计划开始使用这项新的检测和平台。他们将尽快利用这项新的高分辨率FluoroType MTBDR 2.0检测与新开发的、高性能、光学FluoroCycler XT平台,以更高的特异性来提升诊断急性TB的能力。

FluoroCycler XT PCR系统
贝克曼推出Access PCT Assay
贝克曼(Beckman Coulter)推出了Access PCT assay,帮助医生评估危重症患者进展为严重脓毒症或脓毒性休克的风险。检测结果可在不到20分钟内获得。通过Beckman Coulter的Remison Advance中间件将降钙素原检测编程为初步或反射试验,使医生将该检测纳入他们在核心实验室分析仪上运行的常规脓毒症检查中。Access PCT assay于2019年1月底获得CE认证,可用于Access全自动免疫分析家族,包括Access 2、UniCel DxI 600和UniCel DxI 800。
贝克曼Access PCT assay
EntroGen发布肺癌RNA Panel
EntroGen发布了肺癌RNA Panel,预期用于定性检测人肺RNA中的ALK、ROS1和RET融合基因以及MET外显子14跳跃突变。
该一步法反转录酶PCR检测结合了第一链cDNA合成与后续的突变和参考基因扩增,以使手动时间减到最低并降低预扩增期间引入污染物的风险。这个三步操作流程可在不到两小时内产生结果,并在八个反应中检测到47个变种。
该Panel可与若干多通道实时PCR仪器兼容,能够检测FAM、VIC和CY5荧光探针并自带免费的数据分析软件来自动报告结果。该Panel仅供研究使用。
Progenity发布了Resura单基因遗传病产前检测、Innatal产前筛查
Progenity发布了Resura单基因遗传病产前检测,是一款可定制的、无创的单基因遗传病产前检测(NIPT)。该检测可供具有已知单基因遗传病风险的家庭使用,比如囊性纤维化、镰状细胞性贫血和泰-萨二氏病。该检测是使用微滴式数字PCR开发的,利用从母体血液样品中提取的胎儿无细胞DNA,可测定所有遗传类型的致病变体包括隐性、显性和X连锁遗传突变。
Progenity还宣布改进了其Innatal产前筛查,这是一种关于染色体非整倍体的NIPT,如今在评估所有染色体的非整倍性方面具有更高的特异性和敏感性。具体而言,这项基于测序的检测在测定21号、18号、13号、X和Y染色体的非整倍性方面得到了增强。
珀金埃尔默与Helix推出GenePrism: Actionable Insights
珀金埃尔默(PerkinElmer)与Helix推出了一项基因筛查检测,GenePrism: Actionable Insights。据说它是目前市场上"最全面的临床级别DNA测序和解析"检测。这项检测使用户能够了解自身的潜在患病风险。由Helix对用户进行DNA测序,并由在PerkinElmer Genomics通过职业验证的遗传学家,使用本公司的专有高通量软件平台——有序数据解析网络对结果进行解析。合作伙伴表示,其他商业公司只评估一个基因序列中有限数量的字母,而GenePrism:Actionable Insights评估全部59个基因,包括BRCA1/2。他们还指出,PerkinElmer Genomics拥有全球最大的已知遗传变异数据库之一,为客户提供更深入的评估。
Quidel的相关检测可在欧盟国家使用
Quidel的Sofia Quantitative Vitamin D FIA获得了CE认证,与Sofia荧光免疫分析仪配套用于定量测定血清样品中的总25-OH维生素D。该检测预期用于辅助评估维生素D缺乏症,是在Sofia分析仪上运行的第一款定量检测。
该公司的即时Sofia 2 Lyme+ FIA检测也获得了CE认证,预期与Sofia 2荧光免疫分析仪配套用于快速鉴别人血清和血浆标本中Borrelia burgdorferi、Borrelia garinii和Borrelia afzelii的IgM和IgG抗体。
Quidel还表示将重新开始生产同样经过CE认证的Quidel Triage PLGF Test,预计于2019年第一季度在美国境外上市并用于临床用途。该公司收购了Alere的Triage业务,Triage胎盘生长因子产品的所有权已转移给Quidel。
MDNA Life Sciences推出子宫内膜异位血液检测
MDNA Life Sciences推出了一款关于子宫内膜异位的血液检测。该公司表示,这是第一款关于此适应症的血液检测,且检出率高达90%。检测结果可在几天内获得,使医生能够做出早期诊断决策和治疗。这家公司位于佛罗里达州西棕榈滩,其技术基于使用线粒体DNA突变作为一系列疾病的生物标志物。该公司补充道,发表在《医学生物标志物》上的一项临床研究表明,新鉴别的生物标志物能够从血样中检测出子宫内膜异位,包括早期病变。
Roche的NGS癌症检测软件获得CE认证
Roche近日发布了Navify Mutation Profiler临床软件并且宣布其获得CE认证。
该软件为癌症的下一代测序检测提供注释、解析和临床报告。同时,Roche还发布了一款可选的临床决策支持应用Navify Therapy Matcher,帮助临床医生将临床上可采取措施的突变与治疗选择联系起来。
Roche的测序解决方案主管Neil Gunn表示,这两个产品提供了一种临床决策支持解决方案,解决NGS实验室面临的重大工作流程挑战,将大量的医学和科学数据转化为可操作的见解。
Sienna Cancer Diagnostics收购了Sevident,以开发基于外泌体的癌症检测
Sienna Cancer Diagnostics,总部位于澳大利亚墨尔本,近日宣布已与美国Sevident签订购买其NET分子捕获平台的协议。
根据协议规定,Sienna将以现金和公司股票(临时凭证)的形式购买Sevident的知识产权资产包括授权专利,以及某些实验室设备资产。Sevident将获得30万美元的现金付款和在Sienna价值100万美元的新普通股。在实现未来收入里程碑后,Sevident还有资格获得高达150万美元的额外股票或现金付款。
Sevident的NET技术能够从少量临床血样中分离和捕获分子和细胞生物标志物。该技术包含一种灵活的分子基质,被应用于磁珠上,目的在于捕获目标生物标志物。
Sevident指出研究者可利用这项技术加强和简化液体活检的样品制备,既可以用于筛查也可以用于诊断。
Sienna也认为结合目前病理学实验室的样品制备时间表和资源,这项技术将有助于开发基于外泌体的癌症检测。Sienna计划利用NET扩展其在癌症诊断领域的产品供应。Sienna基于抗体的体外诊断方法检测端粒酶反转录酶(hTERT)是否存在,这种生物标志物与标准的尿液细胞学检测联合起来有助于诊断膀胱癌。
Sienna的CEO Matthew Hoskin表示,他们的目标是利用Sienna在开发和商业化hTERT产品过程中建立的能力、知识、基础设施和市场渠道,并构建产品组合。这将创造更大的规模经济,扩大的市场机会,以及一个长期可持续增长和创造价值的平台。
Sevident的首席科学家和NET发明人Emily Stein表示,她很高兴这项独特且突破性的技术现在具有进入市场的最佳机会,对患者诊断产生积极影响,并为股东创造价值。
根据协议规定,Stein将加入Sienna引领NET技术的进一步开发和商业化。另外,Sevident的CEO Peter French也将以顾问的身份加入Sienna,以支持该公司的技术扩展计划。
Sienna先前于3月份与Inside Diagnósticos签订了独家经销协议,将其hTERT检测销售到巴西的病理学实验室中。
Theradiag与Immunodiagnostic Systems签订开发、经销协议
法国体外诊断公司Theradiag近日宣布已与Immunodiagnostic Systems达成协议,可以使用该公司的IDS-i10自动化系统。
根据协议条款,Theradiag将在IDS-i10系统上推出其Tracker生物治疗监测产品线,并补充说,它已经为基于IDS技术的Tracker检测创建了一个新的商业开发计划。Tracker检测使临床医生能够监测和优化生物治疗。
Theradiag将以其品牌商业化Tracker生物治疗监测产品线和相关试剂,从Lisa Tracker系列试剂盒开始,这些试剂盒旨在监测循环TNF-α水平、处方TNA-α抑制剂及药物中和抗体的血清水平,以帮助医生管理治疗方案。
另外,总部位于英国的Immunodiagnostics将以Theradiag品牌在这家法国公司没有业务的33个国家销售Tracker技术,包括部分欧洲国家比如德国、以及整个拉丁美洲和中东地区。
协议的财务和其他条款尚未披露。
Chembio Diagnostics与Perseus Science达成协议,推进即时脑震荡检测的开发
Chembio Diagnostics近日宣布已与Perseus Science Group达成协议,推进轻度创伤性脑损伤(TBI)或脑震荡诊断检测的开发。
根据协议条款,总部位于纽约州德福德的Chembio将从Perseus获得一笔资金,具体金额尚未披露,以满足某些里程碑为条件,推进即时脑震荡定量检测的开发(结合Perseus的脑震荡生物标志物与Chembio的DPP色谱免疫测定平台)。
Chembio表示,该协议建立在两家公司之前的协议基础之上。根据之前的协议,从技术上确定了检测 Perseus(位于康涅狄格州老莱姆)的专利生物标志物的可行性。
协议的财务和其他条款尚未披露。
Chembio指出,目前TBI的诊断方法包括神经病学检查、认知测验和影像学检查比如CT扫描、MRI和PET扫描。利用即时检测快速诊断脑震荡能够实现早期干预并减少继发损伤的概率。
DPP平台凭借一滴指尖血即可在15分钟内得出结果。
Banyan Biomarkers与雅培签订有关创伤性脑损伤标志物的协议
Banyan Biomarkers近日宣布,将其专有的创伤性脑损伤(TBI)标志物,非独家授权给雅培(Abbott)。
泛素羧基末端水解酶L1和胶质原纤维酸性蛋白,在脑损伤后不久即可在血液中检测到。Banyan公司,总部位于圣地亚哥,基于这两种标志物开发了Brain Trauma Indicator产品。该产品于2018年初获得US FDA的上市授权。
该授权建立在Banyan与Abbott之间的多年合作之上,计划将这些标志物用于基于血液的TBI评估检测。此检测为即时检测,并与核心实验室仪器配套使用。协议的具体条款尚未披露。
Abbott的诊断部医学总监Beth McQuisto表示,当医生在急诊室看到疑似脑损伤的患者时,有可用的客观检测至关重要。利用类似的新型标志物,有助于他们开发即时和核心实验室血液检测,供临床医生评估脑损伤。
奥森多医疗与中国IVD公司达成合作
近日,奥森多医疗(Ortho Clinical Diagnostics)与北京利德曼生化股份有限公司合作在中国市场推出4款检测。
4款检测分别为:胱抑素C,用于慢性肾病的早期诊断;α-羟丁酸脱氢酶,用于心脏病发作的诊断;同型半胱氨酸,用于评估冠状动脉粥样硬化、阿尔茨海默病、静脉血栓、新生儿缺陷和习惯性流产的风险因素;以及总胆汁酸,用于肝损伤的早期检测。
这些检测被批准在中国用于Ortho的Vitros 4600全自动生化分析仪和Vitros 5600全自动免疫生化分析仪。它们均是MPA检测(Microtip Partnership Assays),通过Orthos和合同战略伙伴之间的合作,已验证可用于支持Microtip的Vitros分析仪。利德曼,是一家总部位于北京的体外诊断公司,将提供预灌装的专用包装试剂,专门用于 Vitros分析仪。
这些检测尚未批准在美国使用。
Ortho的临床实验室菜单业务主管Heidi Casaletto 表示,与利德曼的合作将有助于加快提升Orthos在中国的存在,最重要的是,提供一个新的MPA试剂项目组合,有助于使医院急诊(STAT)实验室更加灵活和高效。
利德曼公司总裁张海涛表示,该合作拓展了他们在封闭系统上的产品布局,有利于提高利德曼产品在高端客户中的市场份额,同时也有利于他们在研发、生产及质量控制等方面的持续改进。
Nova Biomedical与Premier签订了多年团购协议
Nova Biomedical与Premier签订了有关重症监护血气分析仪的多年团购协议。根据协议规定,除了Nova的10-test Prime之外,Premier会员在Nova的Stat Profile Prime Plus重症监护血气分析仪和耗材方面也可以享受特殊、预先协商定价和条款。
Prime Plus采用免维护传感器技术,提供20种重症监护检测,包括BUN、肌酐、电离镁、血气、电解质、代谢物、血液学和碳氧测定。
Oncimmune签署了肺癌诊断检测在葡萄牙的经销协议
英国诊断公司Oncimmune近日宣布已与Sabartech签订在葡萄牙独家销售其肺癌检测EarlyCDT-Lung的协议。
EarlyCDT-Lung检测于2012年在美国发布,用于测定7种肿瘤相关抗原的自身抗体水平。Oncimmune表示,该检测能检测任何阶段的各种肺癌。
Sabartech目前在西班牙销售EarlyCDT-Lung检测。根据本协议条款,Sabartech将在葡萄牙销售该检测,最低销售承诺为五年内70万英镑(911,619美元)。双方还将Sabartech的西班牙经销协议从三年延长到五年,后两年的额外最低销售承诺为180万英镑。
Oncimmune的CEO Adam Hill表示,葡萄牙和西班牙是重要的欧洲市场,且Sabartech迄今为止取得了良好进展,包括通过西班牙最大的私立医院网络Quirónsalud出售EarlyCDT-Lung用于筛查。将葡萄牙纳入我们的合作范围是顺理成章的,标志着EarlyCDT-Lung的商业化又上一层楼。
2017年,Oncimmune将EarlyCDT-Lun在以色列和韩国的经销权分别授予Best Medical Opinion和Dow Biomedica/Biodiscovery。2019年3月,该公司以高达410万英镑的价格收购了Protagen Diagnostics。
Novacyt与Immunexpress延长了脓毒症检测开发的合作关系
法国诊断公司Novacyt近日表示,其分子检测部Primerdesign延长了与Immunexpress的脓毒症检测开发合同。
协议的具体条款尚未披露。
Novacyt表示双方已合作三年,Primerdesign为Immunexpress提供检测开发服务。2017年,Immunexpress(总部位于西雅图)的直接血液脓毒症检测获得了US FDA批准;2019年初,它从美国卫生与公众服务部获得了商业化其SeptiCyte从样品直接出结果的脓毒症检测合同。
Immunexpress的CEO Rolland Carlson表示,他们与Novacyt的继续合作关系有助于共同开发能够改善全球脓毒症患者的管理和临床结局的多重检测。Primerdesign快速开发检测的能力和及时获得CE认证的诊断检测业绩记录让他们印象深刻。
深感悲痛!IFCC主席Howard Morris教授去世

2019年4月18日,IFCC遗憾地宣布IFCC主席Howard Morris教授在哈萨克斯坦担任客座讲师时突然去世。IFCC对此深感悲痛!IFCC和检验医学界失去了一位伟大的科学家,许多人都钦佩和尊重他。
定向点金(DDM)向他的妻子Helen Martin夫人、家人、澳大利亚临床生物化学家协会(AACB)以及澳大利亚检验医学界专家表示诚挚的哀悼!
HHoward Morris教授生前担任国际临床化学和检验医学联合会(IFCC)主席、南澳大利亚大学药学和医学科学院医学教授、澳大利亚阿德莱德南澳病理学研究所化学病理学临床科学家,同时还是澳大利亚临床生物化学家协会(FAACB)和澳洲皇家病理学院(FFSc(RCPA))的成员
2012年至2014年期间,Morris教授曾任国际临床化学和检验医学联合会(IFCC)副主席,2003年至2008年期间,任IFCC科学部秘书。他还曾担任IFCC国际骨质疏松基金会骨转换标志物标准化联合工作组主席(2012-2017),还是IFCC全球糖尿病防治运动特别工作组(2003-2008)和国际临床联络小组(2009-2011)的成员。
Morris教授曾是澳大利亚阿德莱德南澳病理学研究所化学病理学临床科学家,为该学科提供临床建议。他在免疫分析和内分泌学临床生物化学诊断领域拥有30年的工作经验,还管理过一个重要的临床内分泌实验室。在1997-1998年期间,该实验室出具了约245,000例患者报告。Morris教授于2003年到2009年期间担任汉森研究所的主任,该研究所是澳大利亚医学和兽医科学研究所(IMVS)和皇家阿德莱德医院(RAH)的研究机构。
Morris教授领导的研究团队已经获得了超过1,000万美元的科研经费,已发表的论文、专业评论及书刊章节累计达到280篇。他的研究领域包括代谢性骨病的病理生理学,以及由澳大利亚研究理事会(Australian Research Council)与国立健康与医学研究理事会(National Health and Medical Research Council)资助的包括维生素D在内的激素影响课题。





