连续检测ST2对急性心力衰竭患者的预后价值

连续检测ST2对急性心力衰竭患者的预后价值
摘 要
背 景:有些临床研究评估了ST2与心力衰竭(HF)患者结局之间的关联。然而,关于频繁检测ST2对急性HF患者的预测价值,我们所知甚少。
目 的:本研究的目的在于描述基线ST2和重复ST2检测对急性HF患者的预后价值。
方 法:在2009年至2014年期间,荷兰的14家医院招募了496位急性HF患者,参加了TRIUMPH(关于心力衰竭患者管理的独特和新颖策略的转化倡议)临床队列研究。在1年随访期间对这些患者重复采集血样(7次)。在中心实验室检测血样中的ST2和N末端B型利钠肽前体(NT-proBNP)水平。主要终点是指全因死亡和HF再入院的复合终点。使用联合模型评估重复生物标志物检测与主要终点之间的关联。
结 果:患者的年龄中位数为74岁,其中37%为女性。随访中位数为325天(四分位间距:85-401天),188位患者(40%)到达了主要终点。基线ST2水平中位数为71ng/ml(四分位间距:46-102ng/ml)。对临床因素和NT-proBNP进行校正后,基线ST2与主要终点风险增加有关,且基线ST2水平每增加1SD(log2的自然对数)的危害比为1.30(95%置信区间:1.08-1.56;p=0.005)。考虑重复检测时,对临床因素和重复NT-proBNP检测进行校正,随访期间基线ST2水平每增加1SD(log2的自然对数)的校正危害比增加至1.85(95%置信区间:1.02-3.33;p=0.044)。此外,ST2水平在主要终点发生前几周会升高。
结 论:重复ST2检测是急性HF患者结局的强大预测因子,独立于重复NT-proBNP检测。因此,ST2在临床实践中可用于预后和治疗监测。
关键词:生物标志物、心衰、预后、重复检测、ST2
心力衰竭(简称心衰,HF)是西方国家心血管病死亡的主要原因。患者治疗和管理需要改进,因为大多数HF患者即使接受了循证治疗最后仍死亡。血清生物标志物可在弥补HF评估与不良结局发生之间的空白方面发挥重要作用,它们可能暴露出新的潜在可更改的疾病途径。
目前为止有关HF生物标志物的预后价值的大多数研究,均将随访期间的不良结局与基线单一测量联系在一起。这种方法没有探究具有高度变异性、异质性、进展性疾病比如HF的患者自身存在的生物学变异。因而,可能需要重复检测生物标志物来更准确地反映潜在病理生理过程比如机械超负荷、心脏纤维化和炎症的动态和进展特性,因此它们更适合用于预后和治疗监测。
ST2是白介素-1(IL-1)受体家族的成员,有跨膜(ST2L)和可溶性(sST2)两种形式。IL-33,一种IL-1相关蛋白,是ST2L的功能性配体。IL-33/ST2L通路保护心肌在压力超负荷下不会肥大和纤维化。可溶性ST2,也是现有试验检测的ST2形式,是IL-33诱骗受体,阻止IL-33/ST2L相互作用和心脏保护级联作用。ST2的主要来源目前尚未完全确定。很长一段时间以来,我们假设在心脏疾病中循环sST2来源于心肌,因为体外数据显示sST2是心肌细胞在生物机械超负荷情况下分泌的。相应地,血清ST2水平与血清利钠肽水平密切相关。然而,近期研究表明在人心脏疾病中,血管内皮细胞可能是sST2的主要来源,而不是人心肌细胞。
临床研究显示,在稳定性和急性HF患者中,单一ST2水平是独立于N末端B型利钠肽前体(NT-proBNP)之外的死亡风险因素。近期的荟萃分析支持使用ST2对慢性稳定性HF患者进行风险分层。此外,一些研究评估了多次检测ST2的预后价值。已知急性HF患者的ST2水平显著高于慢性HF患者,并且在治疗后数天到数周迅速下降。急性HF患者经过治疗后ST2水平不下降预示着死亡。另外,ST2水平居高不下与死亡风险增加有关。只有少数主要针对慢性收缩性HF患者的研究,评估了ST2水平变化的预后价值,其中ST2的检测间隔至少为1个月。从基线到12个月ST2水平升高与全因死亡风险显著增加有关。然而,CORONA研究(罗苏伐他汀用于心衰患者的多国对照试验)表明从基线到3个月的ST2水平变化与死亡率无关。RELAX-AHF试验(松弛素用于急性心衰治疗的功效和安全性)显示在多标志物组合中连续检测 sST2对急性HF患者具有预后价值。
考虑到HF的动态和进展特性以及ST2的病理生理学,我们假设对于因急性HF入院的患者,随访期间频繁检测ST2将为重复检测NT-proBNP提供附加预后信息。美国心脏协会/美国心脏病学会(AHA/ACC)的心衰管理指南认为,ST2可用于预后和治疗监测,但需要更多研究来支撑这个建议。因此,在TRIUMPH(关于心力衰竭患者管理的独特和新颖策略的转化倡议)临床队列研究中,对于496位因急性HF入院的患者,我们评估了在频繁检测NT-proBNP之外,频繁检测ST2与1年随访期间全因死亡和HF再入院之间的关联。
方 法
目的和研究设计。TRIUMPH是一个从实验台到床旁的转化研究项目,包含需要临床确认(clinical validation)的所有新发现生物标志物。临床确认研究是观察性、前瞻性研究,参与研究的对象为2009年9月至2013年12月因急性HF住进14家荷兰医院的患者。此队列研究的目的在于,确认成功通过TRIUMPH生物信息学和早期确认阶段的生物标志物的临床价值,以及进一步评估更成熟的HF生物标志物。特别感兴趣的是生物标志物水平随时间的变化,在HF患者随访期间对重复取样生物标志物的分析及其预后意义。此研究经过所有参与中心医学伦理委员会的批准。
患者选择。患者入选条件为年龄在18岁以上,由于已知慢性HF而失代偿或新诊断HF入院。此外,还必须满足另外3个条件:1)利钠肽水平升高至正常上限的3倍以上;2)持续收缩性或舒张性左心室功能不全;3)经过静脉注射利尿剂治疗。由于非心脏疾病、严重瓣膜功能障碍但没有持续左心室功能不全或急性ST段升高心肌梗死被发现的HF患者被排除在外。另外,已安排冠状动脉重建术、等待心脏移植、严重肾衰以致于需要透析或具有预期寿命不足1年的共存疾病的患者不能参加研究。所有研究参与者均提供了书面知情同意书。
患者管理。患者管理由主治医生按照欧洲心脏病学会指南决定。重要的是,本观察性研究获得的生物标志物数据并不用于治疗决策。
研究程序。在患者入院当天(第1天)、住院第2-4天以及出院当天分别采集一次血样。随后,在门诊随访期间重复采集血样,预计时间点为出院后第2-4周、3个月、6个月、9-12个月。基线血样为入选研究后采集的第一份血样,不超过入选后2天。每次随访均按照纽约心脏协会功能分类评估HF症状。出院时确定使用的药物,有3种:1)血管紧张素转换酶抑制剂或血管紧张素II受体拮抗剂,或者两者皆用;2)β-阻断剂,或3)利尿剂。对患者进行体检,系统检查体重、血压和心率。
血液收集。按照标准化程序,通过静脉穿刺术收集非空腹血样,并送到每个参与医院的临床生化实验室进一步处理。以1700g相对离心力离心收集的血样,然后分离肝素血浆与血清。在血样收集后2小时内,将所有等分试样储存于-80℃。
ST2测量。在可控条件下将血清样本和肝素血浆样本送至中心实验室(Future Diagnostics Solutions B.V., Wijchen,the Netherlands),批量检测ST2和NT-proBNP水平。使用定量夹心法单克隆酶联免疫吸附测定(Presage ST2 Assay,Critical Diagnostics,Inc., San Diego,California),单次测定血清中的ST2浓度。我们的结果显示试验间变异的平均变异系数为4.9%,与厂商报告的5.2%平均试验间变异系数一致。在Cobas 8000分析仪(Roche Diagnostics,Ltd., Rotkreuz, Switzerland)上使用Elecsys NT-proBNP电化学发光夹心法免疫测定,检测肝素血浆中的NT-proBNP浓度。分析员对患者特征和终点不知情。
ST2模式。执行事后分析来鉴别到达和未到达主要终点的患者的ST2模式。由两位对基线患者特征和临床结局数据不知情的研究者分别分析ST2模式。ST2模式被归为以下几类:1)“U形”模式,ST2水平最初下降后来又升高;2)“J形”模式,ST2水平最初下降且后来不再升高;3)“无法解释的”模式,ST2检测次数少于3次或3次检测ST2相隔太近;或4)“其他”模式,不同于以上ST2模式。如果意见分歧,则另行达成共识。
终点。获取自索引住院(index hospitalization,最早或报告所指的住院)后9个月到400天的生命状况和再入院信息。我们查询了民事登记,筛查了所有病历,并在随访期间询问患者相关信息。
主要终点是指全因死亡和HF再入院的复合终点。HF再入院是指在意料之外患者由于HF失代偿而再入院,至少满足以下其中2个标准:利钠肽水平升高至正常上限的3倍以上;心脏失代偿症状(罗音、水肿或中心静脉压升高);以及经过静脉注射利尿剂治疗。次要终点包括主要终点的其中任一终点和心血管死亡。成立了一个对生物标志物信息不知情的事件判定委员会,对终点进行审查和判定。
统计分析。通过目视观察柱状图和Kolmogorov-Smirnov检验,评估连续变量是否为正态分布。呈正态分布的变量用平均值±SD表示,否则用中位数和四分位间距(IQR)表示。类别变量用数量和百分比表示。ST2和NT-proBNP水平不是正态分布,因此进行了对数转换供进一步分析。
根据ST2分布的四分位对患者分类,并通过卡方检验(类别变量)、方差分析或Kruskal-Wallis检验评估这些四分位之间的基线特征差异。
我们应用Cox比例风险模型评估基线ST2水平与研究终点之间的关联。在研究终点、死亡及预计随访终点对研究对象进行检查。
生存函数log minus log图(对数累积生存函数乘以-1后再取对数)没有发现与比例风险假设的偏离。我们执行了单变量分析以粗略地估计基线ST2水平的影响(模型1),对年龄和性别进行校正(模型2),以及另外对收缩压、糖尿病、左心室射血分数(LVEF)、过去6个月内因HF住院、缺血性HF、体重指数、估计肾小球滤过率(eGFR)和基线NT-proBNP水平进行校正(模型3)。结果用生物标志物水平每增加1SD(log2的自然对数)的校正危害比(HR)表示,含95%置信区间(CI)。我们使用肾脏病饮食改良(MDRD)简化公式计算eGFR。
我们拟合了联合模型,评估随访期间估计瞬时生物标志物水平(用重复时间依赖性 [简称时依,time-dependent] 生物标志物水平计算)与指定研究终点之间的关联。联合模型是连续检测的混合效应线性回归模型与指定研究终点风险的Cox比例风险模型的组合。混合模型采用了三次样条曲线,节点设在初始住院后1周和1个月。我们对重复ST2检测执行了单变量分析(模型1)。我们将重复ST2检测和重复NT-proBNP检测合并到1联合模型中以评估其独立预后价值,并校正了年龄和性别(模型2)。我们另外校正了收缩压、糖尿病、LVEF、过去6个月内因HF住院、缺血性HF、体重指数、eGFR和出院使用药物(血管紧张素转换酶抑制剂和/或血管紧张素II受体拮抗剂,β-阻断剂,利尿剂)(模型3)。我们还检验了ST2曲线本身的斜率在添加到模型3中以后是否为独立的预测因子。我们执行了诊断学和灵敏度分析以评估联合模型。最终结果用任何时间点生物标志物水平每增加1SD(log2的自然对数)的校正HR表示,含95%CI。93%患者的协变量数据是完整的,除了LVEF,只有78%患者的数据是完整的。单一估计被认为是协变量值缺失的原因。
使用Statistical Package for Social Sciences软件版本21.0(SPSS,IBM Corp., Armonk,New York)进行描述性数据分析。使用R统计软件(版本2.15.0,R Foundation,Vienna,Austria)对纵向生物标志物数据和研究终点进行高级统计分析。所有统计检验均为双边的,且p值<0.05具有统计学意义。
结 果
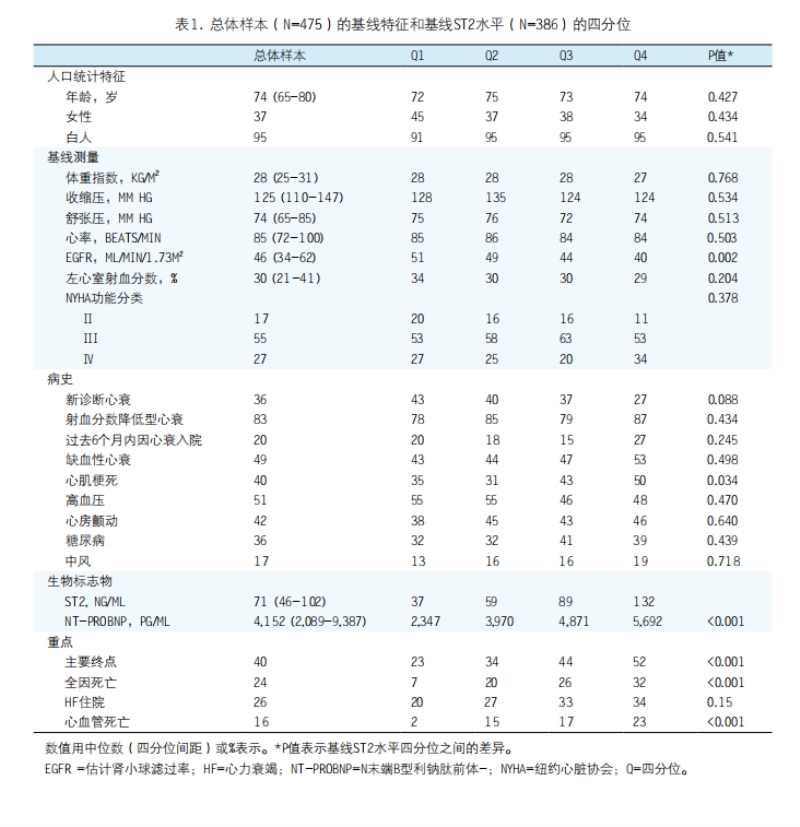
患者。共496位患者参与了TRIUMPH临床队列研究。其中3位患者撤销了知情同意书。18位患者由于不符合入选标准退出了统计分析。超声心动图显示这些患者没有持续收缩性或舒张性左心室功能不全的迹象。因此,475位患者组成了分析数据集。他们的年龄中位数为74岁(IQR:65-80岁),37%为女性(表1)。收缩压中位数是125mm Hg(IQR:110-147mm Hg),LVEF中位数是30%(IQR:21%-42%)。大多数患者为射血分数降低型HF(83%)。基线ST2水平中位数为71ng/ml(IQR:46-102ng/ml),NT-proBNP水平中位数为4,152pg/ml(IQR:2,089-9,387pg/ml)。另外,表1显示了位于不同ST2四分位的患者的基线特征。位于更高ST2四分位的患者,其肾脏功能更差且其中更多患者具有心梗历史。
基线ST2水平和研究终点发生率。随访中位数为325天(IQR:85-401天),188位患者(40%)到达了全因死亡(n=113)或HF再入院(n=123)的主要终点。这与每100患者年55.9%的主要终点发生率相符。386位患者有基线ST2水平。在最高基线ST2四分位中,50位患者(52%)到达了主要终点,而在最低基线ST2四分位中,22位患者(23%)到达了主要终点。最高四分位中患者的全因死亡率也高于最低四分位中的患者:分别为31(32%)和7(7%)。这与心血管死亡率相似:分别为22(23%)和2(2%)(表1)。
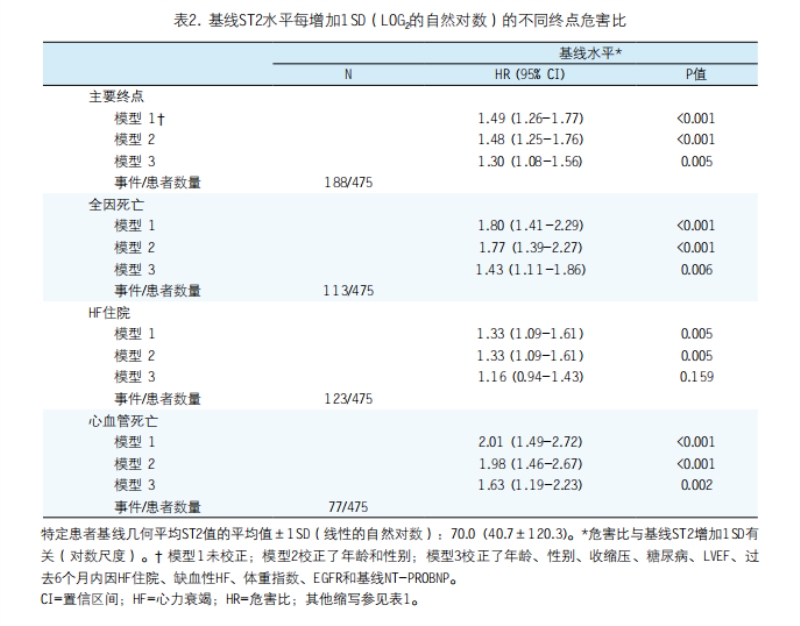
基线ST2水平与所有预定研究终点的风险增加有关(表2)。其与主要终点、全因死亡和心血管死亡的关联,在对所有选定潜在混杂因素包括基线NT-proBNP水平校正后(模型3),仍具有统计学显著性。
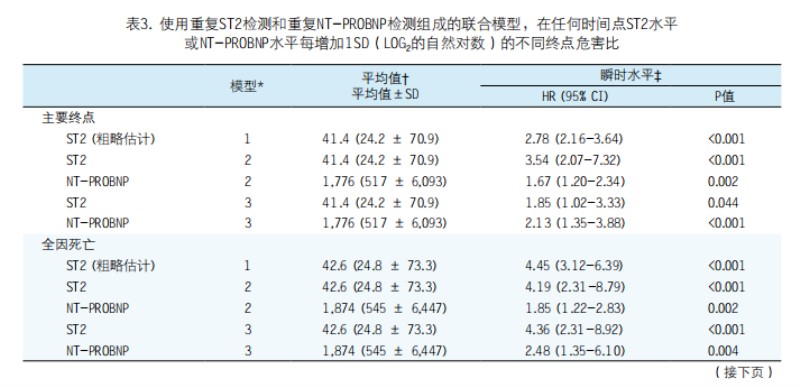
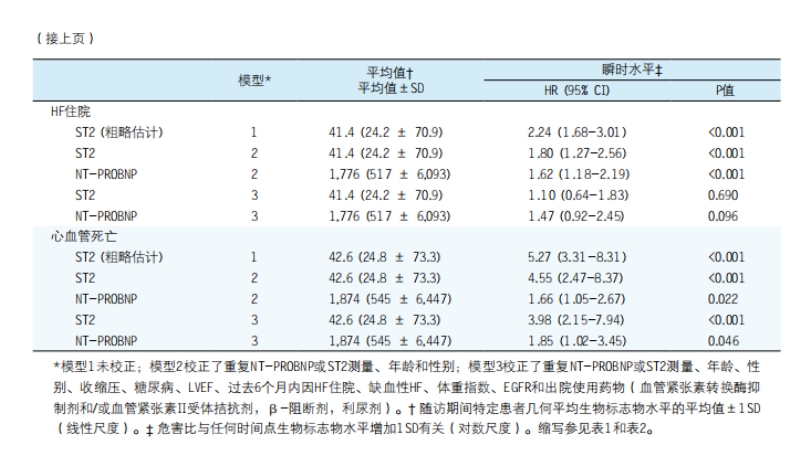
重复ST2检测的预后价值。随访期间每位患者的平均ST2检测次数为3.9,平均NT-proBNP检测次数为4.1。对重复NT-proBNP检测、年龄和性别校正后(模型2),随访期间ST2水平每增加1SD(log2的自然对数)的主要终点HR为3.54(95% CI:2.07-7.32;p<0.001)。对更广泛潜在混杂因素包括重复NT-proBNP检测校正后(模型3),此关联仍具有统计学显著性,随访期间ST2水平每增加1SD(log2的自然对数)的主要终点HR为1.85(95% CI:1.02-3.33;p0.044)。对模型3和重复ST2检测校正后,随访期间NT-proBNP水平每增加1SD(log2的自然对数)的主要终点HR为2.13(95% CI:1.35-3.88;p<0.001)(表3)。对所有协变量和重复检测NT-proBN校正后(模型3),随访期间ST2水平每增加1SD(log2的自然对数)的全因死亡和心血管死亡HR具有高度统计学显著性:分别为(95% CI:2.31-8.92;p<0.001)和3.98(95% CI:2.15-7.94;p<0.001)。ST2曲线本身的斜率不是主要终点的独立预测因子。
图1表示具有U形模式的3位个体以及具有J形模式的3位个体的测定ST2水平。在到达主要终点的患者中,56%患者在终点事件发生之前具有U形ST2模式,如图1患者I、II和III所示。图1患者IV、V和VI是具有J形ST2模式的示例,他们没有到达主要终点。在随访期间出现J形ST2模式时,82%患者没有发生任何事件。
图2和图3表示对模型3校正后到达和未到达主要终点的患者的平均估计生物标志物水平及个别生物标志物测量。初始住院期间,对所有患者进行失代偿性HF治疗时,平均估计ST2水平下降(图2A)。初始住院之后,到达主要终点的患者的平均估计ST2水平高于没有到达主要终点的患者。此外,在主要终点发生之前几周,平均估计ST2水平升高(图3)。初始住院之后平均估计NT-proBNP模式的形状可与平均估计ST2模式的形状相比较(图2B)。
讨 论
本研究清楚地表明基线ST2水平,尤其是重复ST2检测,是因急性HF入院的患者在1年随访期间全因死亡或HF再入院复合终点的强大和独立预测因子。研究结果支持以下概念:虽然NT-proBNP仍是HF的金标准生物标志物,但连续检测ST2对于(连续检测)NT-proBNP具有巨大的增量预后价值。
TRIUMPH研究的目的在于鉴别和确认能够改善HF预后的新型生物标志物。TRIUMPH是一个转化研究项目,结合了新型生物标志物的生物学发现、技术进步和在急性HF患者中进行临床确认。在此临床确认研究中,在1年随访期间利用独特的重复测量设计,评估生物标志物的预后性能。TRIUMPH研究发现ST2是一个很可能改善HF预后的生物标志物。
已确定ST2水平可用于急性失代偿性HF患者的预后预测。基线ST2水平与所有预定研究终点显著相关的研究结果证实了这点。与以前的研究发现一样,对所有潜在混杂因素和基线NT-proBNP校正后,基线ST2水平与HF再入院之间的关联不如基线ST2与死亡终点之间的关联强。
重复ST2检测与主要终点及其单独终点强烈相关。重复ST2水平与主要终点之间的关联具有高度显著性,且远强于基线ST2水平与主要终点之间的关联。重复测量考虑到了ST2水平随着时间的动态和连续变化,这可能更好地反映个体HF患者的潜在病理生理学过程的真实变化。本研究利用重复ST2检测估计瞬时ST2水平(也就是随访期间任何时间点的估计ST2水平)。这些估计瞬时ST2水平与预定终点的发生率高度相关,很可能是因为估计ST2水平接近真实ST2水平并因此反映了在随访当时患者的真实心脏状况。这点很重要,因为HF是一个动态并且通常是一个进展性的疾病,其炎症、心脏纤维化和重构都是持续的过程,单个时间点的一次生物标志物评估无法捕获全部信息。
本研究的另一个发现是,平均估计ST2水平在患者到达主要终点之前就升高了,而随访期间没有到达主要终点的患者的平均估计ST2水平是稳定的。ST2曲线本身的斜率并没有为估计瞬时ST2水平提供重要的附加预后信息。对于此发现的解释可能是,生物标志物测量的分布不是评估瞬时斜率的最佳方法。为了阐明这些发现,我们执行了事后分析来确定个体患者的ST2模式。分析证明与没有事件发生的患者相比,几乎有两倍于在随访期间到达主要终点的患者具有所谓的U形ST2模式。此外,在具有J形ST2模式的患者中,82%在1年随访期间没有事件发生。虽然我们知道ST2模式的分类可能受主观性影响,且根据事后分析下结论应谨慎,但这些发现表明ST2水平的变化的确对于HF患者评估很重要。ST2水平升高或稳定在日常实践中可能是一个有用变量,不仅可用于对患者进行高危和低危分层,甚至可以根据门诊随访期间ST2水平升高对患者的预期心脏恶化采取措施。
另一个重要发现是重复ST2检测提供了不同于重复NT-proBNP检测所提供的独立预后信息。NT-proBNP和ST2水平反映不同的HF潜在病理生理学过程,可能是该发现的最重要原因。NT-proBNP是容量超负荷的标志物。ST2也反映机械超负荷,但也是心脏纤维化、炎症和重构的标志物。通过这种方式,ST2和NT-proBNP提供关于病理生理学状态的互补信息,以及与预后评估相关的信息。因此,本研究的结果表明不仅重复ST2检测可用于HF预后,而且其与重复NT-proBNP检测可联合用于HF预后。
本研究将重复ST2和NT-proBNP检测联合用于急性HF患者,因此为AHA/ACCHF管理指南中的声明提供了重要证据:除了NT-proBNP,ST2也可用于预后和治疗监测。
未来研究应评估重复ST2检测用于指导治疗决策的价值。可以假设ST2水平高或不利(不断升高)的患者应进行强化治疗。另外,重复ST2检测可有助于鉴别更可能受益于某些治疗的患者。其他研究还应该确定最佳预后和治疗监测所需的ST2测量次数。每位患者应测量ST2水平的频率可能不完全相同,这取决于患者的临床情况、给予的治疗、ST2水平、随访期间ST2水平的进展。基于这些因素,可以绘制个体生存曲线,用于计划下一次ST2检测。由于在稳定性HF患者中ST2与NT-proBNP相比生物学变异性明显更低,大家认为ST2可能是监测HF患者的更好生物标志物。
研究局限性。虽然本研究是一项大型、多中心、前瞻性、观察性研究,但研究群体似乎不能完全代表普通HF人群。本研究群体的平均年龄为74岁,且女性代表不足。此外,只有17%入选的HF患者具有保留射血分数(preserved ejection fraction,EF>50%)。未来研究需要调查含更多女性对象、不同年龄范围且具有保留射血分数的HF患者群体是否得出相似结果。
结 论
TRIUMPH清楚地表明重复ST2检测是因急性HF入院患者发生不良结局的强大和独立预后因子。与单一基线ST2水平相比,重复ST2检测鉴别出具有明显更高不良事件风险的患者。另外,重复ST2检测具有其他已知风险因素尤其是NT-proBNP所提供信息以外的增量预后价值。这些结果表明除了NT-proBNP测量,重复ST2检测在临床实践中有助于鉴别不良结局风险增加的HF患者。
本文重点
医学知识点。因HF住院后1年内,血液白介素受体ST2水平持续升高或居高不下与不良临床结局相关,包括因失代偿性HF再入院和全因死亡。重复ST2检测可提供不同于NT-proBNP所提供的附加预后信息。
转化前景。未来研究应评估连续检测ST2水平在慢性HF患者的长期管理中对于指导特定治疗干预的作用。
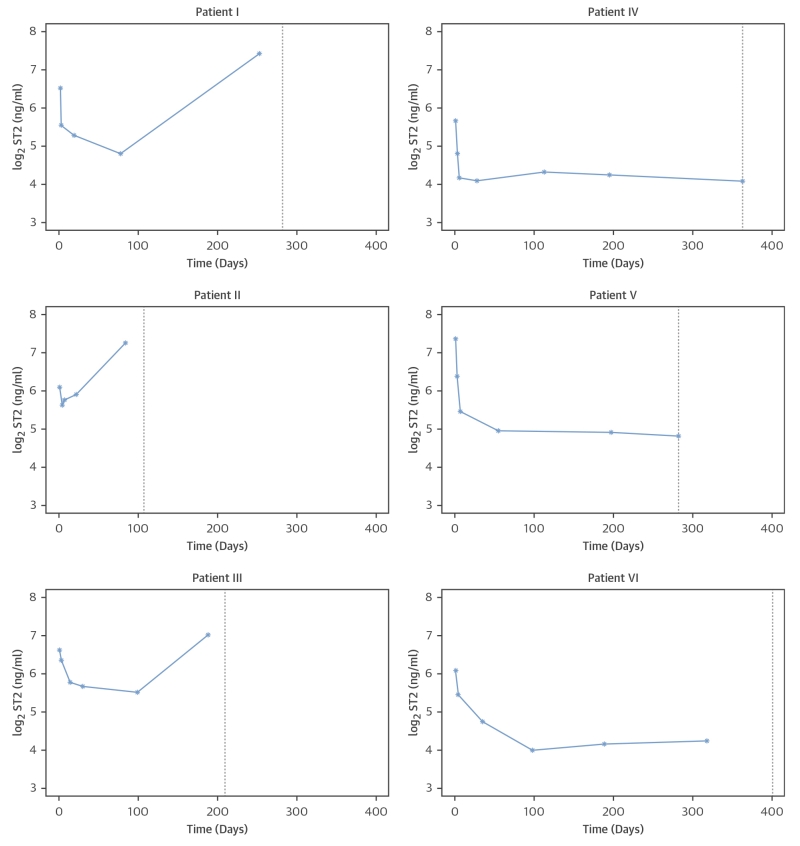
图1. 随访期间不同患者的ST2模式示例。
随访期间6位患者的ST2水平变化。垂直虚线代表主要终点或预计随访终点的发生时间。患者I、II和III显示U形ST2模式并到达主要终点。患者IV、V和VI显示J形ST2模式,且在随访期间没有事件发生。
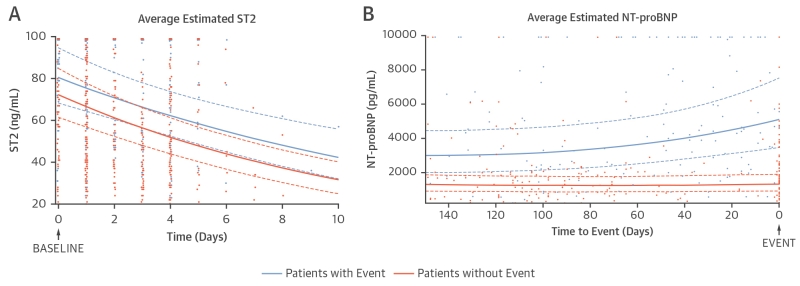
图2. 随访期间到达和未到达主要终点的患者的平均估计生物标志物模式,结合个别生物标志物测量。
(A)初始住院期间到达和未到达主要终点的失代偿性心衰患者的平均估计ST2模式。(B)在主要终点发生之前或随访结束时到达和未到达主要终点的患者的平均估计NT-proBNP模式。平均估计ST2和NT-proBNP水平经过年龄、性别、收缩压、糖尿病、LVEF、过去6个月内因HF住院、缺血性HF、体重指数、eGFR和出院使用药物(血管紧张素转换酶抑制剂和/或血管紧张素II受体拮抗剂,β-阻断剂,利尿剂)校正(模型3)。
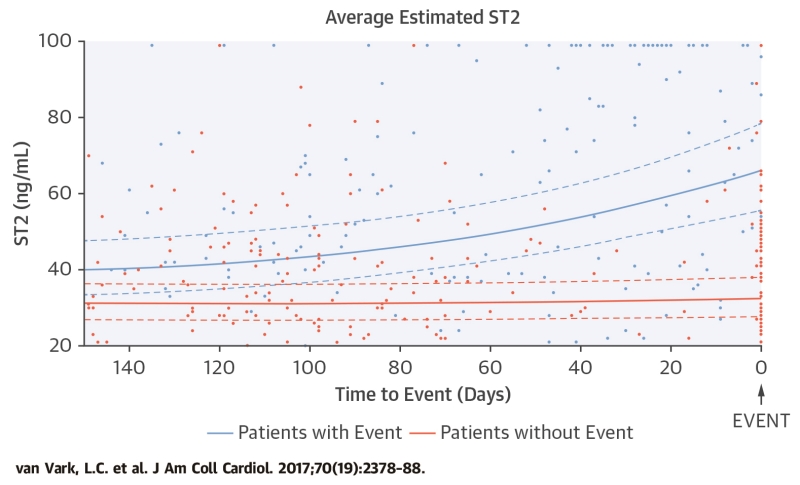
图3. 平均估计ST2模式,结合个别ST2测量。
主要终点(全因死亡和心衰再入院的复合终点)发生之前或随访结束时的平均估计ST2模式,结合个别ST2测量。用不同颜色分别表示经历(蓝色)和没有经历(橘色)主要终点的患者。平均估计ST2水平经过年龄、性别、收缩压、糖尿病、LVEF、过去6个月内因HF住院、缺血性HF、体重指数、eGFR、出院使用药物(血管紧张素转换酶抑制剂和/或血管紧张素II受体拮抗剂,β-阻断剂,利尿剂)及NT-proBNP校正。




