糖化血红蛋白质控品性能参数评价研究
作者: 马越云 黄 月
【摘要】目的 对糖化血红蛋白(HbA1c)质控品的各项性能参数进行评估,以确定该糖化血红蛋白质控品的可靠性和稳定性。方法 采用糖化血红蛋白国家标准物质(GBW09181a和GBW09183a)作为校准品,对日本TOSOH ORPORATION生产的HLC-723G8型全自动糖化血红蛋白分析仪进行校准;对世瑞纳科(天津)医疗科技有限公司生产的糖化血红蛋白质控品的性能参数:正确度、准确度、精密度、稳定性等性能参数进行评估。结果(1)准确度检测结果:检测结果与国家标准物质标示值的相对误差为-1.00、0.65和1.42;(2)均匀性检测结果:瓶内精密度与瓶间精密度的变异系数均≤3.0%;(3)稳定性检测结果:检测结果与国家标准物质标示值的相对误差为-1.00、0.65和1.42。结论 糖化血红蛋白质控品的性能参数:正确度、准确度、精密度、稳定性各项指标稳定,是一种稳定和可靠的糖化血红蛋白检测的质控物。
【关键词】高效液相色谱法;糖化血红蛋白;精密度、线性
糖化血红蛋白(Ghb)是指人血红蛋白的a链和β链与血液中的葡萄糖通过持续、缓慢且不可逆的糖化反应所形成的产物,包括:HbA1a、HbA1b、和HbA1c。其中HbA1c约占70%,HbA1c是β链N端与葡萄糖进行非酶促蛋白糖化反应的产物,是糖尿病患者的一个重要的监测指标[1],可以反映糖尿病患者最近2~3个月血糖控制情况[2, 3]。先后被美国糖尿病协会(ADA)、国际糖尿病联盟(IDF)、世界卫生组织(WHO)等纳入糖尿病诊断标准。美国临床化学协会糖化血红蛋白标准化分会等多组织都建议通过高效液相色谱法检测糖化血红蛋白[3-5];所以HbA1c作为糖尿病筛查、诊断、血糖控制和糖尿病疗效评价的重要指标,在临床上已经被广泛应用。
目前常见的糖化血红蛋白分析仪都是基于离子交换的高效液相色谱技术,而该技术的分析结果受到糖化血红蛋白洗脱液、糖化血红蛋白溶血剂、糖化血红蛋白层析柱、糖化血红蛋白校准品等因素影响,因此准确检测糖化血红蛋白,需要以上部分的完美组合[6]。稳定的柱液系统是检测结果可靠的保证,而质控品在其中又扮演着极其重要的作用。目前市场上高效液相色谱法检测糖化血红蛋白的系统相对封闭,厂家的洗脱液、溶血剂和层析柱较为独立,缺少竞争,造成价格的垄断,广大患者需要承担较高的医疗费用成本;国内市场急需要具有质量稳定、价格低廉的竞品试剂,从而降低医疗机构的检测成本。另外,为保证检验质量,《医学实验室质量和能力认可准则》(ISO15189)要求:实验室更换或使用新的检测试剂或系统,需对之进行性能验证或评价,以判断其能否满足临床需要。故本课题组对国产化的诊断试剂进行了较为详细的质控品参数性能分析,为临床应用中如何选择和评价一个同类的竞争产品为医疗机构和临床应用提供更多参考和依据。
一、研究材料与方法
1. 材料:(1)国家标准物质:人血红蛋白溶液中糖化血红蛋白标准物质(编号:GBW09181a、GBW09182a、GBW09183a)购自于北京医院卫生部临床检验中心;(2)一级参考物质:采用糖化血红蛋白国家标准物质(编号:GBW09181a和GBW09183a),可溯源至国家标准物质;(3)糖化血红蛋白校准品:采用糖化血红蛋白国家标准物质作为校准品(编号:GBW09181a和GBW09183a)。(4)仪器设备:日本TOSOH CORPORATION生产的HLC-723G8型全自动糖化血红蛋白分析仪。(5)糖化血红蛋白分析试剂和糖化血红蛋白层析柱:以下试剂和层析柱购自世瑞纳科(天津)医疗科技有限责任公司:
糖化血红蛋白分析用洗脱液(高效液相色谱法):货号:XN-TSG8-01;批号:TSG80119051701;
糖化血红蛋白分析用洗脱液(高效液相色谱法):货号:XN-TSG8-02、批号:TSG80219051801;
糖化血红蛋白分析用洗脱液(高效液相色谱法):货号:XN-TSG8-03、批号:TSG80319051901。
糖化血红蛋白溶血剂:货号:XN-TSG8-04;批号:TSG80419051401。
糖化血红蛋白层析柱:货号:XN-TSG8-TC;批号:TSG8TC19052001。
2.方法:(1)准确性测试:糖化血红蛋白国家标准物质编号:GBW09181a、GBW09182a和GBW09183a等高值、中值和低值3水平作为检测样本,上述测量系统经国家标准物质(GBW09181a和GBW09183a)作为糖化血红蛋白校准品,对HLC-723G8型全自动糖化血红蛋白分析仪进行校准,校准后对国家标准物质样本进行测试,重复次数为3次;检测结果数值与国家标准物质标识值进行比较,以计算其相对误差,其计算方法如下:相对误差(RE)=(均值-理论值)/理论值×100% 。(2)均匀性测试:① 瓶内精密度:选取糖化血红蛋白质控品最小包装单元(水平1和水平2)各1瓶,采用上述糖化血红蛋白HbA1c的测量系统,经国家标准物质(编号:GBW09181a和GBW09183a)校准后,分别对各水平糖化血红蛋白质控品平行测试10次;计算各水平糖化血红蛋白HbA1c质控品的平均值(Mean)、标准差(SD)、变异系数(CV),计算公式为:

② 瓶间精密度:选取5盒糖化血红蛋白质控品的最小包装单元(水平1和水平2)各10瓶,对各水平的糖化血红蛋白质控品的最小包装单元(瓶)随机编号,每瓶校准品各测定1次;采用上述糖化血红蛋白HbA1c的测量系统,经糖化血红蛋白国家标准物质(编号:GBW09181a和GBW09183a)校准后,测试顺序为1-3-5-7-9-2-4-6-8-10-10-9-8-7-6-5-4-3-2-1-2-4-6-8-10-1-3-5-7-9;随机抽取各水平的其中1瓶连续测试3次,计算各水平糖化血红蛋白HbA1c质控品的平均值(Mean)、标准差(SD)、变异系数(CV),计算公式为:

(3)稳定性测试:开瓶/复溶稳定性:① 开瓶/复溶后的瓶内均一性:选取糖化血红蛋白质控品最小包装单元(水平1和水平2)各7瓶,在第7天、第6天、第5天、第4天、第3天、第2天、第1天各复溶1瓶、复溶后储存在2-8℃的避光环境下,最后1次复溶满24小时后,统一采用上述糖化血红蛋白HbA1c的测量系统,经国家标准物质(编号:GBW09181a和GBW09183a)校准后,分别对各水平糖化血红蛋白质控品平行测试10次;计算各水平糖化血红蛋白HbA1c质控品的平均值(Mean)、标准差(SD)、变异系数(CV),计算公式为:

以评价该糖化血红蛋白质控品的瓶内均一性。② 开瓶/复溶后的瓶间均一性:选取糖化血红蛋白质控品最小包装单元(水平1和水平2)各10瓶,在第7天、第6天、第5天、第4天、第3天、第2天、第1天各复溶1瓶、复溶后储存在2-8℃的避光环境下,最后1次复溶满24小时后,统一采用上述糖化血红蛋白HbA1c的测量系统,经国家标准物质(编号:GBW09181a和GBW09183a)校准后,测试顺序为1-3-5-7-9-2-4-6-8-10-10-9-8-7-6-5-4-3-2-1-2-4-6-8-10-1-3-5-7-9;随机抽取各水平的其中1瓶连续测试3次,计算各水平糖化血红蛋白HbA1c质控品的平均值(Mean)、标准差(SD)、变异系数(CV),计算公式为:

以评价该糖化血红蛋白质控品的瓶间均一性。③ 开瓶/复溶后的准确性:选取糖化血红蛋白质控品最小包装单元(水平1和水平2)各1瓶,复溶后储存在2-8℃的避光环境下7天后,统一采用上述糖化血红蛋白HbA1c的测量系统,上述测量系统经国家标准物质(GBW09181a和GBW09183a)作为糖化血红蛋白校准品校准后,对糖化血红蛋白国家标准物质编号:GBW09181a、GBW09182a和GBW09183a等高值、中值和低值3水平作为检测样本,重复次数为3次;检测结果数值与国家标准物质标识值进行比较,以计算其相对误差,其计算方法如下:相对误差=(均值-理论值)/理论值×100% 。
3. 统计学方法:检测结果以Mean±SD格式进行表示,采用SPSS16.0统计学软件对数据进行统计分析和线性回归分析,统计学上以P<0.05表示具有统计学差异。
二、研究结果
1. 准确性测试结果:由上述试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,重复3次测量国家标准物质,检测结果均值(Mean)、标准差(SD)和国家标准物质标识靶值的相对误差(RE)见表1。
表1. 国家标准物质的检测结果
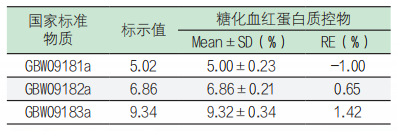
上述产品准确度检测结果的相对误差均≤±3.0%,符合糖化血红蛋白检测可接受范围要求。
2. 均匀性测试结果:(1)瓶内精密度:由上述试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,测量水平1和水平2物质,检测结果均值(Mean)、标准差(SD)和国家标准物质标识靶值的变异系数(CV)见表2。
表2. 瓶内水平1和水平2的检测结果
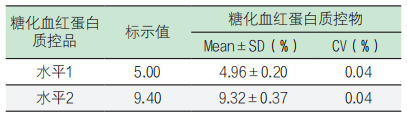
上述产品均一度检测结果的变异系数均≤3.0%,符合糖化血红蛋白检测可接受范围要求。(2)瓶间精密度:由上述试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,测量水平1和水平2物质,检测结果均值(Mean)、标准差(SD)和国家标准物质标识靶值的变异系数(CV)见表3。
表3. 瓶间水平1和水平2的检测结果
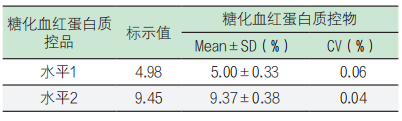
上述产品均一度检测结果的变异系数均≤3.0%,符合糖化血红蛋白检测可接受范围要求。
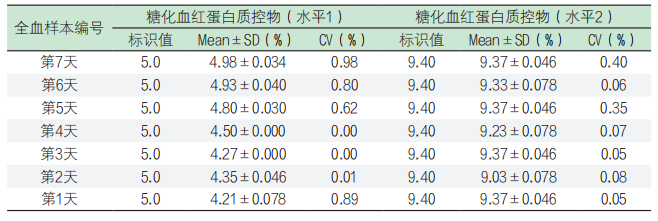
3. 稳定性测试结果:(1)由上述同一批次试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,测量瓶内均一性,检测结果均值(Mean)、标准差(SD)和变异系数(CV)见表4。
表4. 瓶内均一性测试
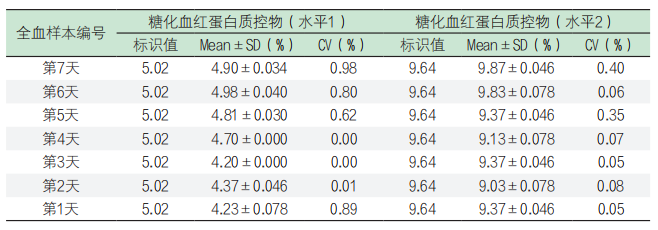
上述该试剂产品对样本检测,检测结果的瓶内均一性变异系数均≤3.0%,符合糖化血红蛋白检测可接受范围要求。(2)上述同一批次试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,测量瓶内均一性,检测结果均值(Mean)、标准差(SD)和变异系数(CV)见表5。
表5. 瓶间均一性测试
上述该试剂产品对样本检测,检测结果的瓶间均一性变异系数均≤3.0%,符合糖化血红蛋白检测可接受范围要求。(3)由上述试剂产品与TOSOH CORPORATION HLC-723G8型糖化血红蛋白分析仪组成测量系统,重复3次测量国家标准物质,检测结果均值(Mean)、标准差(SD)和国家标准物质标识靶值的相对误差(RE)见表6。
表6. 国家标准物质的检测结果
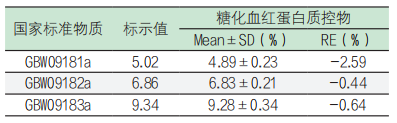
上述产品准确度检测结果的相对误差均≤±3.0%,符合糖化血红蛋白检测可接受范围要求。
三、分析与讨论
质量控制是实验检测质量保证体系中的重要组成部分,其目的是为了保证每例样本分析结果的可靠性和稳定性。一是准确度高,即测定结果正确,接近真值;二是精密度高,即测定结果的重复性好,实验室每天测定的结果变化很小,消除或减少随机误差造成的影响。主要消除或减少系统误差的影响。质控物在临床化学质量控制工作中起着决定性的作用,对糖化血红蛋白质控物的各项性能参数的评价可以准确反应该系统是否适合实验室的分析检验工作。
从临床应用上看,糖化血红蛋白分析仪的试剂系统相对封闭,需要做到专机配专业洗脱液、溶血剂和糖化血红蛋白层析柱等耗材。中国市场依赖更多进口设备厂商配套的糖化血红蛋白质控品,糖化血红蛋白质控的性能参数决定着实验室检测的质量,因此,对糖化血红蛋白质控品的性能做出客观的评价,是临床检测重要节点。
本研究是通过对糖化血红蛋白质控品性能参数分析,来判断糖化血红蛋白质控品性能是否适用实验或临床检测。由相关性能参数的检测结果显示:从准确度的检测结果来看:该试剂产品的准确度的相对误差均≤±6.0%,符合糖化血红蛋白检测标准的要求,该糖化血红蛋白质控品的均匀性的精密度≤3.0%,符合糖化血红蛋白检测临床标准的要求;糖化血红蛋白质控品的稳定满足精密度≤3.0%和准确度的的相对误差均≤±6.0%;因此可以确定糖化血红蛋白质控品满足临床应用要求。
综上所述,世瑞纳科(天津)医疗科技有限公司生产的糖化血红蛋白质控品的性能参数指标准确稳定,可以满足临床检测的要求。
参考文献
Chapelle JP, Teixeira J, Maisin D, Assink H, Barla G, Stroobants AK, Delzenne B, van den Eshof W: Multicentre evaluation of the Tosoh HbA1c G8 analyser. Clin Chem Lab Med 2010, 48(3):365-371.
Imdahl R, Roddiger R, Casis-Saenz E: Multicenter Evaluation of a New High-Throughput HbA1c Testing Platform. Clin Lab 2016, 62(12):2405-2412.
Maesa JM, Fernandez-Riejos P, Mora CS, de Toro M, Valladares PM, Gonzalez-Rodriguez C: Evaluation of Bio-Rad D-100 HbA1c analyzer against Tosoh G8 and Menarini HA-8180V. Pract Lab Med 2016, 5:57-64.
Lenters-Westra E, English E: Evaluating new HbA1c methods for adoption by the IFCC and NGSP reference networks using international quality targets. Clin Chem Lab Med 2017, 55(9):1426-1434.
Manley SE, Hikin LJ, Round RA, Manning PW, Luzio SD, Dunseath GJ, Nightingale PG, Stratton IM, Cramb R, Sikaris KA et al: Comparison of IFCC-calibrated HbA(1c) from laboratory and point of care testing systems. Diabetes Res Clin Pract 2014, 105(3):364-372.
Wu X, Chao Y, Wan Z, Wang Y, Ma Y, Ke P, Wu X, Xu J, Zhuang J, Huang X: A comparative evaluation of the analytical performances of Capillarys 2 Flex Piercing, Tosoh HLC-723 G8, Premier Hb9210, and Roche Cobas c501 Tina-quant Gen 2 analyzers for HbA1c determination. Biochem Med (Zagreb) 2016, 26(3):353-364.
Peter A, Fritsche A, Stefan N, Heni M, Haring HU, Schleicher E: Diagnostic value of hemoglobin A1c for type 2 diabetes mellitus in a population at risk. Exp Clin Endocrinol Diabetes 2011, 119(4):234-237.
Van Aelst S, Claerhout H, Nackers E, Desmet K, Kieffer D: Hemoglobin S monitoring on TOSOH G8 in hemoglobin A1c mode in case of urgent red blood cell exchange. J Clin Lab Anal 2018, 32(7):e22453.





