合并融合基因异常的慢性髓细胞白血病急髓变患者临床和实验室特征分析

王小蕊,上海市第一人民医院检验医学中心,内科学(血液病学)硕士/生物工程学硕士,主管技师,从事血液肿瘤细胞遗传和分子诊断的研究。中国医药质量管理协会血液病学组委员。主持上海市教委人才计划1项,参与国家级/市级课题10余项,以第一作者/通讯作者发表核心期刊论文7篇, SCI论文4篇,其中“Prognostic significance of diagnosed WT1 level in acute myeloid leukemia: a meta-analysis”被收录于NCCN-AML指南(v1.2022)。

李莉,医学博士、美国匹兹堡大学医学院(UPMC)博士后、主任医师/主任技师,博士生导师。现任上海市第一人民医院检验医学中心主任。长期从事肥大细胞与疾病研究,培养研究生40余名。获得国家自然科学基金资助项目等重点研究课题30余项,发表论文140余篇,著作21部。现兼任中华医学会检验医学分会和微生物与免疫学分会副主任委员,中华医学检验教育学院副院长,中国老年保健医学研究会检验分会副主任委员,中国医师协会检验医师分会副会长,中国医院协会检验专业委员会常委。
【摘要】目的 探讨伴KMT2A-MLLT3基因阳性的慢性髓细胞白血病急变(CML-BP)患者临床和实验室特征,以提高对该类型疾病的认识和及时发现,积累经验并提供参考。方法 回顾性分析我院收治的1例伴KMT2A-MLLT3基因阳性的CML-BP患者临床特征、诊治过程和实验室指标。结果 患者于2017年确诊为CML,2018年进展为CML-BP,BCR-ABL1伴KMT2A-MLLT3阳性且T315I突变。2019年1月行异基因造血干细胞移植,6个月后复发,经普纳替尼联合供者淋巴细胞输注治疗无效后死亡。结论 伴KMT2A-MLLT3阳性的CML-BP患者疾病进展迅速,预后差,尽早行异基因造血干细胞移植或可改善预后。多种融合基因筛查有助于有效补充核型分析数据,辅助临床早期制定治疗方案和评估预后。
【关键词】BCR-ABL1;KMT2A-MLLT3;T315I突变;异基因造血干细胞移植
近年来,得益于靶向药物的大量涌现,精准医学尤其在肿瘤领域,得到了迅猛的发展。精确诊断是精准医学的重要保障。血液肿瘤的实验室诊断是血液肿瘤治疗的基石,传统的骨髓涂片、细胞化学染色和骨髓病理检查已无法满足精准医疗的需求。检测肿瘤特异性基因突变,RNA水平基因表达量,细胞表面抗原等基于生物学样本的监测可以动态评估疾病,贯穿治疗始终,继而使靶向药物和治疗方案更具有针对性。
慢性髓细胞白血病(chronic myeloid leukemia,CML)是一种源于多能造血干细胞的恶性克隆性疾病,占成人白血病的15%[1],约95%以上的CML细胞中会出现BCR-ABL1融合基因[2]。依据白细胞数量、原始细胞比例等,可将CML分为慢性期(chronic phase,CP),加速期(accelerated phase,AP)和急变期(blast phase,BP)。其中约76%的CML-BP患者可检出额外细胞遗传学异常,但合并其他融合基因较为罕见[3]。
KMT2A基因位于11号染色体长臂2区3带(11q23),在成人AML中约占3%-7%,目前已发现约77种对手基因。11q23/KMT2A与其他染色体的平衡易位,影响如HOXA等基因的表达导致细胞分化阻滞引发白血病[4]。伴11q23/KMT2A易位的AML预后主要取决于其对手基因。目前最为常见的为t(9;11)(p22;q23)易位,形成KMT2A-MLLT3(MLL-AF9)融合基因。KMT2A-MLLT3在欧洲白血病网络(ELN)危险度分层中位于标危组(intermediate),而其他伴11q23/KMT2A易位的AML均位于高危组,预后不良[5]。KMT2A-MLLT3在伴11q23/KMT2A易位的AML中发生率约为44%,虽被列为标危组,但研究显示,预后优于其他标危组患者[4]。但对于CML急变并伴KMT2A-MLLT3的患者的预后尚需更多临床实践的积累。现复习相关文献并分析我院收治的伴有KMT2A-MLLT3融合基因的CML-BP患者临床情况,与读者共讨论分析实验室诊断在血液肿瘤精准治疗中的积极作用,以期获得指导和提升。
一、病例资料
患者,男,48岁,因出现无明显诱因低热、乏力、盗汗于2017年1月11日来我院就诊,血细胞分析结果:白细胞总数224.5×109/L,血小板总数306×109/L。查体:全身粘膜无黄染,无瘀点瘀斑及出血点,全身浅表淋巴结未触及肿大,腹平软、无压痛,肝脾肋下未触及。骨髓象:粒系增生极度活跃,比例明显增高,占88%,嗜碱性粒细胞占6%;红系增生受抑制;碱性磷酸酶(AKP)积分8分/100NC。核型分析显示46,XY,t(9;22)(q34;q11)[6],BCR-ABL1定量136.8%(图1)。
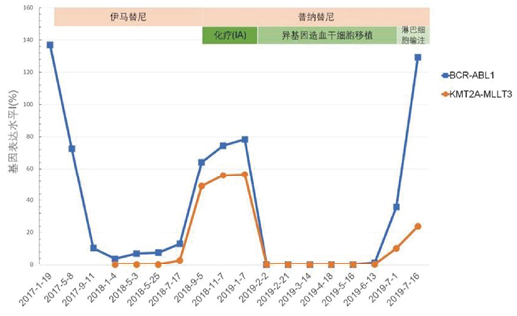
图1. BCR-ABL1和KMT2A-MLLT3在各治疗阶段表达水平
以慢性髓细胞白血病慢性期(CML-CP)收治入院。入院后给予伊马替尼400mg/d治疗。2018年1月患者达到血液学缓解,BCR-ABL1比例下降至3.61%,ABL1激酶突变检查显示未见突变。2018年9月15日骨髓象示原始细胞增多,占66%,以单核细胞为主(图2);BCR-ABL1定量64.01%。ABL1激酶突变检测示T315I突变。核型分析示未见分裂象。56种融合基因PCR筛查发现KMT2A-MLLT3阳性(48.79%)。荧光原位杂交(fluorescence in situ hybridization,FISH)检测分别显示约80%的细胞呈现BCR-ABL1融合信号,约75%的细胞呈现KMT2A分离信号(图3),故诊断慢性粒细胞白血病急髓变(AML-M5)。再次入院,治疗方案改为去甲氧柔红霉素(Idarubicin,IDA)联合阿糖胞苷(cytarabine,Ara-c)的IA方案加普纳替尼(Ponatinib),经3个月治疗无效,于2019年1月21日行异基因造血干细胞移植,移植后继续口服普纳替尼预防复发。BCR-ABL1和KMT2A-MLLT3融合基因在移植后6个月内多次随访均显示低于检测限,达到分子生物学完全缓解。2019年6月13日检测到BCR-ABL1定量1.12%,KMT2A-MLLT3定量0.21%,2019年7月11日骨髓象示有核细胞增生活跃,原始细胞占12%。BCR-ABL1定量35.75%,KMT2A-MLLT3定量10.10%;ABL1激酶突变显示T315I突变;核型分析示未见分裂象。FISH检测BCR-ABL1融合基因和KMT2A基因显示阳性率分别为82%和62%。确诊为CML-BP异基因造血干细胞移植后复发,经普纳替尼联合供者淋巴细胞输注治疗无效,于2019年8月5日死亡。
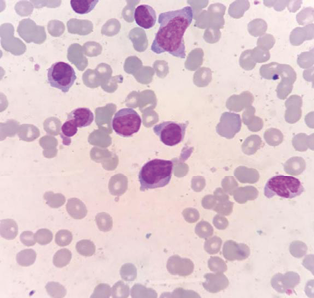
图2. 伴KMT2A-MLLT3的CML-BP患者骨髓象,原始细胞增高,以原/幼单核细胞为主
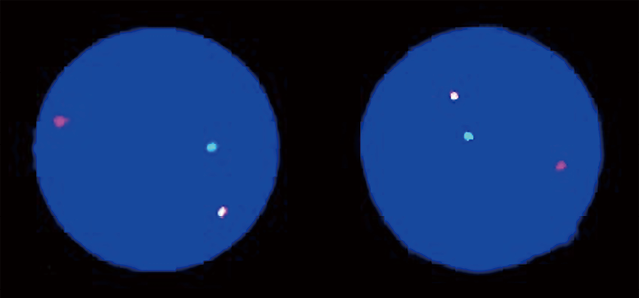
图3. KMT2A分离探针间期FISH检测结果,红/绿为KMT2A分离信号,提示KMT2A基因有易位
二、讨论及文献复习
出现额外核型异常是CML常见的进展和急变现象,约76%的CML-BP患者可伴有额外核型异常。研究认为,一些异常是由BCR-ABL1造成的染色体不稳定导致,而另一些异常则可引发向急性白血病的转变[3]。常见额外核型异常包括+8,+Ph,-7,i(17q),+21和-Y等,但伴有融合基因异常则非常罕见。Z Chen等[3]研究显示伴inv(16)的CML-BP患者约占2.2%。Salem等[6]对10例CML-BP伴CBFβ-MYH11融合基因阳性患者研究发现,这些患者多为男性,均因出现额外融合基因异常而进展为AML,且预后差,与本例患者相似。
KMT2A基因位于11号染色体长臂2区3带(11q23)。11q23/KMT2A基因的异常多见于血液系统恶性肿瘤,多数预后不良[7]。涉及KMT2A易位的急性白血病常见于急性单核细胞白血病或急性粒单核细胞白血病,该病例骨髓涂片与此表现吻合。伴KMT2A-MLLT3异常的AML患者在预后危险度分级评估为预后中等,但合并CML发生的鲜有报道[8]。Marum等[9]运用RNA测序发现2例CML-BP患者具有KMT2A融合基因异常(KMT2A-BCAT1和KMT2A-MLLT6),且皆在短时间内由CML-CP转入CML-BP,说明伴KMT2A易位的CML-BP疾病进展较快。本例患者从明确诊断至急性变仅21个月,远低于文献报道CML中位急变期41个月[10],这与Marum等人的研究结果一致。“二次打击”假说认为,信号通路活化、促进增殖密切相关的I类基因异常和参与细胞分化阻滞的II类基因异常协同作用是引起血液肿瘤发生的重要原因。推测作为I类基因异常的BCR-ABL1和II类基因异常的KMT2A-MLLT3的联合作用,可能是加速疾病进展的主要原因[11]。同时,回溯该患者CML-CP期间样本的KMT2A-MLLT3融合基因检测,均为阴性。提示病程中发生的KMT2A-MLLT3可能在该患者进展为AML中起关键作用[9, 10]。
普纳替尼作为三代TKI已被推荐用于治疗T315I突变的CML患者[12]。陈晨等和周雅等[13, 14]的小样本研究均显示三代TKI抑制剂普纳替尼在T315I患者移植后的挽救性治疗中效果显著。而此例T315I突变CML-BP患者在治疗中和移植后均给予三代TKI,但未能奏效,与以往报道不符,推测可能与伴有KMT2A-MLLT3有关。更多临床样本的研究或许能揭示KMT2A-MLLT3在CML进展为AML中的作用及其机制。
在检验实践中,虽然核型分析在血液肿瘤尤其是CML诊断中起到重要作用,但不可避免的因各种原因会出现标本中无可供检测、分析的中期分裂象的情况。研究表明,AML患者中约有10%的患者会遇到核型分析失败的情况,如没有分裂象或者分裂象质量差无法进行分析。将该现象结合患者的临床信息综合分析后发现此类患者对化疗不敏感,且生存状况与高危组近似,是预后不良的标志[15]。本例患者CML-BP后,两次培养法核型分析均未见分裂象,而在56种融合基因PCR筛查中同时检出BCR-ABL1和KMT2A-MLLT3融合基因阳性。提示我们,伴有此类额外异常的CML-BP患者染色体分裂象在体外不易分裂,难以观察到,仅依靠核型分析有可能漏检,需联合其他检测方法作为核型分析的补充,确保早发现、不漏诊。虽然定量PCR和FISH检测显示BCR-ABL1和KMT2A-MLLT3比例趋势呈现一致性,但无法明确两个融合基因是否来源于同一克隆。改进培养方式,或可提高此类患者的核型分析检出率,有助于甄别克隆来源。
该病例提示我们,①伴有KMT2A-MLLT3阳性的CML-BP疾病进展迅速,预后差,常规AML预后分层规则对其没有指导意义。尽早进行异基因造血干细胞移植或可改善生存;②普纳替尼对于T315I突变的此类患者可能疗效不佳;③对CML加速期和急变期患者骨髓细胞在常规核型分析基础上,监测多种融合基因,既能弥补核型分析精确度低的缺陷,又能从基因改变早期发现疾病由慢性向急性转变,辅助临床评估预后并早期采取有效治疗措施。虽然基因检测和异基因造血干细胞移植在白血病中诊断和治疗中的应用还有许多未解之谜,需要不断积累病例,深入研究。但可以看到,基于生物学样本的实验室精确诊断,可以更快速有效反映疾病变化状况,在疾病发生发展早期为临床个体化治疗提供依据,有效延长患者生存。
利益冲突:所有作者均声明不存在利益冲突
参考文献
Chinese society of hematology cma. [The guidelines for diagnosis and treatment of chronic myelogenous leukemia in China (2020 edition)] [J]. Zhonghua Xue Ye Xue Za Zhi, 2020, 41(5): 353-364 DOI: 310.3760/cma.j.issn.0253-2727.2020.3705.3001.
李章坤, 赖应昌, 姚淑仪, 等. 伴JAK2+V617F突变的慢性粒细胞白血病一例并文献复习 [J]. 白血病·淋巴瘤, 2019, 28: 298-300 DOI:210.3760/cma.j.issn.1009-9921.2019.3705.3011
Chen Z, Shao C, Wang W, et al. Cytogenetic landscape and impact in blast phase of chronic myeloid leukemia in the era of tyrosine kinase inhibitor therapy [J]. Leukemia, 2017, 31(3): 585-592 DOI:510.1038/leu.2016.1231. .
Bill M, Mrozek K, Kohlschmidt J, et al. Mutational landscape and clinical outcome of patients with de novo acute myeloid leukemia and rearrangements involving 11q23/KMT2A [J]. Proc Natl Acad Sci U S A, 2020, 117(42): 26340-26346.
Dohner H, Estey E, Grimwade D, et al. Diagnosis and management of AML in adults: 2017 ELN recommendations from an international expert panel [J]. Blood, 2017, 129(4): 424-447 DOI:410.1182/blood-2016-1108-733196.
Salem a, Loghavi S, Tang G, et al. Myeloid neoplasms with concurrent BCR-ABL1 and CBFB rearrangements: A series of 10 cases of a clinically aggressive neoplasm [J]. Am J Hematol, 2017, 92(6): 520-528 DOI:510.1002/ajh.24710.
Meyer C, Burmeister T, Groger D, et al. The MLL recombinome of acute leukemias in 2017 [J]. Leukemia, 2018, 32(2): 273-284 DOI:210.1038/leu.2017.1213.
Leukemia lymphoma group csohcma. [Chinese guidelines for diagnosis and treatment of adult acute myeloid leukemia (not APL) (2017)] [J]. Zhonghua Xue Ye Xue Za Zhi, 2017, 38(3): 177-182 DOI: 110.3760/cma.j.issn.0253-2727.2017.3703.3001.
Marum J E, Wang P P, Stangl D, et al. Novel fusion genes at CML diagnosis reveal a complex pattern of genomic rearrangements and sequence inversions associated with the philadelphia chromosome in patients with early blast crisis [J]. Blood, 2016, 128(22): 1219-1219.
Jain P, Kantarjian H M, Ghorab A, et al. Prognostic factors and survival outcomes in patients with chronic myeloid leukemia in blast phase in the tyrosine kinase inhibitor era: Cohort study of 477 patients [J]. Cancer, 2017, 123(22): 4391-4402 DOI:4310.1002/cncr.30864.
Takahashi S. Current findings for recurring mutations in acute myeloid leukemia [J]. J Hematol Oncol, 2011, 4(36 DOI:10.1186/1756-8722-1184-1136.
Hochhaus A, Baccarani M, Silver R T, et al. European leukemiaNet 2020 recommendations for treating chronic myeloid leukemia [J]. Leukemia, 2020, 34(4): 966-984 DOI: 910.1038/s41375-41020-40776-41372.
周雅, 许娜, 谢双锋, 等. 泊那替尼挽救性治疗allo-HSCT后复发伴T315I突变CML+12例的疗效分析 [J]. 中华器官移植杂志, 2018, 39: 338-343 DOI:310.3760/cma.j.issn.0254-1785.2018.3706.3004
陈晨, 许娜, 江雪杰, 等. T315I基因突变的慢性髓性白血病临床特征及泊那替尼疗效 [J]. 南方医科大学学报, 2019, 39: 364-368 DOI:310.12122/j.issn.11673-14254.12019.12103.12116
Medeiros B C, Othus M, Estey E H, et al. Unsuccessful diagnostic cytogenetic analysis is a poor prognostic feature in acute myeloid leukaemia [J]. British journal of haematology, 2014, 164(2): 245-250 DOI:210.1111/bjh.12625.




