肿瘤NGS液体活检技术评估标准

肖燃,广州燃石医学检验所有限公司,获英国阿伯丁大学与南京农业大学联合培养博士;主持或参与国家级、省级自然科学基金4项;以第一作者发表SCI学术文章3篇;具有肿瘤基因诊断领域医学科研项目经验。
【摘要】近期,SEQC2项目对5家全球领先肿瘤靶向NGS检测试剂盒厂商(Roche Sequencing Solutions(简称ROC)、Illumina、IDT(Integrated DNA Technologies)、Thermo Fisher Scientific(简称TFS),以及燃石医学(BRP)的ctDNA分析方法的分析性能进行多站点、跨平台评估的结果在线发表于Nature Biotechnology上。研究采用模拟测序数据和对人工合成的人类ctDNA参考材料,以ctDNA测序工作流程中每个步骤变量对分析结果的影响,严格评估五种领先的ctDNA分析方法的结果有效性。结果显示,当ctDNA VAF≥0.5%时,所有检测方法都能可靠检出(具有较高的灵敏度和重复性),但在ctDNA VAF<0.5%时,检测准确性有所下降,且各检测方法间存在差异。SEQC2项目结果显示,基于靶向捕获平台开发的燃石(朗清® 168基因)ctDNA检测panel在检测灵敏度、特异性、准确性、可重复性和稳定性等方面均有优异表现,从各维度横向比较均名列前茅。SEQC2项目所评估的灵敏度、假阳性率、可重复性等指标让临床可以直观、客观、全面、且定量地感受液体活检技术,为基于NGS的液体活检产品提供判断标准。
【关键词】循环肿瘤DNA;液体活检;检测灵敏度;SEQC2
近年来,随着技术的不断更新推进,基于循环肿瘤DNA(ctDNA)的液体活检技术为驱动基因的检测及微小残留病灶(MRD)的追踪提供了精准、便捷的方法,成为早期肿瘤患者预后分层与复发风险评估的新兴手段,无法获得组织样本的肿瘤患者的有效替代方案,以及患者全病程管理的有效助力工具,具有重要的临床价值和良好的应用前景。
基于NGS液体活检技术作为肿瘤精准医疗领域的核心技术之一,已被广泛应用于临床实践。但NGS技术较为复杂,检测质量难以量化和标准化评估是临床应用面临的挑战之一。2021年4月,Nature Biotechnology(IF=36.558)在线发表了由美国食品药品监督管理局(FDA)领导的基因芯片/测序质控(MicroArray/Sequencing Quality Control,MAQC)协会在SEQC2项目中的循环肿瘤DNA(ctDNA)靶向测序研究结果,指出辨别优秀液体活检技术的关键性能指标,为临床实践中量化评估液体活检产品提供了坚实的依据。
SEQC2研究通过单盲的多站点、跨平台分析性能验证,评估液体活检产品的临床实践核心指标,旨在建立行业标准,提供技术指南。研究纳入了5家全球领先肿瘤靶向NGS检测试剂盒厂商:Roche Sequencing Solutions(简称ROC)、Illumina、IDT(Integrated DNA Technologies)、Thermo Fisher Scientific(简称TFS),以及燃石医学(BRP),采用模拟测序数据和对人工合成的人类ctDNA参考材料,以ctDNA测序工作流程中每个步骤变量对分析结果的影响,严格评估五种领先的ctDNA分析方法的结果有效性。结果显示,当ctDNA VAF≥0.5%时,所有检测方法都能可靠检出(具有较高的灵敏度和重复性),但在ctDNA VAF<0.5%时,检测准确性有所下降,且各检测方法间存在差异。
1. SEQC2研究内容与结果:ctDNA检测是从提取的含非肿瘤细胞的游离DNA——cfDNA背景中识别的,为去除混杂的实验变量,首先生成模拟NGS文库,通过杂交捕获测序模拟无细胞DNA的靶向分析,然后使用模拟自然人类基因和突变的合成DNA序列评估ctDNA分析性能。血浆中ctDNA丰度的变化可能与患者肿瘤进展、对治疗的敏感或耐药等相关,因此,定性识别突变的同时,还须准确检测ctDNA突变频率。研究显示,在最大片段深度处,可以可靠地解析0.8%的变异等位基因频率(VAF),但低于该水平的VAF分析结果不准确,同时会受到测序深度与覆盖率的影响。证明患者早期或治疗期间准确识别低频ctDNA突变具有难度。
大规模的多站点、跨平台ctDNA分析研究中,使用合成参考DNA样本,从十种不同人类癌细胞系中提取的基因组DNA以相同的丰度合并,模拟癌症样本(样本A)。收集的样本以及每个单独的细胞系进行基因分型,在外显子编码区内建立一组约40000个“已知变体”和约10.2MB的“已知阴性”(与每个细胞系中的人类参考基因组相匹配的位置)编码区域,构成参考注释。为了模拟ctDNA实际场景中的VAF范围,将样品A以已知比例与从非癌症背景细胞系(样品B)提取的DNA混合,以创建另外两个参考样品:高Lbx(20%A/80%B)和低Lbx(4%A/96%B),并进行酶切筛选约160-180bp的DNA片段,模拟体内ctDNA长度与浓度,分配至各平台进行敏感性、准确性、重复性评估。各平台分别采用内部分析流程,提交最终结果供独立团队集中评估,该项目是迄今为止ctDNA测序分析性能的最全面评估。
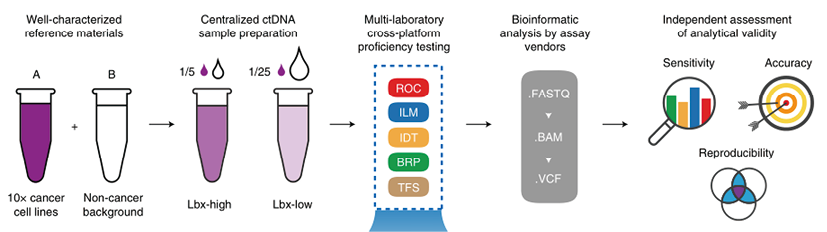
图1. 肿瘤ctDNA高通量测序性能评估过程
2. 灵敏度评估-不仅仅需要足够的测序深度:ctDNA中包括大量低丰度基因变异,一直以来液体活检临床应用的最大瓶颈在于低丰度突变的准确检出,提高测序深度有助于提高检测灵敏度已成为临床专家普遍共识。然而SEQC2项目结果显示,当建库技术能力受限时,单纯增加测序深度已无法有效提高检出率,只有当建库技术提升了灵敏度的天花板,测序深度才能带来更准确的结果。此外,测序覆盖率、覆盖的均一性等也非常重要。SEQC2项目结果揭示了不同建库技术之间的能力差别。
(1)覆盖深度与有效片段回收率:有效片段回收率代表相同体积血液经过重重信号采集和处理后被有效保留的细胞游离DNA(cell free DNA,cfDNA)片段,可直接决定ctDNA检出的可能性。SEQC2项目中测序的单片段中位覆盖深度在1,235X-4,698X之间,ROC(4,698X)>BRP(4,528X)>TFS(3,280X)>IDT(2,476X)>LIM(1,235X),有效片段回收率为63%>60%>44%>33%>17%,意味着ctDNA建库技术方面ROC(罗氏)和BRP(燃石)表现最好。
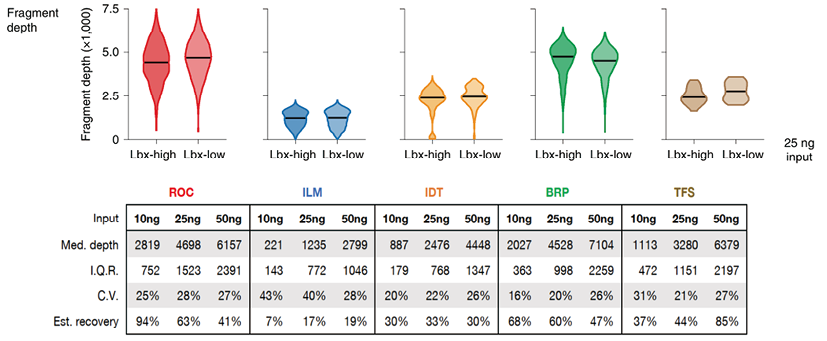
图2. 覆盖深度与有效片段回收率
(2)panel覆盖均一性:在同样都是25ng的DNA投入量情况下(相当于7500个基因组拷贝),SEQC2比较了不同panel测序深度对目标设计区域覆盖率的差异,更好的覆盖均一性可以保障即使困难区域也能得到良好的覆盖,从而提升检测的灵敏度。覆盖均一性最好的是BRP(燃石)和IDT。另外,在燃石朗清与ROC panel有效片段回收率相近的情况下,燃石朗清的覆盖均一性更好。综合以上参数看到,即使原始测序深度并非最高的燃石,在充分保证有效片段回收率、覆盖均一性的情况下,灵敏度仍表现非常突出。
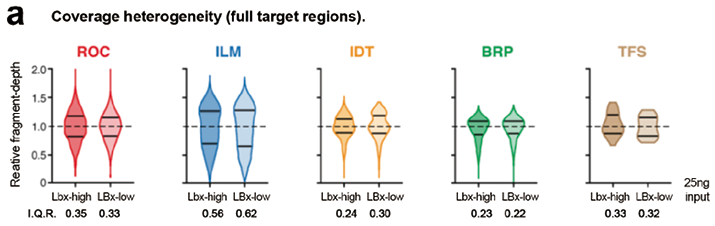
图3. 液体活检panel覆盖均一性评估
高灵敏度检测不仅有助于更精准的晚期用药指导,更加拓展了液体活检的临床应用场景。将液体活检获益的患者从晚期推进到围手术期的MRD(微小残留病灶)检测技术进展迅速,与检测灵敏度的提升密不可分。随着技术的发展和完善,灵敏度的提升有望进一步扩大从液体活检中获益的患者数量,让更多患者受益。
3. 保证液体活检准确性,高灵敏度和低假阳性率缺一不可:临床最关注的液体活检panel性能指标除了灵敏度之外,还有假阳性率,即检测特异性。高灵敏度可保证低频突变的准确识别、不漏检,高特异性则保证“火眼金睛”识别肿瘤来源突变,为患者抓取真正获益的治疗机会,避免错过最佳治疗时间和经济浪费,技术层面往往在灵敏度和特异性不可兼得,如何平衡是液体活检技术准确性面临的又一难题。
SEQC2通过对每个文库目标区域已知变异的检出结果分析,来评估基于杂交捕获法的ctDNA检测灵敏度。在高频突变中,所有panel都表现出了极高的灵敏度,再次佐证了样本中ctDNA含量对检测结果的重要影响。但在VAF到达0.5%以下的“挑战区”时,不同panel的表现开始呈现显著的差异。其中,低VAF突变中燃石朗清与IDT panel成为此次研究中灵敏度最佳的NGS液体活检panel:在VAF为0.3-0.5%时,灵敏度>90%。
此外,也验证了单纯覆盖度深并不一定意味灵敏度高,尽管IDT的单片段覆盖深度较低,但较ROC的灵敏度更高,可能与IDT panel的覆盖均一性高有关。
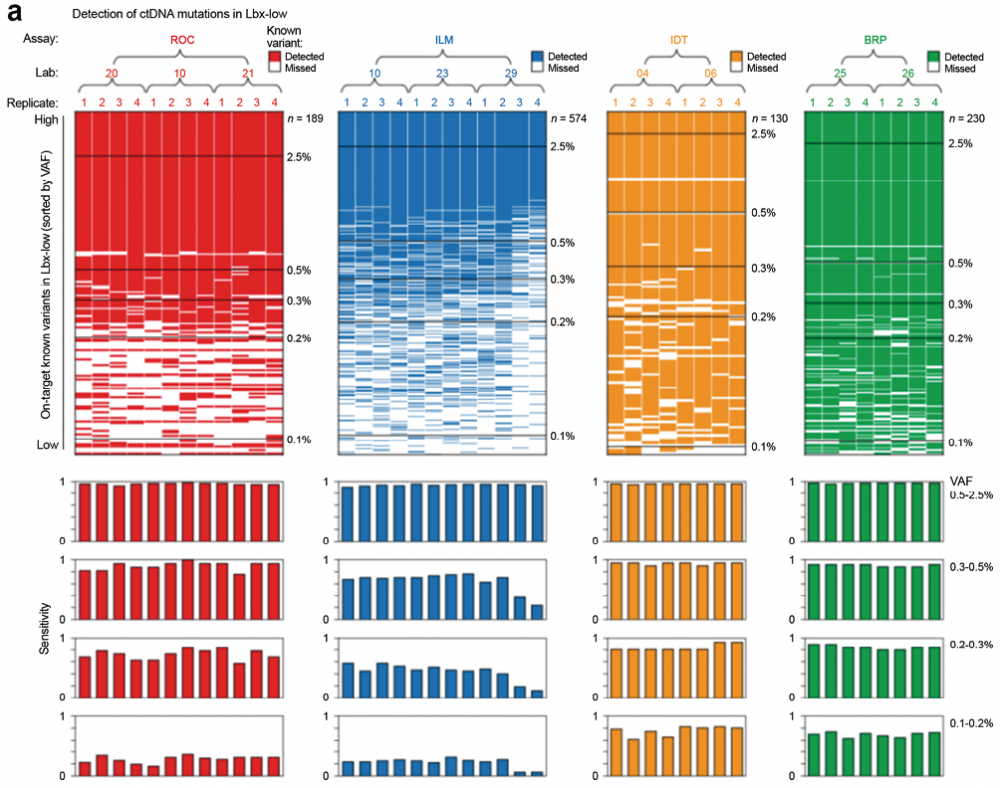
图4. ctDNA检测灵敏度的性能评估
为保证高灵敏度与低假阳性率,所有panel分析均使用独特的分子标识符(Unique Molecular Identifiers,UMIs)纠正测序错误,假阳性率相对较低。在25ng DNA投入量下,假阳性率最低的是BRP(燃石)和ILM(因美纳),分别为0.030FP/kb和0.039FP/kb。综合灵敏度与特异性的整体评估,4个NGS液体活检panel中燃石朗清准确性最佳(见图5)。
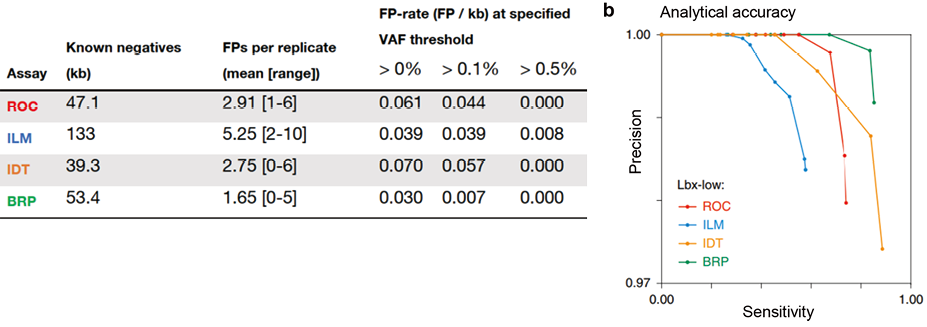
图5. 假阳性率与25ng DNA投入量时的分析准确性
4. ctDNA检测结果可重复性:SEQC2评估了同样的样本在实验室内和实验室间的检测结果可重复性,结果显示,同一panel在同一实验室内不同批次之间和不同实验室不同批次之间的可重复性是相似的。这表明参与SEQC2研究的NGS panel试剂盒的检测性能和生信分析具有较强的稳定性,结果的波动性来自随机而非系统性的室间差异。
它与灵敏度相似,ctDNA VAF≥0.5%时重现性普遍较高,但在0.1%~0.5%时,重现性相对较低,灵敏度是测定重现性的决定因素;尽管样本和组间差异很大,研究人员在实验室内和实验室间比较中没有观察到重现性的显著差异,这表明所有参与的ctDNA panel检测产品和生信分析都是稳定的,结果的波动性来自随机而非系统性的室间差异。该结果表明参与评估的液体活检产品具有较强的稳定性,可保障不同渠道患者检测结果的统一性,帮助患者得出可靠、有效的指导建议。
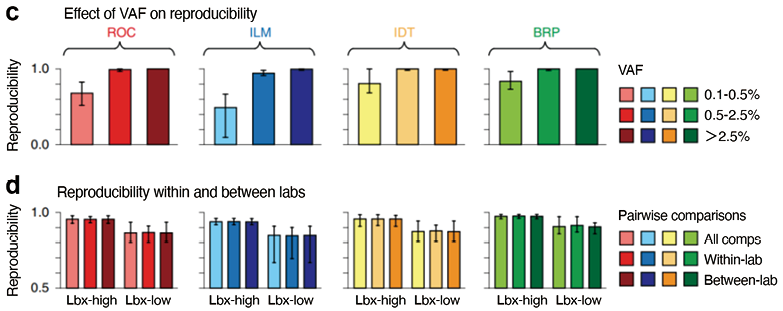
图6. ctDNA检测结果可重复性
5. 低cfDNA总量的“困难”样本检测对液体活检技术提出更高要求:临床实际应用过程中,常面临患者血液样本提取cfDNA含量极低的情况,尤其早期肿瘤患者更为常见,因此,低cfDNA投入量时液体活检性能值得格外关注。SEQC2项目中分别检测高(50ng)、中(25ng)和低(10ng)DNA投入量时各panel的分析性能。覆盖深度与投入量成线性关系,但在不同分析中差异较大。与10 ng相比,25 ng提供的片段深度增加,导致所有分析,尤其是低频变异的灵敏度、重现性和总体诊断性能显著提高。最低10ng DNA投入量时,其中BRP(燃石)稳定性最佳(见图7)。
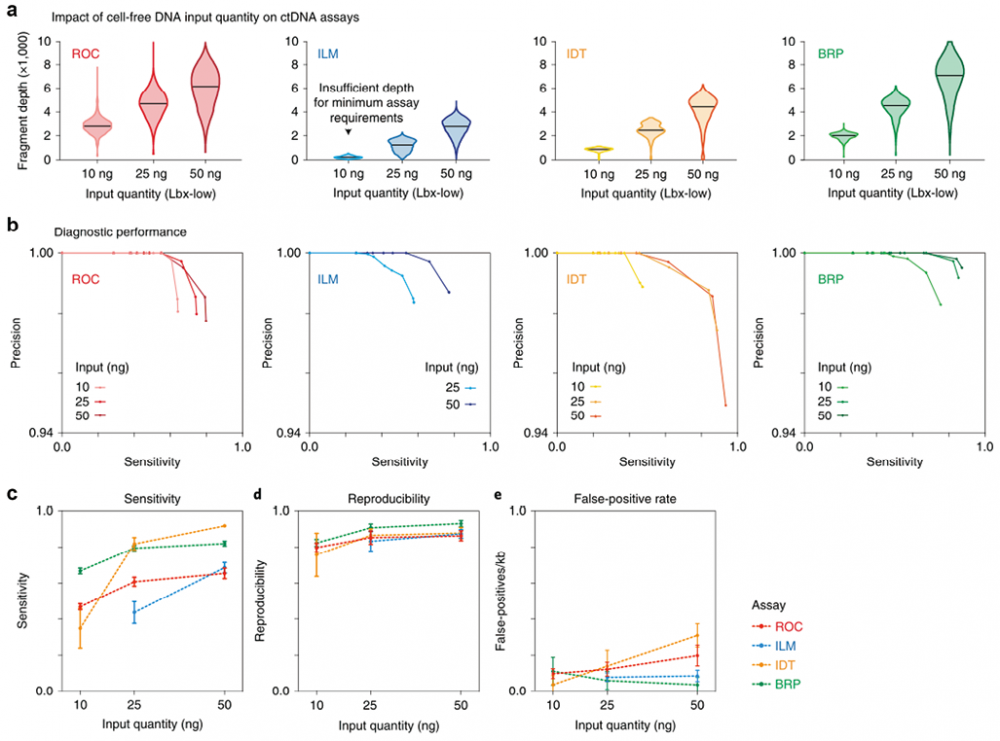
图7. 不同DNA投入量对panel性能的影响
液体活检技术的发展将可以从精准医疗中获益的患者从晚期逐步推进到早期,极大拓展了临床应用场景,同时可以帮助医生进行患者治疗全程管理。然而,从血液中可靠地检测出微量的片段ctDNA仍然是一个主要的技术挑战。SEQC2项目所评估的灵敏度、假阳性率、可重复性等指标让临床可以直观、客观、全面、且定量地感受液体活检技术,为基于NGS的液体活检产品提供判断标准,为ctDNA分析性能的全面评估提供了最佳实践指南。




