我国D-二聚体检测与报告现状调查2023

张李涛,医学硕士,副教授,副主任技师。现任武汉亚心总医院检验科主任。毕业于华中科技大学同济医学院,2019年在英国利物浦大学皇家利物浦医院访问学者,擅长疑难血栓与止血分析和管理。先后主持省自然科学基金课题等9项,近5年以第一作者身份发表论文24篇,SCI收录20篇,2018-2021连续三年获得“最高引用论文”和“最受欢迎论文”证书。2020年入选“武汉中青年医学骨干人才工程”。学术兼职:武汉市非公医疗机构医学检验专委会副主任委员,湖北省医学会检验分会青年委员,武汉医学会检验分会青年委员,《检验医学》杂志青年编委,《血栓与止血杂志》编委。
D-二聚体是交联纤维蛋白被纤溶酶降解的终产物之一,被认为是机体高凝状态和血栓形成的敏感标志物之一,广泛用于深静脉血栓栓塞症(Venous Thromboembolism,VTE)和弥散性血管内凝血(disseminated intravascular coagulation,DIC)等疾病的辅助诊断[1]。近些年,D-二聚体的应用范围不断拓展,其在胸痛鉴别、重症感染和抗凝治疗等领域的应用逐渐引起关注,D-二聚体已成为最受临床重视的实验室检验指标之一[2]。尽管如此,D-二聚体定量检测的标准化工作一直进展缓慢,且由于D-二聚体还存在报告方式、单位、检测平台的差异,导致不同实验室间结果缺乏可比性,此外,随着国产凝血检测设备的广泛应用,D-二聚体检测试剂盒厂家快速增长,这些都为D-二聚体的检测和报告带来不确定性,也造成临床和实验室的诸多困惑和误解。本研究旨在对当前国内D-二聚体的检测和报告情况进行调查研究,并作为《D-二聚体实验室检测与临床应用中国专家共识》的前置背景[3],为更好地推进D-二聚体检测和报告的规范化提供数据支持。
一、调查研究方法
1. 调查方法:本次调查采用微信小程序“问卷星”,通过中国研究型医院协会血栓与止血分会发布调查问卷链接。问卷内容包括13个部分:(1)单位全称;(2)用于D-二聚体检测的主力设备和品牌;(3)用于D-二聚体检测的试剂品牌;(4)所使用的D-二聚体的报告方式;(5)D-二聚体报告单上的参考范围设置;(6)D-二聚体报告的单位;(7)D-二聚体目前使用的参考范围或截断值(cutoff value)来源;(8)是否有计划使用年龄校正的截断值;(9)D-二聚体常规情况下是否与纤维蛋白(原)降解产物(Fibrinogen degraded product,FDP)联合检测;(10)是否只在检验科开展D-二聚体检测;(11)检验科之外开展D-二聚体检测的科室;(12)其他科室所用D-二聚体检测系统与检验科是否相同;(13)其他科室或实验室使用的设备类型。
2. 数据处理方法:对所有在线填写的问卷被直接导入Excel表格进行去重和二次核查,并根据所填写单位全称,对医院的等级和性质进行分类。调查结果描述性统计分析以频率(百分比)表示。
二、调查研究结果
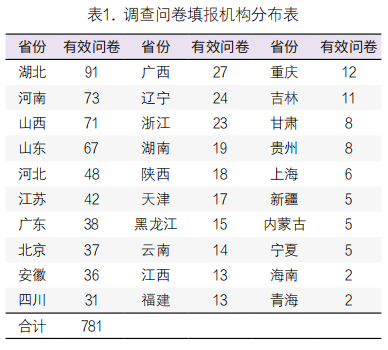
1. 参与机构分布:本研究共收到来自全国30省份医疗机构填报问卷825份(图1),经去重和二次核查后确认有来自781家医疗机构的有效问卷纳入分析,其中三级医疗机构554家,占比70.9%,二级医疗机构191家,占比24.4%,一级医疗机构36家,占比4.6%。
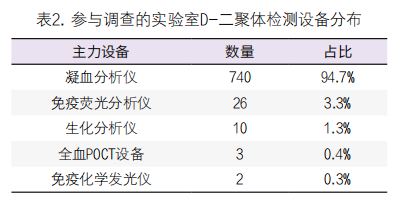
2. 检测方法与平台:在781家医疗机构中,用于D-二聚体检测的设备平台见表2,主力设备以凝血分析仪为主占比达94.8%(740/781),部分实验室选择免疫荧光分析仪(26/781,3.3%)、生化分析仪(10/781,1.3%)、全血POCT设备(3/781,0.4%)、免疫化学发光仪(2/781,0.3%)等平台。其中,82.3%(643/781)的机构使用设备品牌配套的检测试剂盒,17.7%(138/781)的机构使用开放试剂。在所有参与调查的实验室中,93.7%(732/781)实验室使用单一品牌进行D-二聚体检测,另有6.3%(49/781)的实验室使用两种及以上品牌的设备。
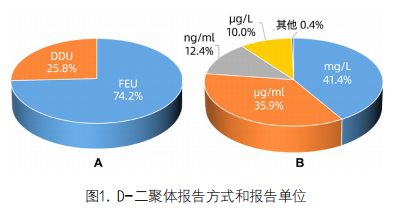
3. 报告方式和报告单位:D-二聚体的报告方式分为二种,FEU单位和DDU单位。本次调查的781家实验室中,74.2%(580/781)的实验室D-二聚体报告方式为FEU,25.8%(201/781)的实验室报告方式为DDU(图1A)。
D-二聚体报告的单位为μg/ml或mg/l的占78.3%,ng/ml或μg/l的占13.4%,mg/ml或g/l的占8.3%(图1B)。36.5%的实验室D-二聚体基本都与FDP联合检测,17.5%的实验室D-二聚体多数情况下与FDP联合检测,16.3%的实验室D-二聚体少数情况下与FDP联合检测,7.7%的实验室D-二聚体基本不与FDP联合检测,22.0%的实验室未开展FDP检测。
4. 参考范围和截断值:在参与调查的机构中,仅11.9%(93/781)的实验室明确区分了正常参考区间和截断值,其余88.1%(688/781)参与调查的实验室D-二聚体报告中提供的“参考范围”,经核实其实是截断值,而非“正常参考区间”。而在这些正常参考区间或截断值中,81.6%来源于试剂说明书,9.4%来源于指南或研究文献,6.5%来源于实验室自建。
对于年龄校正截断值(Age-adjusted cutoff value)的应用方面,5.8%的实验室已开始使用年龄校正截断值,21.8%的实验室了解且计划使用,37.6%的实验室了解但无计划使用,34.8%的实验室不了解。
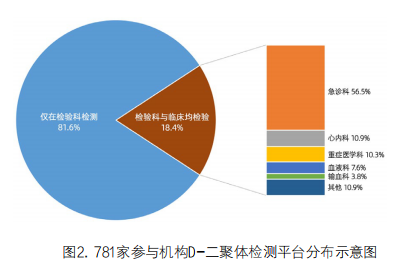
5. 检测实验室分布:参与调查的781家机构中,有18.4%的单位在除检验科以外的其他科室开展D-二聚体检测(图2)。其中以急诊科居多,占56.5%,心内科占10.9%,重症医学科占10.3%,血液科占7.4%。 其他科室用于D-二聚体检测的设备68.1%为全血POCT设备,15.3%为免疫荧光分析仪,5.6%为凝血分析仪,1.4%为生化分析仪。值得注意的是,其他科室用于D-二聚体检测的系统仅6.6%与检验科一致,93.4%的机构与检验科不一致。
三、讨论与分析
本调查发现D-二聚体的检测呈现逐渐向自动化凝血分析仪集中的趋势,本研究发现在凝血分析仪上检测的比例高达94.7%,这一变化与临床诊疗及服务需求的变化密切相关:(1)血栓性疾病的预防和管理越来越受到重视,凝血检测的申请随之增加,实验室逐渐普遍使用全自动凝血分析仪完成凝血检测任务;(2)D-二聚体检测多推荐使用枸橼酸钠抗凝试管采集样本,样本类型与PT、APTT等凝血项目的检测相同,可统一共管在全自动凝血分析仪上检测有助于减少样本周转同步报告结果及减少采血量;(3)自动化凝血分析仪多采用乳胶增强免疫比浊法检测D-二聚体,这种方法与ELISA、免疫荧光等方法学均属于高敏感方法,可满足D-二聚体在不同临床场景中的应用需求。但也应看到,由于D-二聚体在胸痛鉴别中重要的应用价值[4],其在急诊、胸痛中心等场景中的应用需求大幅增加,以全血检测D-二聚体的床旁检验设备占比快速增长。除此之外,还有部分专科实验室也有开展D-二聚体检测,同一个医疗机构使用几种不同方法学检测同一个项目,甚至报告单位不同,应用场景重合的情况可能会给医疗质量增加隐患。这些都为D-二聚体的检测与报告的规范化带来了更多的不确定性。
D-二聚体的检测和报告的规范性亟待改进。国家临床检验中心曾报道国内FEU和DDU的使用比例为3:2[5],与国际上的报道接近[6]。本研究中调查的比例呈现出FEU比例增加的趋势。这一点可能与国产凝血设备的应用及近些年快速上升有关,因为大多数国产D-二聚体检测试剂盒均选择FEU的报告方式;另外,也与近些年国内外VTE管理指南推荐使用年龄校正的截断值有关,因为有关D-二聚体年龄校正截断值的绝大多数研究均是基于FEU的结果,基于DDU的较少。也曾有学者呼吁从指南和学会层面推荐全面使用FEU单位,取消DDU单位,原因是相比于FEU,DDU仅是一种当量单位,并未给D-二聚体带来任何检测性能和临床应用效能的增强,反而由于二种单位的存在,造成D-二聚体结果报告的天然差异[7]。
本研究显示共计77.3%的实验室使用的报告单位为mg/L(等效单位:μg/ml)和ng/ml(μg/L),这些单位间存在的换算关系常给临床和患者带来困扰,甚至同一机构内的不同实验室使用的报告方式和报告单位都会存在差异,为D-二聚体结果的一致性带来更多困难。有多位学者呼吁各级学会应积极促进D-二聚体报告的规范化[6],mg/L具有成为国际标准单位的潜力,笔者团队也曾提出使用D-二聚体比值(D-dimer ratio,DDR)作为现阶段改善D-二聚体报告一致性的措施[7]。
年龄校正截断值近些年越来越被推荐用于VTE的阴性排除,然而从实际调查数据来看,真正能将年龄校正截断值在报告中进行体现的实验室依然很少,大部分实验室并无计划使用,甚至不了解这个概念。这一现象的原因可能跟以下因素有关:(1)临床检测D-二聚体的目的并不全是用于VTE的阴性排除,非此目的的D-二聚体检测申请对年龄校正的截断值的需求并不迫切;(2)多数实验室的实验室信息系统针对设置年龄校正的截断值可能系统架构或技术困难;(3)实验室或临床相关人员缺乏使用年龄校正截断值的意识。
本研究为调查性研究,有几点局限。首先,尽管参与单位来源于全国30个省份有一定的代表性,但参与调查的机构数量偏少可能会造成统计效能的偏倚;其次,本次参与的医疗机构多数为三级医院,而在国内数量更多的一、二级医疗机构参与数量偏少;最后,限于电子问卷调查的特点和参与者对相关问题的回答存在局限,可能会影响统计数据的精确度,但不影响研究结果。
四、结论
本研究主要针对国内医疗机构D-二聚体的检测和报告现状进行了随机问卷调研,发现D-二聚体检测呈现方法学集中化,检测分布分散化的趋势;D-二聚体报告的规范化亟待改善,为进一步规范D-二聚体的检测与应用提供了证据支持。
参考文献
Olson JD.D-dimer: An Overview of Hemostasis and Fibrinolysis, Assays, and Clinical Applications. Adv Clin Chem, 2015. 69: p. 1-46.
Zhang L. Use of D-dimer in oral anticoagulation therapy. Int J Lab Hematol, 2018. 40(5): p. 503-507.
中国研究型医院学会血栓与止血专业委员会, D-二聚体实验室检测与临床应用中国专家共识. 中华医学杂志, 2023. 103(35): p. 2743-2756.
急诊胸痛心血管标志物联合检测共识专家组 and 中国医疗保健国际交流促进会急诊医学分会, 急诊胸痛心血管标志物检测专家共识. 中华急诊医学杂志, 2022. 31(04): p. 448-458.
彭明婷. D-二聚体实验室检测现状与规范化 %J 中华医学杂志. 2015(34): p. 2740-2743.
Lippi G. International survey on D-dimer test reporting: a call for standardization. Semin Thromb Hemost, 2015. 41(3): p. 287-93.
Zhang L, Zhang Z. Standardization of D-dimer reporting in the COVID-19 era. Res Pract Thromb Haemost, 2022. 6(6): p. e12772.




