新一代多靶点粪便DNA检测在结直肠癌筛查中的应用价值
【摘要】目的 研究者开发了新一代多靶点粪便DNA检测,包括DNA分子标记物和血红蛋白水平的评估,以提高结直肠癌筛查的性能(主要是在特异性方面)。方法 在一项前瞻性研究中,我们在接受结肠镜筛查的≥40岁无症状成人中评估了新一代多靶点粪便DNA检测方法。主要目标是评估该检测方法对结直肠癌的灵敏度和对晚期肿瘤(结直肠癌或晚期癌前病变)的特异性。晚期癌前病变包括一处或多处腺瘤或无蒂锯齿状病变(最长部分至少为1cm)、具有绒毛状组织特点的病变以及高度的不典型增生。次要目标是量化晚期癌前病变的灵敏度和对非肿瘤发现或结肠镜检查阴性的特异性,以及比较多靶点粪便DNA检测和市售粪便免疫化学检测(FIT)对结直肠癌和晚期癌前病变的灵敏度。结果 在20,176例参与者中,98例患有结直肠癌,2,144例患有晚期癌前病变,6,973例患有非晚期腺瘤,10,961例为非肿瘤性发现或结肠镜检查阴性。在新一代检测中,对结直肠癌的灵敏度为93.9%(95%置信区间[CI],87.1-97.7),对晚期肿瘤的特异性为90.6%(95% CI,90.1-91.0)。对晚期癌前病变的灵敏度为43.4%(95%CI,41.3-45.6),对非肿瘤性或结肠镜检查阴性的特异性为92.7%(95%CI,92.2-93.1)。FIT对结直肠癌的灵敏度为67.3%(95%CI,57.1-76.5),对晚期癌前病变的灵敏度为23.3%(95%CI,21.5-25.2);晚期肿瘤的特异性为94.8%(95%CI,94.4-95.1),非肿瘤性检查或结肠镜检查阴性的特异性为95.7%(95%CI,95.3-96.1)。这与FIT相比,新一代检测对结直肠癌和晚期癌前病变具有较高的灵敏度(P<0.001),但对晚期肿瘤的特异性较低(P<0.01),未发生不良事件。结论 新一代多靶点粪便DNA检测对结直肠癌和晚期癌前病变的灵敏度高于FIT,但特异性较低。
在美国,每年有153,000人被诊断为结直肠癌,是癌症相关死亡的第二大常见原因,美国预防服务工作组(USPSTF)和美国癌症协会(American Cancer Society)建议对处于一般风险的45-75岁成人进行结直肠癌筛查,尽管结直肠癌筛查在降低结直肠癌发病率和相关死亡率方面有效,但2021年筛查依从性略低于60%,低于美国国家结直肠癌圆桌会议制定的80%的目标。在一种包括DNA分子标志物和血红蛋白水平评估的无创性粪便多靶点DNA检测法于2014年获得美国食品药品监督管理局(FDA)批准,并被纳入针对一般风险人群的结直肠癌筛查指南。在多靶点粪便DNA检测法的最初试验中,结直肠癌和晚期癌前病变的检出率显著高于对照的粪便免疫化学检测法(FIT),但特异性较低。为了提高特异性并减少假阳性结果的发生,同时保持或提高灵敏度,我们开发了新一代多靶点粪便DNA检测法。在当前的BLUE-C研究中,我们评估了新一代检测法的性能特征,主要目标是确定该检测对结直肠癌的灵敏度和对晚期肿瘤的特异性,次要目标包括对晚期癌前病变的灵敏度和对非肿瘤性发现或结肠镜检查阴性的特异性进行量化,并将检测结果与市售FIT的结果进行比较。
一、研究对象与方法
1. 研究设计和监督:在美国186个研究中心开展了这项研究,研究方案(与本文全文可在NEJM.o rg获取)在各研究中心由中央或当地机构审查委员会的酌情批准,所有参与者均提供了书面知情同意。本研究按照《涉及人类受试者的生物医学研究国际伦理准则》、《赫尔辛基宣言》和《药物临床试验质量管理规范》的原则进行。这项研究由Exact Sciences资助,由赞助商和作者设计,数据收集和监测由独立的临床研究组织ICON进行。
2. 研究人群:研究人群包括年龄≥40岁、安排进行或计划接受结肠镜筛查的无症状者。排除了结直肠癌或晚期癌前病变病史;家族性腺瘤性息肉病、遗传性非息肉病性结直肠癌或其他遗传性癌症的病史或家族史;炎症性肠病或Cronkhite-Canada综合征;在之前2年内,第一代多靶点粪便DNA检测结果呈阳性或者在之前6个月内,FIT或粪便隐血检测结果呈阳性;在过去9年内接受过结肠镜检查或在过去30天内有直肠出血的患者。根据2020年人口普查结果,将研究对象的人口特征与美国人口特征进行了比较,从而评估了试验对象在年龄、性别、种族和民族群体方面的代表性。
3. 临床程序:在结肠镜检查之前获得用于新一代多靶点粪便DNA检测和FIT的粪便样本,邮寄并在收到时检查是否可接受。记录样本采集过程中发生的不良事件。可能发生的事件包括手腕扭伤,在打开试剂盒、获取样本或准备装运粪便样本时发生轻微割伤或受伤以及意外接触到防腐缓冲溶液。在各研究中心,根据标准治疗进行结肠镜筛查。所有提交的组织样本(包括所有结直肠癌和晚期癌前病变)以及结肠镜检查报告、组织病理学报告、结肠镜检查后的相关随访程序或癌症相关成像报告等信息均由至少一名独立病理学专家集中审核,并被视为参考标准,中心实验室的内镜医生和病理学医生不知道多靶点粪便DNA检测和FIT的结果。对于每名参与者,根据检出的最具临床意义病变的组织病理学诊断对结肠镜检查结果进行了分类(可在NEJM. org获取),结肠镜检查的肠道准备被评为优秀,良好,一般或差。如果记录了盲肠插管,并且肠道准备的质量被评为一般或良好,则结肠镜检查被认为是完整的,可用于研究目的。结肠镜检查发现结直肠癌或晚期癌前病变的,无论是否存在任何限制因素,均被视为完整的结肠镜检查。可评估的结肠镜检查的定义为在获得粪便样本后180日内进行的完整结肠镜检查,我们收集了结肠镜检查中切除的组织的组织病理学信息,并用于确定最新的发现。
4. 主要与次要目标:主要目标是多靶点粪便DNA检测对结直肠癌的灵敏度(检测结果呈阳性的结直肠癌参与者的比例)和对晚期肿瘤(结直肠癌或晚期癌前病变)的特异性(检测结果呈阴性的未患晚期肿瘤参与者的比例)。晚期癌前病变包括腺瘤和最长尺寸至少1cm的无蒂锯齿状病变(包括大的增生性息肉)、具有绒毛状组织学特征的病变和高度不典型增生。次要目标包括对晚期癌前病变的灵敏度、对非肿瘤性发现或结肠镜检查阴性的特异性,以及多靶点粪便DNA检测与商用FIT检测对结直肠癌和晚期癌前病变灵敏度的比较。其他预设目标包括以下内容:根据癌症分期(根据美国癌症联合委员会分期系统划分为I至IV期)、病变位置(结肠或直肠近端或远端,见下文)、病变大小、晚期癌前病变类型进行亚组分析、根据参与者年龄进行特异性分析、根据非肿瘤性检查结果或结肠镜检查呈阴性的参与者进行亚组分析、结肠镜检查呈阴性的参与者进行特异性分析、新一代粪便多靶点DNA检测与FIT的受试者工作特征(ROC)曲线以及下一代多靶点粪便DNA检测与固定特异性FIT的比较。近端结肠包括盲肠、升结肠、肝曲、横结肠、脾曲,“右半结肠”所述的任何部分或者插入深度超过60cm的区域。远端结肠包括降结肠、乙状结肠、直肠乙状结肠,“左半结肠”所述的任何部分或插入深度为16-60cm的区域。直肠包括插入深度为0-15cm的区域。
5. 实验室程序:新一代多靶点粪便DNA测试在赞助商的实验室进行,FIT由一个单独的中央实验室(分子病理学实验室网络)进行。简单来说,新一代检验纳入了一个新的分子面板(panel,包括甲基化的DNA标志物神经酰胺合酶4基因[LASS4]、富含亮氨酸重复序列蛋白4基因[LRRC4]、丝氨酸-苏氨酸蛋白磷酸酶2A 56-kDa调节亚基γ亚型基因[PPP2R5C]和参考标志物含锌指DHHC型1基因[ZDHHC1],同时保留了粪便血红蛋白)。新的生物标志物panel、新一代算法以及用于DNA检测的粪便收集和处理的详细信息见图S1。技术人员不知道结肠镜检查和替代检查的结果。根据制造商的说明书操作商品化FIT(OC-AUTO FIT,Polymedco),血红蛋白水平超过100ng/ml缓冲液(>20μg/g粪便)的粪便样本被视为FIT阳性,在算法和临床数据库锁定之前,赞助商不知晓结果。
6. 统计学分析:计算得出,纳入至少71例结直肠癌参与者将为本研究提供至少90%的统计学功效来评估关于结直肠癌灵敏度的假设。主要和次要分析是基于获得的所有数据,未对缺失数据进行估算,主要有效人群包括符合纳入标准,并且进行有效的新一代多靶点粪便DNA检测和可评估的结肠镜检查的所有纳入参与者。比较效果人群包括主要效果人群中有效FIT的所有参与者,由于主要效果人群中只有32例参与者被排除出比较效果人群,因此本文仅给出比较效果人群的结果。对所有研究对象进行多重插补法分析,以评估缺失数据的潜在偏倚。本研究有2个预设的主要假设和4个预设的次要假设,主要假设检测了新一代多靶点粪便DNA检测对结直肠癌的灵敏度,反对75%的无效假设(零假设),并检测对晚期肿瘤的特异性,反对85.9%的无效假设。次要假设检测了新一代多靶点粪便DNA检测对晚期癌前病变的灵敏度,反对38.9%的无效假设,在对结直肠癌和晚期癌前病变的灵敏度以及对非肿瘤性发现或阴性结肠镜检查的特异性方面,新一代检测方法优于商品化FIT,反对87.5%的无效假设。
为了将总体I型误差控制在2.5%的单侧α水平,必须拒绝两个主要无效假设,才能宣布研究成功并进行次要假设检验。对于次要假设,采用了以下预先指定检验顺序的分层检验策略来控制I型误差:新一代多靶点粪便检测法对结直肠癌的灵敏度必须高于FIT,新一代检测法对晚期癌前病变的灵敏度必须高于FIT,新一代检测法对晚期癌前病变的灵敏度必须大于38.9%,新一代检测法对非肿瘤性发现或结肠镜检查阴性的特异度必须大于87.5%。在2.5%的单侧显著性水平,通过精确McNemar检验比较了新一代检测和FIT对结直肠癌和高级别癌前病变的灵敏度,还比较了新一代检测法和FIT对晚期肿瘤的特异性,因为开发新一代检测法的目的是特异性方面的改善。除主要和次要结果外,其他结果的置信区间未进行多重性调整,因此不能用于推断效果。补充附录中提供了主要、次要假设检验和插补分析的详细信息,所有统计分析均使用SAS软件9.4版(SAS Institute)进行。
二、研究结果
1. 研究人群:本研究于2019年11月15日至2023年1月5日进行,在纳入的26,758例参与者中,20,176例(75.4%)的结果可用于全面评估(比较效果人群),最常见的排除原因包括结肠镜筛查不完整(2,218例[8.3%])、粪便样本无法按照研究方案使用(851例[3.2%])和未收到粪便样本(832例[3.1%])。可评估样本的参与者平均年龄为 63.0岁,53.2%的参与者为女性,60.1%为白人,研究人群基本代表了美国符合筛查条件人群的种族和民族分布情况。在结果可用于全面评估的20,176例参与者中,98例(0.5%)被检出结直肠癌,其中82例(84%)为I期、II期或III期,2,144例晚期癌前病变(10.6%),6,973例非晚期腺瘤(34.6%),3,451例非肿瘤性发现(17.1%),7,510例结肠镜检查结果为阴性(37.2%),多靶点粪便DNA测试或FIT的粪便收集过程均未报告不良事件。
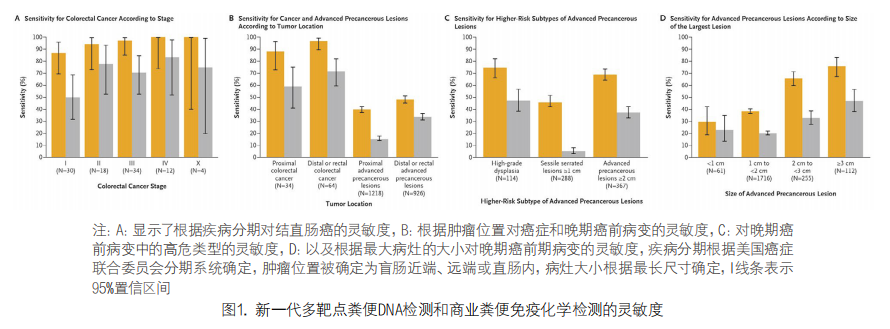
2. 新一代检测的特点:在考虑到多重性的预设假设检验策略下,所有主要和次要无效假设均被拒绝,这里的结果是根据临床类别(灵敏度,然后是特异性)给出的,而不是根据统计学检验的顺序给出的,在99.5%的可用样本(24,354/24,477)中,新一代检测得到了有效结果。新一代多靶点粪便DNA检测发现了,98例结直肠癌参与者中的92例,82例筛查相关癌症参与者中的76例(I、II或III期),检测灵敏度分别为93.9%(95% CI,87.1-97.7)和 92.7%(95% CI,84.8-97.3)(表1)。灵敏度没有因疾病分期或部位的不同而有显著差异(图1A和1B),根据癌前病变亚型和病变大小定义的亚组灵敏度见图1C和1D。在2,144例有晚期癌前病变的参与者中,931例的新一代多靶点粪便DNA检测结果为阳性,灵敏度为43.4%(95% CI,41.3-45.6)。在<65岁的参与者和≥65岁的参与者中,结直肠癌的灵敏度分别为93.3%(95% CI,81.7-98.6)和94.3%(95% CI,84.3-98.8)。在这些亚组中,对晚期癌前病变的灵敏度分别为39.6%(95% CI,36.6-42.6)和47.0%(95% CI,44.1-50.0)。新一代检测方法对结直肠癌和晚期癌前病变的灵敏度在各年龄组中一致,在有一级亲属患结直肠癌的参与者和无一级亲属患结直肠癌的参与者中,对结直肠癌和晚期癌前病变的灵敏度相似。
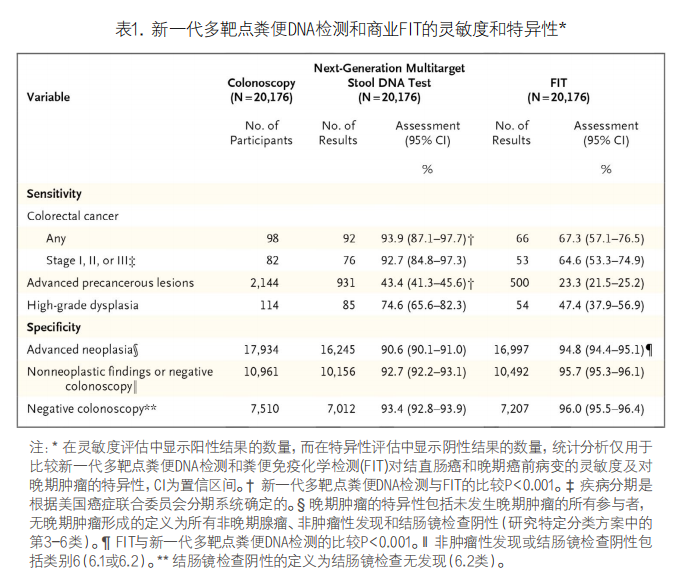
在非结直肠癌或晚期癌前病变(即无晚期肿瘤)的17,934名参与者中,新一代多靶点粪便DNA检测的特异性为90.6%(95% CI,90.1-91.0)。在10,961名非肿瘤性检查结果或结肠镜检查阴性的参与者中,特异性为92.7%(95% CI,92.2-93.1),在7,510名结肠镜检查呈阴性的参与者中特异性为93.4%(95% CI,92.8-93.9)(见表1)。在<65岁的参与者和≥65岁的参与者中,晚期肿瘤的特异性分别为92.7%(95% CI,92.1-93.2)和88.2%(95% CI,87.5-88.9)。在根据5年年龄区间进行的分析中,45-49岁参与者的特异性为97.3%(95% CI,94.8-98.8),50-54岁参与者为95.9%(95% CI,94.8-96.9),70-75岁参与者为87.0%(95% CI,85.7-88.3),≥76岁参与者为84.6%(95% CI,81.7-87.2),在有一级亲属患结直肠癌和无一级亲属患结直肠癌的参与者中,特异性相似。对于观察到的0.5%的结直肠癌患病率,结直肠癌阳性预测值为3.4%(95% CI,2.7-4.1),阴性预测值为99.97%(95% CI,99.93-99.99)。对于11.1%的晚期肿瘤患病率,晚期肿瘤的阳性预测值为37.7%(95% CI,35.9-39.6),阴性预测值为93.0%(95% CI,92.6-93.4)。在多靶点粪便DNA检测结果阳性的参与者中,3.4%被检出结直肠癌,34.3%被检出晚期癌前病变,32.6%被检出非晚期腺瘤,29.7%未发现结直肠癌。结直肠癌的阳性似然比为7.19(95% CI,6.75-7.64),阴性似然比为0.07(95% CI,0.02-0.13)。晚期肿瘤的阳性似然比为4.84(95% CI,4.53-5.16),阴性似然比为0.60(95% CI,0.58-0.62)。
3. 新一代检测与FIT的比较:在检测结直肠癌和晚期癌前病变方面,新一代多靶点粪便DNA检测的灵敏度高于FIT(两种比较均P<0.001)。FIT检测出了98例结直肠癌中的66例(67.3%;95% CI,57.1-76.5)和2,144例晚期癌前病变中的500例(23.3%;95% CI,21.5-25.2)(见表1)。在新一代检测的特异性固定为90.6%时,FIT对结直肠癌的灵敏度为75.5%(95% CI, 65.8-83.6),对晚期癌前病变的灵敏度为31.8%(95% CI,29.8-33.8),两种估计值均低于新一代多靶点粪便DNA检测的估计值。新一代检测的灵敏度性在检测I至III期癌症结直肠癌(92.7% vs 64.6%)、近端结直肠癌(88.2%对58.8%)和远端结直肠癌(96.9% vs 71.9%)以及晚期癌前病变的高危亚型(包括无蒂锯齿状病变[45.8% vs 5.2%]和最长尺寸为1-3cm或更长的晚期癌前病灶)方面,似乎高于FIT(见表1和图1)。在FIT未能检出的32例结直肠癌中,新一代多靶点粪便DNA检测结果为阳性的有26例(81%),在29例与筛查相关的结直肠癌中的23例(79%)和1,644例晚期癌前病变中的555例(33.8%)。FIT对新一代检测未发现的结直肠癌均未呈阳性,对新一代检测未发现的1,213例晚期癌前病变中的124例(10.2%)呈阳性。
FIT对晚期肿瘤的特异性为94.8%(95% CI,94.4-95.1),优于新一代多靶点粪便DNA检测的结果(P<0.001)(表1),FIT对非肿瘤性结果或结肠镜检查阴性的特异性为95.7%(95% CI,95.3-96.1),对结肠镜检测阴性的特异性则为96.0%(95% CI:95.5-96.4)(表1)。各年龄组的FIT特异性始终很高,就结直肠癌的灵敏度而言,新一代多靶点粪便DNA检测的ROC曲线下面积在结直肠癌的灵敏度和晚期肿瘤的特异度(0.98 vs 0.85)以及在晚期结直肠癌的灵敏度和晚期肿瘤的特异度(0.76 vs 0.65),均大于FIT。对所有参与者进行的多重插补分析得出的结果与具有可评估样本的参与者的结果一致。在这些分析中,新一代多靶点粪便DNA检测法对结直肠癌的灵敏度为93.7%(95% CI,89.4-97.9),FIT为65.2%(95% CI, 56.6-73.9)。新一代检测法和FIT法对晚期癌前病变的灵敏度分别为43.3%(95% CI,41.2-45.5)和23.9%(95% CI,21.1-25.8),新一代检测法和FIT法对晚期肿瘤的特异度分别为90.6%(95% CI,90.2-91.0)和94.6%(95% CI,94.3-94.9)。
三、讨论与分析
在美国对结直肠癌筛查的依从性远低于80%的全国目标,而无创筛查可提高筛查依从性,在这项纳入20,000多名参与者的前瞻性研究中,我们评估了新一代多靶点粪便DNA检测法,发现该检测法对结直肠癌的灵敏度为93.9%,对晚期肿瘤的特异度为90.6%,与FIT比较,粪便DNA检测的灵敏度较高,但特异度较低。
这些结果是通过在病例对照数据集的基础上识别出最具鉴别性的结直肠癌和晚期癌前病变分子标志物的系统性过程获得的,随后进行了严格的算法开发,我们在确定了多靶点粪便DNA检测特征的研究中,使用锁定算法对大样本进行了新标志物的初步检测,以在启动当前研究分析之前对算法进行独立验证。提高粪便多靶点DNA检测法的特异性是设计和评估新一代检测法的主要目标,在一项回顾性分析中,我们在先前临床试验前瞻性采集的7,662份存档样本中比较了当前和新一代粪便多靶点DNA检测法,结果显示新一代检测法对晚期肿瘤的特异度为88.5%,当前检测法为86.9%,两种检测法对结直肠癌的灵敏度分别为93.0%,对晚期癌前病变的灵敏度分别为48.4%和41.2%。在筛查患病率低的情况下,特异性是阳性检测结果的主要驱动因素,所以需要高特异性的无创检测方法以减少不必要的结肠镜检查数量以及相关的筛查直接和间接成本。
这与当前版本的多靶点粪便DNA检测一样,新一代检测的特异性与年龄相关,而FIT未观察到这一情况。在70-75岁和≥76岁的参与者中,新一代检测法对晚期肿瘤的特异性分别为87.0%和84.6%,因假阳性结果接受结肠镜检查的老年人发生结肠镜检查并发症的风险高于平均水平,相反,在较年轻的参与者中,我们观察到新一代检测法的特异性较高(在45-49岁的参与者中为97.3%,在50-54岁的参与者中为95.9%),并且结果与FIT的结果相似。新一代多靶点粪便DNA检测包括新的生物标志物,其目的是在不降低灵敏度的情况下提高特异性,新一代检测方法对结直肠癌的灵敏度为93.9%,对晚期癌前病变的灵敏度为43.4%,可治愈期(I、II或III)结直肠癌的灵敏度为92.7%。在之前一项对当前版本检测进行的研究中,对结直肠癌的灵敏度为92.3%(95% CI, 83.0-97.5),对晚期癌前病变的灵敏度为42.4%(95% CI,38.9-46.0),对晚期肿瘤的特异度为86.6%(95% CI,85.9-87.2),本研究未直接比较两种检测方法,两项研究之间不应进行直接比较。比较FIT对结直肠癌和晚期癌前病变的灵敏度(分别为67.3%和23.3%),新一代多靶点DNA检测的相应灵敏度显著更高(93.9%和43.4%)。对结直肠内病变的位置,新一代检测对近端和远端结直肠癌的灵敏度(分别为88.2%和96.9%)也高于FIT(分别为58.8%和71.9%)。对于晚期癌前病变也观察到类似的趋势,对于高度不典型增生、无蒂锯齿状病变和其他亚型,新一代检测显示出比FIT更高的灵敏度,FIT对晚期肿瘤的特异性(94.8%)高于新一代多靶点粪便DNA检测(90.6%)。
本研究的优势之一是参与者人群庞大且多样化,虽然为了识别足够多的结直肠癌,本研究对老年人群进行了丰富分析,但该人群通常代表美国符合筛查条件的人种和民族。本研究的样本量对结直肠癌的灵敏度以及根据大小、组织学特征和部位对晚期癌前病变亚组的灵敏度提供了合理精确的估计,大样本量还使我们能够对最具临床意义的检查结果类别和各年龄组的特异性进行精确估计,后者的结果显示,特异性随着年龄的增加而预期降低。本研究的另一个优势是对所有结直肠癌的组织学特征和疾病分期进行了集中、盲法判断,这确保了诊断的准确性,从而可以评估下一代多靶点粪便DNA检测和市售FIT的性能。这项研究的一个局限性是,提供知情同意书并被纳入研究但其样本无法根据方案进行评估的人数比例相对较高。可能是在2019冠状病毒病大流行期间进行的研究,这可能影响了登记和结肠镜检查的机会。对所有参与者进行的多重插补分析显示,结果与具有可评估样本的参与者群体的结果一致。另一个局限性是没有直接比较新一代多靶点粪便DNA检测法与当前版本的多靶点粪便DNA检测法的性能,因此,本研究的结果无法与已发表的用于筛查的粪便多靶点DNA检测结果进行可靠性比较,而有效的比较需要在筛查的背景下,同时对同一人和样本的两种检测进行评估。
在本研究中,我们发现新一代多靶点粪便DNA检测对结直肠癌的灵敏度为93.9%,对晚期癌前病变的灵敏度为43.4%,对晚期肿瘤的特异性为90.6%。对于所有与筛查相关的病变,这种新版本的检测比商业化FIT更敏感,但FIT的特异性更高。
编译节选自:《N Engl J Med》2024;390:984-93.




