患者的低钾血症和低氧血症原因分析
一、病例介绍
患者,女,72岁,因营养不良和嗜睡2个月就诊。无呕吐或腹泻史,未服用任何药物。入院时,体温37.2℃,血压110/73mmHg,脉搏111次/分钟,呼吸频率19次/分钟,常态下的血氧饱和度为98%。心电图未见传导异常。心血管和呼吸系统未见异常,腹部检查未发现肝脾肿大。血液检查显示白细胞增多,伴有贫血、血小板减少和严重低钾血症(表1)。免疫细胞化学证实急性髓系白血病,原始细胞占93%。其他血液异常结果包括高尿酸血症、乳酸脱氢酶升高、肌酐升高,总蛋白和白蛋白降低(表1)。开始接受静脉补钾治疗(24小时内给予40mmol),以1000ml 0.9%氯化钠溶液稀释,并口服羟基脲(首次剂量500mg,之后每日一次1g)。治疗后24小时再次测定的血钾浓度(表1)反而较前更低。随后采集动脉血液样本,快速进行血气分析[血液收集在血气注射器中,置于冰上,即时(POC)血气分析仪(ABL90 Flex分析仪,Radiometer)],测得的血钾水平为2.9mmol/L,较之前有所提高。
住院期间,患者出现高烧,体温39.4℃。对此,医生申请血培养和药敏测试、动脉血气测量(表1)和胸部X光检查。血气样本在冰镇状态运输并行即时分析。发现动脉氧分压(PO2)和动脉氧饱和度(SaO2)与胸部X光检查结果及通过呼吸机工作站测量的外周血氧饱和度存在差异(表1)。但患者并未表现出任何呼吸困难或发绀症状。
血培养最终证实为链球菌属导致的脓毒血症。尽管已开始使用静脉注射哌拉西林和他唑巴坦(每6小时4.g,Tazocin EF)、退热支持治疗—对乙酰氨基酚(每6小时1g)以及口服钾补充剂(每8小时16mmol),患者的病情仍持续恶化,并在入院第3天去世。
需要考虑的问题

二、讨论与分析
患者出现高尿酸血症和乳酸脱氢酶升高(表1)是由于细胞周转率高,而肌酐升高则反映肾脏功能受损,可能是由白血病细胞浸润或尿酸性肾病引起。增殖的恶性细胞过度消耗磷导致低磷血症的发生。总蛋白和白蛋白降低与营养不良状况相符。低白蛋白血症也可能是因为机体的应急性反应。血清镁浓度正常排除了低镁血症引起的低血钾。
1. 白血病中的低钾血症和假性低钾血症:高白细胞计数(Hyperleukocytosis),即白细胞(WBC)计数>100×109/L,见于30%到40%的急性白血病患者中。具有单核细胞分化的急性髓系白血病患者的低钾血症可能是溶菌尿症(lysozymuria)的结果,这是一种罕见的副肿瘤综合征。在这种情况下,大量溶菌酶被释放到血液循环中,经肾小球过滤后被近端肾小管重吸收。从而导致中毒性肾小管损伤,使肾小管对钾的排泄增加(2)。使用化疗药物如顺铂、袢利尿剂或氨基糖苷类药物是白血病患者肾性失钾的另一个原因。假性低钾血症,定义为血液中钾的虚假减少,可能出现在送检延迟的白细胞增多症血液样本中,不应将其误认为真正的低钾血症。与正常的白细胞相比,白血病白细胞具有增强的钠-钾泵活性,导致体外实验中钾从血浆中移入白细胞内,从而降低血浆中的钾活性(见图1)。本文中的患者可能由于长时间的饮食摄入不足而出现了轻度低钾血症。该患者出现的高白细胞计数是导致钾从细胞外向细胞内转移的关键因素,这种转移即使在抽血后仍继续进行,从而导致假性低钾血症。实际上的体内低钾血症与假性低钾血症的结合,使得测得的钾值低于体内实际的钾浓度。然而,需要注意的是,极端的白细胞增多并不一定会导致假性低钾血症,因为文献中也有报道由于白细胞脆弱性和溶解而导致的假性高钾血症。
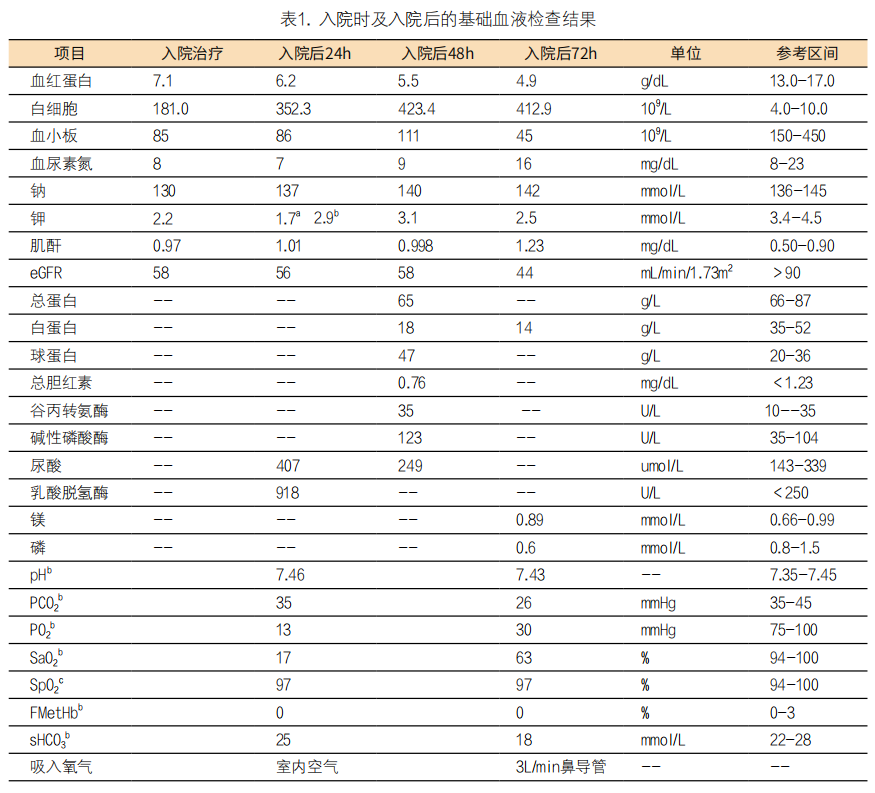
注:换算系数:血尿素氮(mg/dL)×0.357=尿素(mmol/L);肌酐(mg/dL)×88.42=肌酐(μmol/L);胆红素(mg/dL)×17.1=胆红素(μmol/L);尿酸(μmol/L)×0.02=尿酸(mg/dL)。eGFR:基于慢性肾脏病流行病学协作组估算的肾小球滤过率;PCO2:动脉二氧化碳分压;SpO2:外周氧饱和度;FMetHb:高铁血红蛋白比例;sHCO3:标准碳酸氢盐。
注释:a 样本在室温下运送至实验室分析仪(Cobas 6000自动分析仪)(从采血到分析的时间约为60分钟)。 b 样本在冰水中运送至即时分析仪(ABL90 Flex分析仪)(从采血到分析的时间约为15分钟)。 c 通过呼吸工作站或脉搏血氧仪(Carescape V100)获得的读数。
假性低钾血症如果未被识别,可能会导致有害后果。不必要的钾补充可能导致心室颤动和心脏节律失常。对于高白细胞计数的患者,立即测试全血(如通过床边检测仪POC analyzer)样本是获得体内钾水平最准确预测的理想方法,因为它减少了体外细胞内钾转移的时间。然而,如果条件不许可,快速分离出血浆/血清,或在预分析阶段使用冰来降低钠-钾ATP酶泵的活性,也可能有助于提供更符合生理的结果。虽然床边检测(POC)使血钾分析能够实现即时检测,但也存在体外溶血而忽略的风险,这可能会掩盖真实的低钾血症。体外溶血会导致红细胞破裂,释放出细胞内的钾,从而使血浆中的钾浓度升高,从而影响检测结果的准确性。因此,在使用POC设备进行钾分析时,应特别注意确保样本没有发生溶血,以避免误诊。
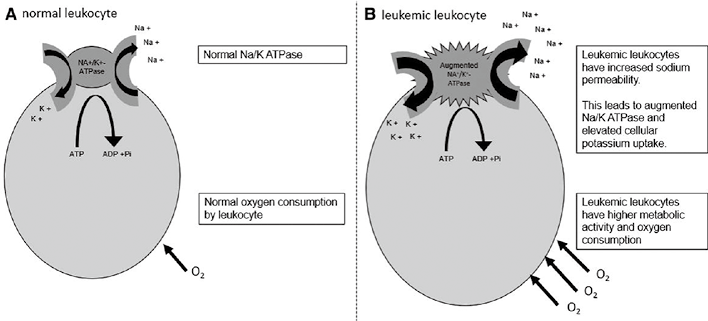
注:(A)正常白细胞在体外维持常规代谢活动;(B)当白血病白细胞中Na+/K+-ATP酶活性增加导致细胞内钾转移增加时,体外血浆钾活性降低,从而发生假性低钾血症。假性低氧血症则是由于大量代谢活跃的白血病白细胞在体外消耗过多氧气所致。Na+/K+-ATP酶,钠钾腺苷三磷酸酶;ATP,腺苷三磷酸;Pi,无机磷酸;O2,氧气。
图1. 白细胞增多症中假性低钾血症和假性低氧血症的机制
2. 白细胞增多引起的假性低氧血症:白细胞增多症使患者面临真性和假性低氧血症的风险。真性低氧血症表现为肺炎、肺栓塞或肺白细胞淤积引起的通气-灌注失调,而假性低氧血症则是由于白细胞在体外消耗氧气所致(见图1)。白细胞的代谢活性是血小板的45倍,几乎占用了血液中所有的氧气,而成熟的红细胞则几乎没有氧气消耗(7)。在血细胞计数正常的情况下,即使从全身循环中移除,代谢活跃的血细胞在室温下储存20分钟后,仍可导致氧分压轻微下降(约8mmHg)。相比之下,白血病患者体内大量的白细胞导致更高的呼吸氧消耗,因此在体外氧分压会有更大的下降,这一现象被称为“氧窃取”或“白细胞盗窃”。氧消耗与白细胞计数的增加成正比,这一点通过治疗后白血病负担消失时假性低氧血症得以解决得到了证实。除了白细胞计数外,白细胞增多症中的氧消耗还取决于白细胞亚型及其成熟阶段。例如,单核细胞在所有细胞类型中消耗最多的氧气,其次是粒细胞和淋巴细胞(6),而幼稚细胞如白血病原始细胞由于钠钾泵活性增加,比成熟白细胞消耗更多的氧气。
评估假性低氧血症应首先考虑常见的前分析原因,如静脉采样错误、样本分析延迟以及通过气动管输送血气样本等问题。一种可靠检测假性低氧血症的方法是将通过脉搏血氧仪获得的外周血氧饱和度值与血气分析仪测得的PO2和SaO2值进行比较。血气分析仪通常通过计算(根据测量的PO2使用‘氧解离曲线’得出)或直接测量(光谱分析)来产生SaO2结果。许多现代血气分析仪,包括本例患者测试使用的仪器,采用后者方法,即通过测量溶血的动脉血样本在多个波长下的吸光度来确定SaO2。脉搏血氧仪通过测量两个对应于氧合血红蛋白和脱氧血红蛋白的波长下的动脉血光吸收来产生外周血氧饱和度结果。当机体周围循环受损、皮肤变色、碳氧血红蛋白升高和高铁血红蛋白水平升高时,脉搏血氧仪的测量结果可能不可靠。然而,在白细胞增多症患者中,脉搏血氧测定更能准确反映体内血氧饱和度,因为其不受白血病细胞体外耗氧的影响。
由于PO2是评估呼吸窘迫综合征的主要标准之一,未被识别的假性低氧血症可能会引发机械通气的不当使用,最终使患者面临额外的肺部氧中毒风险。许多旨在最小化假性低氧血症的方法的基本原理是减少白细胞在体外的代谢活动,从而降低氧气消耗。使用预冷的注射器和缩短采血与样本分析之间的时间间隔是文献中广泛描述的两种方法。然而,尽管我们的案例中采用了冰镇运输血气样本和使用床旁分析仪以尽量减少分析延迟,但仍存在假性低氧血症。这可能如Louw等人的一项研究指出,在室温下短短几分钟内PO2读数就会显著下降。研究还显示,白细胞在样本冷却期间可能继续消耗氧气,并且即使细胞代谢率下降,这种消耗也可能以加速的方式持续进行。第三种方法是使用如氰化钾和氟化钠之类的添加剂来减缓白细胞的代谢活动,防止细胞摄取葡萄糖和氧气。然而,这种方法不仅成本高昂,而且在日常实践中实施起来技术上也具有挑战性。此外,由于氟化钠具有酶抑制作用,不适合全自动化学分析仪测试多数项目。氟化管还可能导致红细胞内的有机磷酸盐耗尽,并改变细胞膜的通透性,最终导致溶血,影响电解质定量。
三、结论
对于白细胞增多症患者,若出现严重的低钾血症但没有临床或心电图变化,以及脉搏血氧仪测试血氧饱和度不符合动脉低氧血症和/或无肺部疾病的情况下,提示可能存在假性低钾血症和假性低氧血症。缩短采血与分析之间的时间间隔、样本冰镇运输以及使用如氰化钾和氟化钠等添加剂是可考虑的技术手段,用以减少假性低钾血症和假性低氧血症对白细胞增多症患者的影响。
要点回顾

本文编译自:Clinical Chemistry 69: 11 Clinical Case Study, 2023, 1220-1226.




